セファゾリンとエルタペネムによるサルベージ療法で持続性メチシリン感受性黄色ブドウ球菌血症を迅速に治癒が可能らしい
本記事は、医療従事者向けに記載をしております。また、本記事の内容は、私の所属している施設などとは一切関係がないことを併せてご承知の上、記事をご覧ください。
さて、今回は、感染症関連の雑誌に過去に掲載されていた論文の内容を記事にしていきます。
持続性メチシリン感受性黄色ブドウ球菌 (MSSA)血症に対してセファゾリンとエルタペネムによる併用療法で、治療が迅速に行えたという内容です。
タイトルの”サルベージ療法”は、がん領域の分野では良く使われるようです。もともとは、救援化学療法の意味で使用されています。
下記リンクにサルベージ療法について記載がされています。
主に造血器腫瘍において、治療の効果が得られない場合(治療抵抗性)、あるいは再発・再燃した場合に用いる治療を、救援化学療法もしくは救援療法と呼びます。
がんの種類によって治療内容は異なりますが、その多くは複数の薬(抗がん剤など)を組み合わせた治療となります。救済療法、サルベージ療法と呼ばれることもあります。
しかし、今回のサルベージ療法は”救援”というより、強化療法という意味合いで使用されているように思います。
もともと、MSSA感染症に対しては、ブドウ球菌活性を有するペニシリン系抗菌薬 (オキサシリン、ナフシリンなど)やセフェム系抗菌薬 (セファゾリンなど)の抗菌薬が使用されています。しかし、国内では、単剤でブドウ球菌活性を有するペニシリン系抗菌薬のオキサシリンやナフシリンの上市はない状態が長年続いています。このため、日本国内では、MSSA感染症といえば、セファゾリンが使用されることが多いです(感受性があれば、アンピシリン/スルバクタムが使用されることもあります)。β-ラクタム系抗菌薬にアレルギーがある場合のMSSA感染症に対しては、抗MRSA薬が使用されることが主流かなと思います。
そもそも、黄色ブドウ球菌は皮膚の常在菌です。何らかの原因で、皮膚軟部組織感染症、菌血症、骨髄炎、感染性心内膜炎など、多岐にわたる感染症を引き起こす可能性があります。特に菌血症を伴うような感染症では、急激に悪化し、致命的な経過を辿ることも良くあります。このため、黄色ブドウ球菌による感染症が発生した場合は、早期から適切な治療を行う必要があります。
黄色ブドウ球菌については、下記リンクのプロが書いた記事を参照ください。私なんかが記載しているよりも遥かにわかりやすいです。
黄色ブドウ球菌感染症に対する適切な治療とは何か?ということですが、なかなか難しいですが、適切な抗菌薬で早期から治療を行うことが大前提。また、感染症の種類によって、対応は異なります。例えば、血流感染症では、適切な抗菌薬による治療開始後、早期に、血液培養(血液に菌がいるかを調べる検査)を再検査し、陰性化(血液の中に菌がいない状態)を確認する必要があります。菌血症と診断された症例で、血管内にカテーテルを留置している場合は、カテーテル抜去+血液培養陰性化確認が原則必要になりますし、感染症の種類により、対応は大きくことなります。
治療期間なんかも、菌血症であれば、血液培養の陰性化を確認した日(検査を行った日)から14日間の治療が必要とされていますし、骨髄炎などでは、長期間 (患者の経過にもよりますが、最低6〜8週間、状態によりさらに長期間)の治療が必要だったりします。
こんな、治療が面倒な黄色ブドウ球菌のうち、MSSA感染症に対する治療オプションとして、併用療法により、治療が強化できるのではないかという報告です。
そもそも、セファゾリンは、セフェム系抗菌薬のうち、第1世代のセフェム系抗菌薬です。セファゾリンの特徴は下記図のとおりです(7年以上前に作成した院内勉強会向けのスライドです。下手くそな資料ですみません)

こんなセファゾリン単剤では、治療に失敗する可能性があるなどとの報告もあるのは確かです。このため、特に感染性心内膜炎などでは、アミノグリコシド系抗菌薬のゲンタマイシンや整形領域の感染症などでは、リファンピシンなどとの併用療法が報告をされています。これは相乗効果が臨床的に認められたり、in vitroで認められたりしているためです。
今回読んだ論文では、カルバペネム系抗菌薬のエルタペネムとの併用でセファゾリン単剤よりも効果が良いのでは?!というような内容でした。
エルタペネムは日本では、上市されていません。このため、日本国内では使用できません。カルバペネム系抗菌薬は、メロペネムやドリペネム、イミペネムなどが非常に良く知られているかと思います。
カルバペネム系抗菌薬の一般的な特徴は、
・抗菌スペクトラムが広い→グラム陽性菌、陰性菌に対して幅広く作用。グラム陰性菌は、緑膿菌までもカバーできる。
・安全性が非常に高い
・バルプロ酸との相互作用がある
などかと思います。
エルタペネムは、上記のカルバペネムとは一部特徴が異なり、緑膿菌に作用しないという特徴があります。このため、ESBLの治療などには、緑膿菌カバーを外せるということで、抗菌薬適正使用の観点から、海外ではESBL産生菌に対しては使用されているというのが現状です。
その辺は、下記リンクの内容を参照ください。参考になると思います。
そんな、今回読んだ論文の内容は・・・
エルタペネムをセファゾリンと共に併用すると、ダブルβ-ラクタムとなるが、相乗効果、相加作用がin vitroおよび動物実験では認められ、患者での後ろ向きの観察でも有効性があったよ
という内容です。
では内容を記載していきます。
Cefazolin and Ertapenem Salvage Therapy Rapidly Clears Persistent Methicillin-Susceptible Staphylococcus aureus Bacteremia
セファゾリンとエルタペネムによるサルベージ療法で持続性メチシリン感受性黄色ブドウ球菌血症を迅速に治癒
Erlinda R Ulloa, Kavindra V Singh, Matthew Geriak, Fadi Haddad, Barbara E Murray, Victor Nizet, George Sakoulas, Cefazolin and Ertapenem Salvage Therapy Rapidly Clears Persistent Methicillin-Susceptible Staphylococcus aureus Bacteremia, Clinical Infectious Diseases, Volume 71, Issue 6, 15 September 2020, Pages 1413–1418,
https://doi.org/10.1093/cid/ciz995
下記より要旨は見れ、2020年9月23日時点は、PDFで本文を無料閲覧可能(supplementary dataは無料での閲覧不可)
要旨
セファゾリンとエルタペネムの併用療法は,持続性メチシリン感受性黄色ブドウ球菌(MSSA)菌血症11例(心内膜炎6例)の救命に成功し,8例では24時間以内に即時消失した。in vitroでの相乗効果は控えめであったが,ラットのMSSA心内膜炎モデルでは,cefazolinとertapenemの相乗効果が認められた。セファゾリンとエルタペネムの組み合わせは,in vitroで予測された以上のMSSAに対するin vivoでの強力な活性を示し,難治性MSSA菌血症および心内膜炎の治療におけるさらなる臨床試験を保証するものであった。
本文
黄色ブドウ球菌は菌血症の主要な原因であり、高リスク患者において重大な罹患率および死亡率を引き起こす [1、2]。持続性メチシリン感受性黄色ブドウ球菌(MSSA)菌血症の管理は、外科的な感染源の管理と、古典的な抗ブドウ球菌薬(例えば、オキサシリン、ナフシリン、フルクロキサシリン)またはセファゾリンを用いたβ-ラクタム療法の早期開始に基づいている[3]。後者の使用が増加しているが、感染性心内膜炎のようにMSSAの接種菌量が高い感染症は、セファゾリンを投与されている患者では臨床治療の失敗と関連している[4-7]。MSSAに対する最適でない治療は臨床的に壊滅的な結果をもたらす可能性があるが、現在のところ、高接種菌量のMSSAに対する最適な治療レジメンに関するガイダンスはない。
私たちは以前、セファゾリンにエルタペネムを加えることで、この薬剤の組み合わせが外科的な病巣のない持続性菌血症に対するサルベージ療法に成功した患者のMSSA血流分離株に対してin vitroおよびin vivoでの相乗効果が得られたことを報告しました[8]。我々は難治性 MSSA 菌血症に対するこのサルベージ療法レジメンで高い成功を経験し続けている。ここでは、難治性 MSSA 菌血症の 11 例のサルベージ療法としてセファゾリン+エルタペネムを使用した臨床経験を報告し、in vitro およびラットの心内膜炎モデルでこの併用療法を検討する。
METHODS
Patient Cases
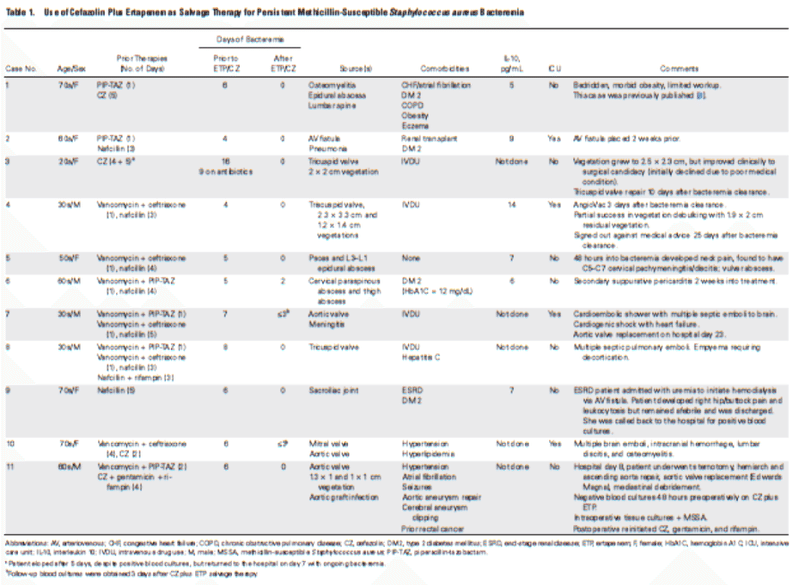
持続性MSSA菌血症の患者は、治療担当医(著者G.S.およびF.H.)を通じて特定され、以下のデータがレトロスペクティブに収集された:患者の年齢、菌血症の原因、菌血症の持続期間、血液学的および化学的検査、および菌血症を除去できなかった以前に投与された抗菌薬。症例報告に記載された11人の患者のうち、9人は日常的な臨床管理の一環として毎日血液培養を行っており、これにより菌血症の持続期間を評価することができた。そのうち2名の患者では、血液培養は最後の陽性から最初の陰性まで3日間の間隔で行われており、特定の菌血症の持続時間を測定することができなかった。これらの詳細は臨床要約(Table 1)に記載されている。エルタペネムとセファゾリンで治療された患者はすべて含まれており、症例報告から除外された患者はないことは注目すべき点である。データ収集の迅速承認は、the Sharp Healthcare内部審査委員会によって与えられました。
Bacterial Strains and In Vitro Assays
初期血液培養から分離されたMSSA(MicroScanを用いた臨床検体のルーチンワークアップにより臨床微生物検査室で分離・同定された)を6例の臨床例から得て,セファゾリン,エルタペネムおよびナフシリンに対するin vitro感受性を、標準的な Clinical and Laboratory Standards Institute(105 colony-forming units [CFU]/mL)および高接種(107 CFU/mL)条件下で、標準的なミューラー・ヒントンブロス(MHB)細菌学的培地およびロズウェルパーク記念研究所(RPMI)生理的細胞培養培地を使用して、5%ルリア・ベルターニ(LB)ブロスを補充した条件下で使用し [9]、評価した。チェッカーボードアッセイもまた、MHB中の標準および高濃度の接種液を用いて実施した[10]。殺傷曲線の研究のために、細菌を37℃のTodd-Hewitt broth中で一晩培養し、静止相に振盪して、MHBまたはRPMI + 5% LBで600 nm = 0.40の光学密度に希釈した。培養液はMHBまたはRPMI+5%LBで希釈し,1×107 CFU/mLの初期接種液とした。抗菌薬をMICの1/4になるように添加し、37℃で振とう培養器に入れた。アリコートを6時間および24時間後に採取し、CFUの計数のために連続的に希釈した。これらのデータは、少なくとも技術的には3回の生物学的レプリケートで実施された少なくとも3回のレプリケートから収集された。すべての抗菌薬は、Sharp Memorial Hospital pharmacy(カリフォルニア州サンディエゴ)から購入し、臨床使用および患者への投与に利用可能なバイアルとして供給した。セファゾリンとエルタペネムの間のディスク拡散シナジーアッセイを、以前に記載されているように行った[8]。簡単に言えば、0.5 McFarland(108 CFU/mL)の細菌懸濁液を、脳-心臓輸液寒天プレート上の芝生としてストリークした。
セファゾリンまたはエルタペネムのディスクをプレートの中央に置き、1時間後に新鮮なセファゾリンのディスクと交換した。阻害ゾーンの直径は、37℃で24時間インキュベーションした後に測定した。シナジーは、単一の抗菌ディスクと比較して、異なる薬剤のディスクを連続して使用した場合に、ゾーンサイズが3mm以上増加したと定義した。ディスクは、Hardy Diagnostics(サンタマリア、カリフォルニア州)から購入した。
Rat Aortic Valve Endocarditis Model
よく特徴づけられたMSSA株TX0117(A型β-ラクタマーゼを有し、セファゾリンの接種効果を示す)[4,11]を、雄のSprague-Dawleyラット(体重200g)を用いた心内膜炎の確立されたモデルで研究した[4,11,12]。細菌接種から30時間後、治療は、8時間ごとにエルタペネム30mg/kgSC、8時間ごとにセファゾリン50mg/kg筋肉内投与、または上記の用量および間隔でのセファゾリン+エルタペネムの組み合わせで開始された。投与量は、抗菌性治療薬を評価するためのこのモデルの先行使用に基づいて選択された(著者K.V.S.、B.E.M.)。抗菌薬治療を3日間行い、最後の抗菌薬投与から約15時間後に動物を死滅させ、大動脈弁およびその周辺組織に形成されたVegitationsを無菌的に除去し、重量を量り取り、0.9%生理食塩水1mL中でホモジナイズした。均質化した組織を連続的に希釈した後、各希釈液の全量(未希釈試料を含む)をBHI寒天にプレートした。Vegitationsから回収したコロニーから幾何平均log10 CFU/gおよび標準偏差を計算し、処理群を無処理対照群と比較した。
動物は、カテーテルが左心室の大動脈弁を横切って見つかった場合にのみ、最終解析に含まれ、治療の最初の24時間を超えて生存したラットのみが治療群に含まれた。この方法による細菌の最小検出限界は、組織の10 CFU/gであった。結果は、以前に記載されたように分析した[4, 11, 12]。
Statistical Analyses
統計解析は、GraphPad Prism、バージョン7.0dを用いて行った。P値<.05は有意であると考えられた。
RESULTS
持続性MSSA菌血症は,セファゾリン+エルタペネム併用療法により,合計11例が消失した(Table 1)。すべての分離株は臨床微生物学的検査ではメチシリン感受性であった。Table 1に記載された最初の症例は、以前の症例報告[8]からのものである。菌血症の持続期間の中央値は6日(範囲4~9日)であり,セファゾリン+エルタペネムによる救済療法の前に抗菌薬を投与していた。感染性心内膜炎は、これらの症例のうち6例で心エコー検査で確定的に確認されたが、そのうち2例は心臓のVegitationsが2cm以上の大きさであった三尖弁心内膜炎であった。驚くべきことに、これらの2例ではサルベージ療法開始後24時間以内に菌血症が消失した。血液培養が毎日行われた9例のうち、8例(88%)で24時間以内に菌血症が消失した。2例では、血液培養がサルベージ療法開始3日目まで行われていなかったため、菌血症の正確な期間を定義することはできなかった。この症例報告に含まれている患者は、結果の指標が事前に指定されている臨床試験に登録されていなかったが、すべての患者は退院まで生存していた。
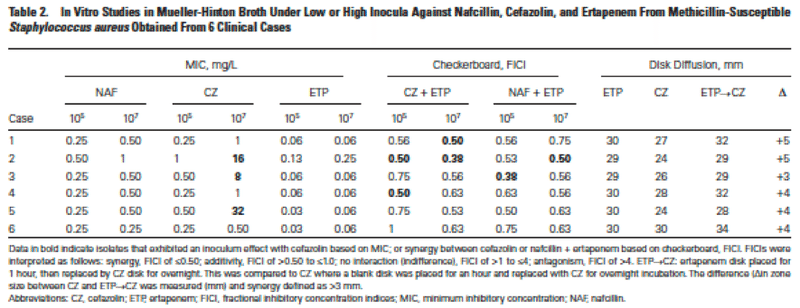
6つの分離株のセファゾリン,エルタペネムおよびナフシリン活性のin vitro評価をTable 2に示した。6株中3株はセファゾリンで有意な接種効果を示し,107 CFU/mLと105 CFU/mLを用いて感受性試験を行った場合には,MICが3倍以上高くなっていた(Table 2)。セファゾリンのMICは8 mg/Lから32 mg/Lの範囲であった。ナフシリンとエルタペネムは接種効果 (inoculum effect)を示さなかった。チェックボード試験では,分画阻害濃度指数の計算に基づいて,エルタペネムとセファゾリンまたはナフシリンとの間で,一般的な親和性が認められ,いくつかの相乗効果が認められた(Table 2)。ディスク拡散アッセイでは,セファゾリンのディスクを寒天プライミングの有無にかかわらず使用し,エルタペネムのディスクを1時間置き,阻害領域を比較した(Table 2)。すべての分離株で、エルタペネムのプライミングにより、セファゾリンの阻害領域が少なくとも4mmの増加を示した。
我々や他の研究者は最近、重炭酸緩衝バクテリア培地や生理学的に関連する組織培養ベースの培地で得られた感受性試験結果が、生体内での抗菌薬活性をより反映していることを認識している[13-15]。
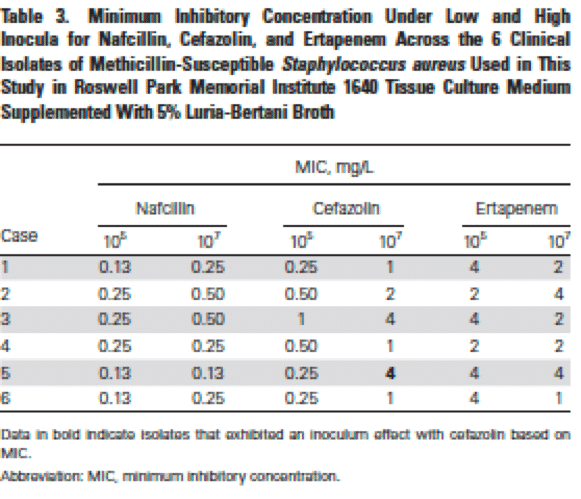
そこで,セファゾリン,ナフシリンおよびエルタペネムの感受性試験を,5%LBを添加したRPMI培地を用いて,標準および高接種条件で実施した(Table 3)。セファゾリンおよびナフシリンについては,標準接種条件のRPMI+5%LBで得られたMICは,標準MHBで得られた結果と同様であった。症例2および症例5の分離株は,高接種条件でRPMI+5%LBではMHBと比較してセファゾリンのMICが8倍に低下していた。MHBで非常に高いセファゾリンMIC(32 mg/L)を示し,高菌種接種下で試験した症例5のMSSA分離株のみが,RPMI+5%LBで有意な接種効果を示した(セファゾリンMIC 4 mg/L)。しかし,RPMI + 5% LB培地では,標準菌接種と高菌接種の両方の試験で,すべての分離株にはるかに高いエルタペネムMICが認められた。標準的な菌株を用いた場合,RPMI + 5% LBで観察されたエルタペネムのMICはMHBの15~133倍であった。
最も困難な高接種量のMSSA感染をシミュレートするために,Table 1に記載された症例1~6の臨床株に対して,標準接種量(105 CFU/mL)に加えて,エルタペネムとセファゾリンを単独または併用して,107 CFU/mLの接種開始時の殺傷曲線を実施した.
結果を補足 Figure 1 に示し,左が MHB での実験,右が RPMI + 5% LB での実験のデータを示した。MHBおよびRPMI + 5% LB培地では,エルタペネムとセファゾリンは6株の間で異質な結果を示し,一部の株では24時間時点で相乗効果(最も活性の高い抗菌薬単独と比較して,併用で2対数10以上の殺傷効果を示す)[16]を示したが,そうでない株もあった.ほとんどの株は 24 時間後に再生を示した。また、MHB と RPMI + 5% LB の両方で、エルタペネムとナフシリンを単独または併用して同様の方法で 2 株を検討した(補足図 2)。両菌株とも、RPMI + 5% LBでのエルタペネムとナフシリンの併用との相乗効果を示し、24時間で約2 log10の殺虫効果を示したが、高接種量(107 CFU/mL)でのみ殺虫効果が認められた。
心内膜炎モデルにおけるセファゾリンとエルタペネムの単独および併用の結果を図1に示す。
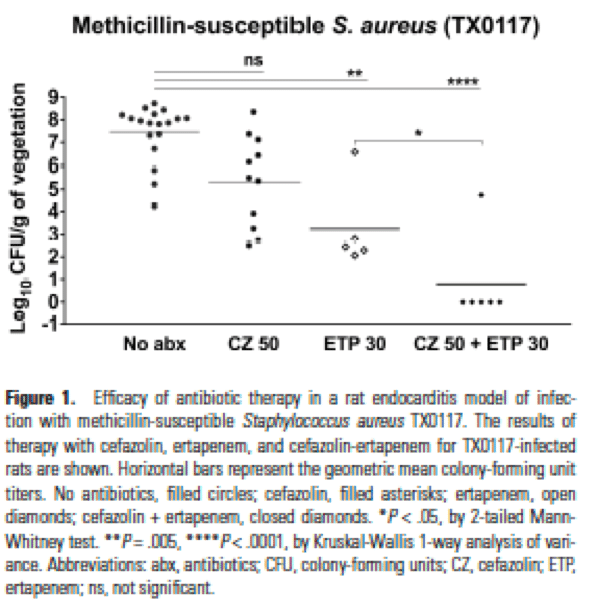
エルタペネムの存在下では、1弁を除くすべての弁の細菌接種は検出限界以下に減少した。セファゾリンをエルタペネムに添加すると、セファゾリン(P = 0.0591)またはエルタペネム(P = 0.005)単独投与群と比較して、活性が増加する傾向にあった(P < 0.0001)。さらに、エルタペネム治療群をセファゾリン+エルタペネムの条件と比較したときに、結果は統計的に有意になった(P < 0.05)。
DISCUSSION
セファゾリンは、菌血症、心内膜炎、骨髄炎などの重篤な MSSA 感染症の治療に使用され、推奨されることが増えている。実際、最近の研究では、オキサシリンやナフシリンなどの古典的な抗ブドウ球菌β-ラクタム薬と比較して、セファゾリンを投与された患者の忍容性が向上し、おそらく良好な転帰が得られることが示されている[17-19]。セファゾリンに関するこれらの好ましいデータは、レトロスペクティブに収集されたものであるためにやや限定的であり、したがってバイアスがかかりやすい(例えば、リスクの高い患者は、セファゾリンよりも抗ブドウ球菌薬のβ-ラクタムの投与に偏りがあるかもしれない)。しかし、特に高齢者を中心としたより重篤な感染症では、4週間以上の治療期間が必要とされるため、セファゾリンの忍容性がより良好であることが示されている。例えば、骨髄抑制および急性腎障害は、セファゾリンでは古典的な抗ブドウ球菌性β-ラクタム系抗菌薬よりもはるかに少ない[17-19]。しかしながら,いくつかのMSSA(例えば,A型β-ラクタマーゼ産生株)に対しては,高接種条件でのセファゾリンの活性が劣るため,治療の失敗が懸念されており,文献にも記載されている[4-7]。高レベルの集団データでは、このような分離株があまり一般的でない場合、セファゾリン接種効果を示すMSSAによる個々の症例が強調されない可能性があり、最近の研究では、これらの分離株はある環境では一般的であっても、他の病院センターではかなり稀であることが示唆されている[20-23]。黄色ブドウ球菌のinoculum effectsは、最近、β-ラクタム/β-ラクタマーゼ阻害剤の組み合わせを含む追加のβ-ラクタム系薬剤についても示されている[24]。MSSAに対する最適でない抗菌薬治療は、心内膜炎や硬膜外膿瘍などの非常に重篤な感染症で壊滅的な臨床結果をもたらす可能性がある。本研究で検討した6株のMSSAのうち3株がセファゾリンのinoculum effectを示したが、RPMI+5%LB培地でセファゾリンの接種効果を示したのは症例5のみであったことは注目に値する。この症例の患者は、エルタペネム中止後、数日後に再入院を余儀なくされたが、セファゾリンは単剤治療のままであったことを強調している。臨床的に有意なセファゾリンの接種効果がRPMIのような生理学的媒体での試験を保証するかどうかは、今後の研究のための潜在的なトピックであり、特にセファゾリンが複雑なMSSA感染症の治療法として古典的な抗ブドウ球菌用βラクタム薬に取って代わることになった場合には、その可能性があります。
本研究では,セファゾリン+エルタペネム併用サルベージ療法により,標準的な単剤治療が不合格となった患者においても,心エコー図上で大きな負担のある血管内感染を認めた症例では,MSSA菌血症の迅速なクリアランスが可能であることを示した。MSSAに対するセファゾリンとエルタペネムの適度な相乗効果や親和性が,細菌学的培地(MHB)と生理学的培地(RPMI)の両方を用いたin vitroで観察された。ディスクディフュージョン法、チェッカーボード法、タイムキル法によるin vitroでの相乗効果試験ではかなりの不一致が見られたため、これらの試験結果が、in vivoでのセファゾリンとエルタペネムの間の強力な相乗効果を評価する上で、臨床的にどの程度の意味があるのか、またラットの心内膜炎モデルでは有意な相乗効果が確認されたことが疑問視された。これらの累積結果に基づき、セファゾリン+エルタペネムは、適切な外科的ソースコントロールが行われていれば、標準的なβ-ラクタム療法に抵抗性のあるMSSA菌血症患者において、実行可能なサルベージレジメンの選択肢を提供すると考えられる。1つの細菌株で得られた臨床データとラット心内膜炎モデルのデータは、エルタペネムとセファゾリンの併用がより有効であるという仮説を支持するものであったが、in vitroでのデータは説得力に乏しく、株やアッセイ間の相関関係は限定的であった。
この組み合わせを選択した当初の理由は、相補的なペニシリン結合タンパク質(PBP)結合性を有する2種類のβ-ラクタム系抗菌薬による治療を提供することで、細胞壁合成の複数のステップを同時に標的にして殺傷力を高めることであった [25]。具体的には、カルバペネム系抗菌薬は、黄色ブドウ球菌の必須PBPであるPBP1との親和性が非常に高く、抗ブドウ球菌β-ラクタム系抗菌薬のそれをも凌駕している[25, 26]。これは、セファゾリンの相対的なPBP2陽性率を補完するものであろう[27]。Enterococcus faecalisによる心内膜炎の治療にアンピシリンとセフトリアキソンを使用することは、同様の根拠に基づいており、より優れた忍容性のため、この疾患における毒性のあるアミノグリコシド療法は段階的に廃止されつつあります[28]。我々のin vitro試験では、試験した分離株に対する拮抗作用の証拠はなく、相加性または相乗効果が示された。しかし、心臓のVegitationsの大きさが2cmを超える患者では、24時間以内に菌血症が消失するという結果は、in vitro試験での予想をはるかに上回っており、さらなる研究が必要な追加要因が関与している可能性が示唆されている。
生体内での深遠な効果の一つの可能性は、両方の抗菌薬にさらされたMSSAが自然免疫系に感作されていることかもしれない。この現象は、我々の先行研究で説明したが、症例1のMSSAは、セファゾリンとエルタペネムの両方のサブMIC濃度に曝露した場合、どちらかの薬剤単独の場合と比較して、ヒトカチオン性宿主防御ペプチドであるカテリシジンLL-37、または多くの抗菌因子を産生する好中球によって、より効果的に死滅した[8]。別の可能性としては、エルタペネムの添加によるPBP1、S. aureusにおける唯一の必須PBPの非常に強力な干渉が、特に別のβ-ラクタムがそれらの機能にも干渉している場合には、他のPBPによって補償することができないいくつかの細胞生存率の閾値を超える可能性がある。最後に、我々の広範な文献のレビューでは、セファゾリンの主要な標的であるPBP2の発現が好中球の存在下で減少することが明らかにされている[27]。このように、人工的に作られた細菌培地での抗菌活性の評価は、生体内で発生する細胞壁の動的変化を調べるには不十分かもしれません。セファゾリン-エルタペネム相互作用については、エルタペネムは、細菌性心内膜炎Vegitationsなどの微小環境で発生している可能性がありますセファゾリンの比較的減衰した活性を「救助」するのに役立つ可能性がある。Vegitationsに存在する自然免疫の成分の存在下でのセファゾリンの相対的な活性を調べるためには、さらなる研究が必要である。
以上のように,セファゾリン+エルタペネム併用療法で迅速な菌血症クリアを達成した難治性MSSA菌血症患者を連続して治療した症例を紹介した。MSSAに対するセファゾリンとエルタペネムの間には、in vitroで相乗効果や親和性が観察され、ラット心内膜炎モデルでの研究でもその効果が確認された。in vitroアッセイで予測された以上の強力な効果がin vivoで観察されたことに基づいて、我々は、以前に記載されているように、セファゾリンとエルタペネムを併用した場合、生体内での自然免疫との協調性が細菌の殺傷にも役立つのではないかという仮説を立てた[8]。エルタペネムとセファゾリンまたは他の抗ブドウ球菌用βラクタム薬との併用療法は、MSSA菌血症および心内膜炎の難治例におけるこれらの併用療法の役割を確立するために、臨床現場でより広範囲に評価されるべきである。
よろしければサポートお願いします。 サポートいただいた費用で、論文の取り寄せ等に使わせていただき、記事を充実させていきます。
