COVID19ワクチン接種後の腎臓の病気 1
こんにちは。新型コロナウイルス感染症でも腎臓に感染症の影響が出ると症状が重くなります。しかし、コロナワクチン接種後に腎臓の病気になった人たちの報告も多数あり、軽症とはいいがたいものが含まれています
はじめに 腎臓の構造と働き
腎臓は2つの豆のような形をした臓器で、それぞれこぶし大の大きさです。胸郭のすぐ下にあり、背骨の左右に1つずつあります
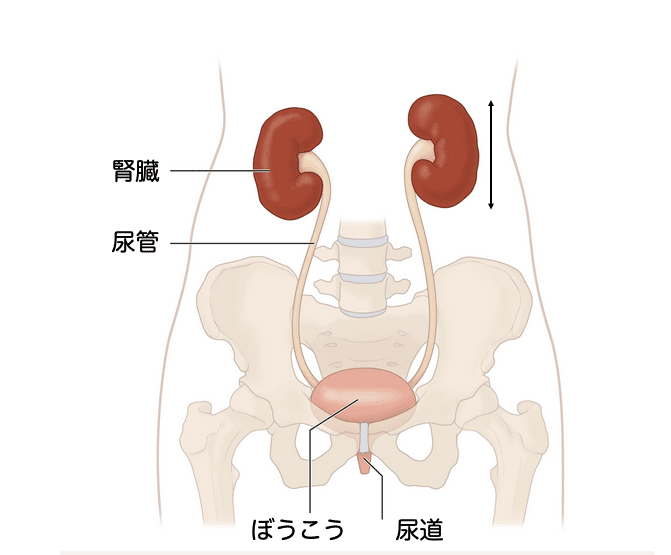
健康な腎臓は、1分間にコップ半分の血液をろ過し、老廃物と余分な水分を排出して、尿をつくります。尿は、腎臓からぼうこう (膀胱) へ、両側に1本ずつある尿管と呼ばれる筋肉の細い管を通って流れ、ぼうこう に貯まります
なぜ腎臓は大切なのか?
腎臓は、老廃物や余分な水分を体外に排出しています。また、体内の細胞から発生する酸を取り除き、血液中の水分、塩分、ミネラル(ナトリウム、カルシウム、リン、カリウムなど)の健康的なバランスを維持します
このバランスが保たれていないと、神経や筋肉などの組織が正常に働かなくなる可能性があります
腎臓はまた、次のようなホルモンを作っています
血圧のコントロール
赤血球を作る
骨を健康に保つ
ここまでの説明を英語スピーキングで見る youtubeリンク
腎臓はどのように機能しているのですか?
腎臓はそれぞれ、ネフロンと呼ばれる約100万個のろ過装置から構成されています。それぞれのネフロンには、糸球体と呼ばれるフィルターと尿細管があります。ネフロンは、糸球体で血液をろ過し、尿細管で必要な物質を血液に戻し、老廃物を除去するという2段階のプロセスで機能しています
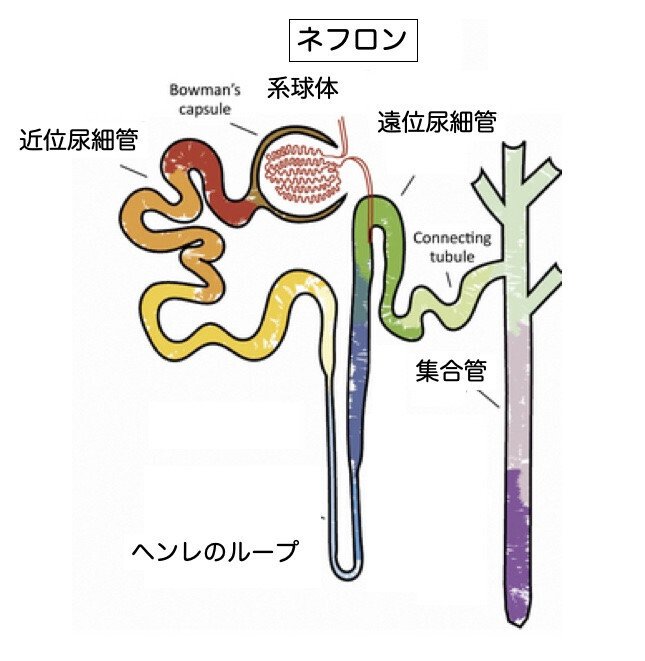
それでは、コロナワクチン接種後に出現した腎臓の障害について説明します
ワクチン接種後の急性腎障害 AKI
症例. 77才白人男性
基礎疾患:2型糖尿病 (15年前より, 網膜症や蛋白尿や血清クレアチニン値上昇を伴わない), 肥満, 喫煙歴、冠動脈疾患
BNT162b2ワクチン初回接種7日後、突然の下肢浮腫あり,蛋白尿は4+,血清アルブミン2.5 g/dlであった.
同12日後, 浮腫による体重増加13.6kg、血圧(152/81mmHg)、尿検査で4+の蛋白尿、尿沈渣が不活性のため、入院となる
同14日後の検査では,24時間尿蛋白23.2 g/dl,血清クレアチニン2.33 mg/dl,血清アルブミン3.0 g/dlであった.全血球数は正常で,ヘモグロビンA1cは7.5%であった.血清検査では,補体C3,C4が上昇し,B型肝炎表面抗原,C型肝炎抗体は陰性であった.
同16日目に腎生検を実施した(図1 )
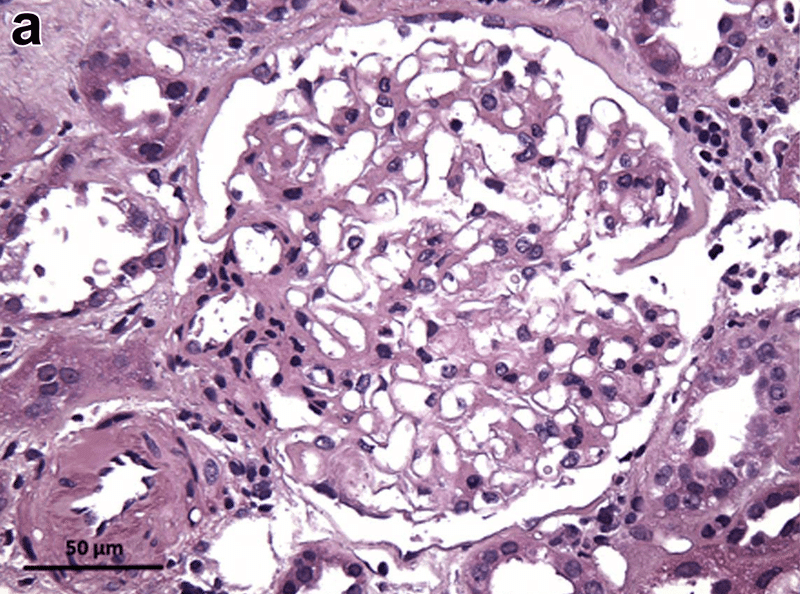
光学顕微鏡で観察した7個の糸球体のうち、4個は全体的に硬化しており、3個は組織学的に異常がなかった
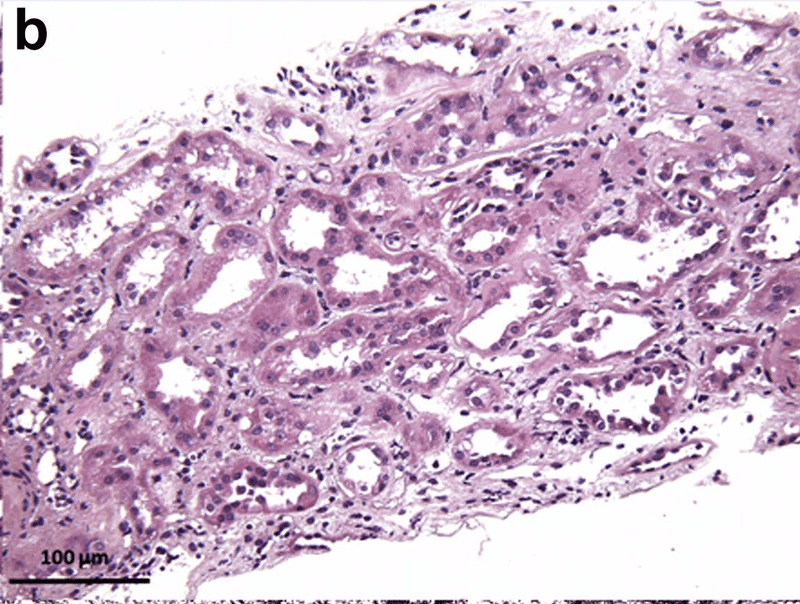
25%の尿細管萎縮と間質性線維化,中等度の動脈硬化を認めた.皮質尿細管にはびまん性の急性上皮障害がみられた.免疫蛍光法(2糸球体)および電子顕微鏡法(2糸球体)で免疫沈着は確認されなかった.
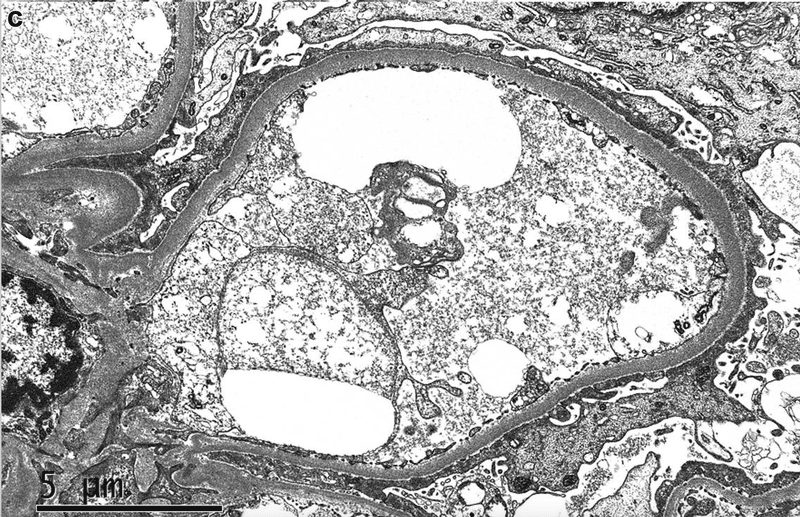
電子顕微鏡ではポドサイト足突起の脱落が100%認められ、急性尿細管損傷を伴うminimal change diseaseと診断された。超微形態学的所見として,微小な分節性メサンギウム硬化症と糸球体基底膜の肥厚(平均460nm)が認められ,軽度の糖尿病性変化が背景にあることが示唆された.
ステロイド治療が行われた
ワクチン接種後の急性腎障害AKI (小児)
症例. 12才健常男児。13カ月前、クレアチニン0.78mg/dL、蛋白尿陰性
基礎疾患なし
ワクチン接種前後に非ステロイド性抗炎症薬などの腎毒性を誘発する薬剤の使用なし
BNT162b2初回接種7日後、パラセタモールに抵抗性の頭痛,下肢浮腫が出現し,体重は65kgから76kgに著増し,全身浮腫に進行した
9日後の入院時、血圧 140/70mmHg,心拍数 80回/分。顔面,上肢,下肢の浮腫を認め,POC超音波検査で腹水が確認された
血清クレアチニン1.3 mg/dL,血清BUN 85 mg/dL,アルブミン2.2 g/dl,c3,c4正常,ANAおよびANCA陰性.SARS -CoV-2のPCR検査スワブは陰性。HBV、HIV、HCV、SARS-CoV-2の血清検査は陰性。スパイク蛋白サブユニットS1、S2のSARS-CoV-2の血清定性検査はIgGで陽性。尿検査では蛋白185mg/dL、β2ミクログロブリン45μg/L、尿沈渣では赤血球10~15個の異形が認められた。胸部X線は陰性であった.入院し、直ちにヒトアルブミン(0,5 g/kg)を点滴静注した。24時間採尿で86 mg/m2/hの蛋白尿が検出された
入院4日目に腎機能低下,血清クレアチニン 4 mg/dLに上昇。フロセミド,スピロノラクトン,チアジド利尿薬に抵抗し、呼吸困難と乏尿を伴う体液過多を呈した.
入院6日目に限外濾過による腎代替療法を開始し,腎生検が施行された.光学顕微鏡による検査では,軽度のメサンギウムの過細胞化,細胞質変性を伴う尿細管閉塞,内腔の剥離成分の存在のみが特徴である11個の糸球体が認められた.免疫蛍光法は陰性であった.電子顕微鏡では,リハッシュの様相を呈するGBM,蛇行を伴う毛細血管壁の伸展,ペディケルの崩壊,腫脹,広範な融合の様相を示し,電子密度の高い沈着は認められなかった.
ステロイド治療を開始し、ステロイド治療開始7日後,クレアチニン1.82 mg/dL,アルブミン3.2 g/dL,24時間採尿で蛋白58 mg/m2/hと腎機能が改善し始め,尿量が増加し,5回で腎代替療法を中止した.
入院15日目、体重10kg減、血清クレアチン0.8mg/dL、血漿アルブミン3.1g/dL、尿検査で蛋白尿消失、蛋白クレアチン比 0.5、血圧 正常となり退院した
保護者は2回目のワクチン接種に同意していない
診断は、急性腎障害(AKI)、minimal change disease(MCD)およびネフローゼ症候群(NS)
ワクチン接種後の急性腎障害AKI
症例. 50才男性
基礎疾患なし
ワクチン接種前後に非ステロイド性抗炎症薬などの腎毒性を誘発する薬剤の使用なし
BNT162b2初回接種4日後、下肢浮腫が出現し,急速に進行し全身性浮腫に進行した
入院時所見:接種10日後に入院, 下肢、手のひら、腹壁、陰茎に点状浮腫あり。腹部は膨満。両肺の基部にラ音。血圧 170/110mmHg、心拍数 80回/分, 血清クレアチニン 2.31 mg/dL,血清BUN 78 mg/dL,アルブミン1.93 g/dL,コレステロール484 mg/dL,トリグリセライド166 mg/dL, 24時間尿蛋白排泄量6.9 g, 尿蛋白(4+), 尿沈渣では高倍率視野あたり3~5個の赤血球(一部異形)、脂肪鋳塊、楕円形の脂肪体が認められた
HBV Hs抗原とHCVは陰性, 補体C3とC4 基準範囲内,。抗好中球細胞質抗体(ANCA),抗粒体基底膜(GBM)抗体,抗核抗体(ANA)は陰性。SARS-CoV-2のPCR反応と血清検査(Cobas Elecsys Anti-SARS-CoV-2 [Roche Diagnostics])は陰性.しかし,スパイク蛋白サブユニットS1,S2に対する免疫グロブリンG抗体価は38.9吸光単位/mlと陽性だった,胸部X線写真で両側胸水貯留あり.造影剤を用いないCT検査では,腎臓は正常で,尿路閉塞は認めなかった.
入院後に腎機能が低下し続け,4日目よりステロイド療法開始。
入院翌日の腎生検 Fig 2。24個の糸球体が検出され,1個は全体的に硬化しており,他は正常であった.糸球体毛細血管には軽度のうっ血がみられ,GBMの肥厚はみられなかった.間質は小さなリンパ球の浸潤が目立った。急性尿細管障害が広範囲に認められ,髄質には石灰化が始まっていた.免疫蛍光法で線状膜およびメサンギウムアルブミン、IgG(痕跡)、メサンギウムIgM(1+)、血管C3(1+)、管状IgG(痕跡)などが検出された。2個の糸球体を電子顕微鏡で観察した。GBMの厚さは360から550nmで、糸球体容積の約90%にわたってポドサイト脚突起のびまん性扁平化がみられた。電子密度の高い沈着物はなかったが、微小絨毛の変形を示す病巣があった。これらの所見は急性尿細管障害を伴うMCDと一致する
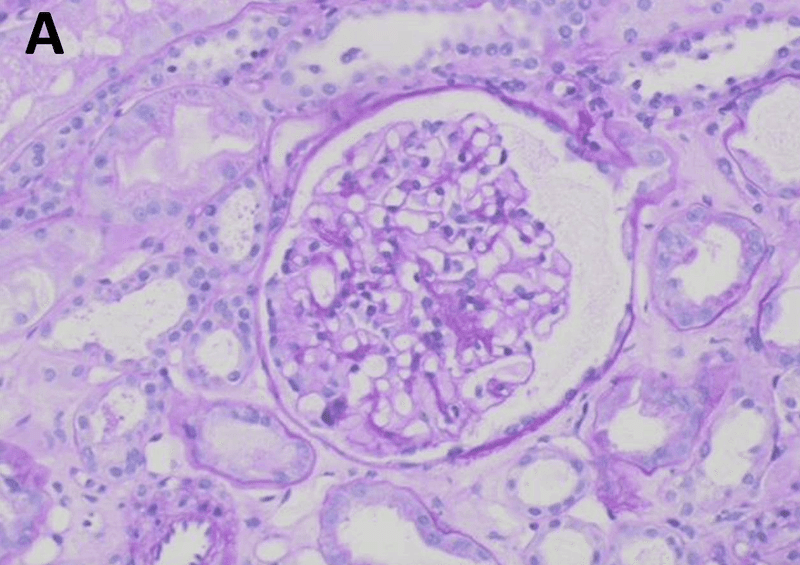
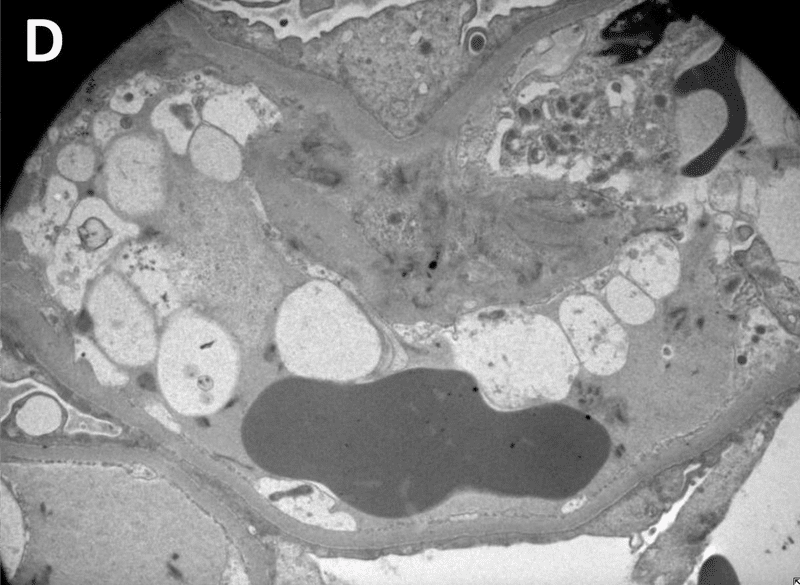
診断は、ネフローゼ症候群と急性腎障害(AKI)を伴うminimal change disease(MCD)
http://fujita2011.livedoor.blog/archives/51851289.html
ワクチン接種後の急性腎障害AKI _____________急性尿細管間質性腎炎
症例 63歳男性
既往歴なし。血清クレアチニン濃度は直近の臨床検査で正常範囲にあった.
患者は薬の服用を否定した
鼻咽頭拭い液からのRT-PCRはSARS-CoV-2陰性であった.患者は過去数カ月間のCOVID-19の症状を否定した
BNT162b2初回接種後3週目に倦怠感,無尿のため入院した
検査所見:初期血清クレアチニン濃度19.0 mg/dl,代謝性アシドーシス,9 mmol/lの高カリウム血症を伴う急性腎不全が認められた.
尿検査では亜硝酸塩陰性の白血球尿、血尿、蛋白尿(アルブミン/クレアチニン比(ACR)393mg/g、蛋白/クレアチニン比(PCR)787mg/g)
腎生検の結果,間質性浮腫,好酸性顆粒球を伴うリンパ球細胞間浸潤,急性尿細管壊死を伴う急性間質性腎炎(AIN)であった.
抗好中球抗体(ANA),抗好中球細胞質抗体(ANCA),IgG4,アンジオテンシン変換酵素(ACE),可溶性IL2受容体(sIL2R),免疫固定,ハンタウイルス血清検査に異常はなかった.
ICUでの腎代替療法とステロイド治療を行い、2週間後に血液透析を中止することに成功した.
診断は、急性腎障害AKINステージIIIを伴う間質性腎炎
ワクチン接種後の急性腎障害AKI _____________急性尿細管間質性腎炎
症例 18才男性
病歴なし
薬の服用なし
過去数ヶ月のSARS-CoV-2感染の症状はない。鼻咽頭ぬぐい液からのSARS-CoV-2 RNA PCRは陰性.SARS-CoV-2ヌクレオキャプシド蛋白に対する抗体の定量分析も陰性であった
2回目のBNT162b2ワクチン接種から約6週間後に,倦怠感と咳のためかかりつけ医を受診し、血清クレアチニン値 1.7 mg/dl上昇のため、当院腎臓内科に紹介された.
腎内初診:血清クレアチニン濃度の上昇、血尿、糖尿、蛋白尿(アルブミン/クレアチニン比(ACR)393mg/g、蛋白/クレアチニン比(PCR)787mg/g)
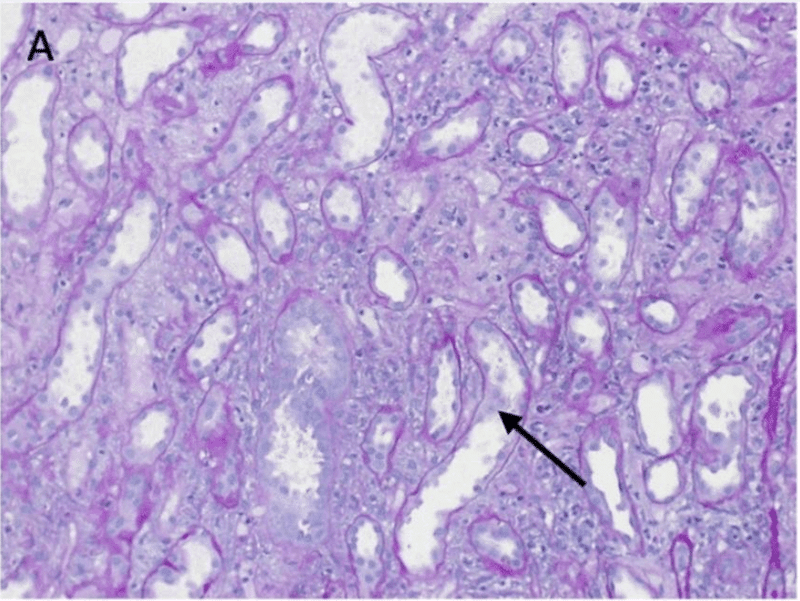
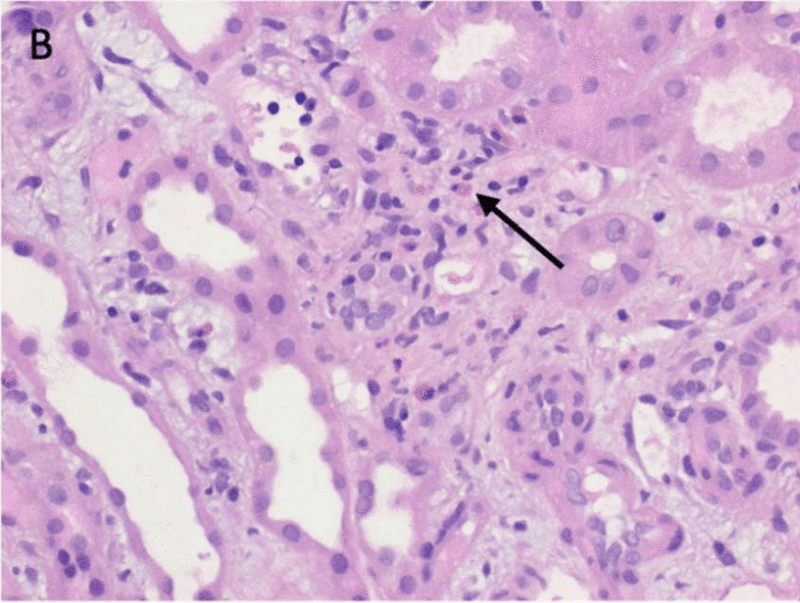
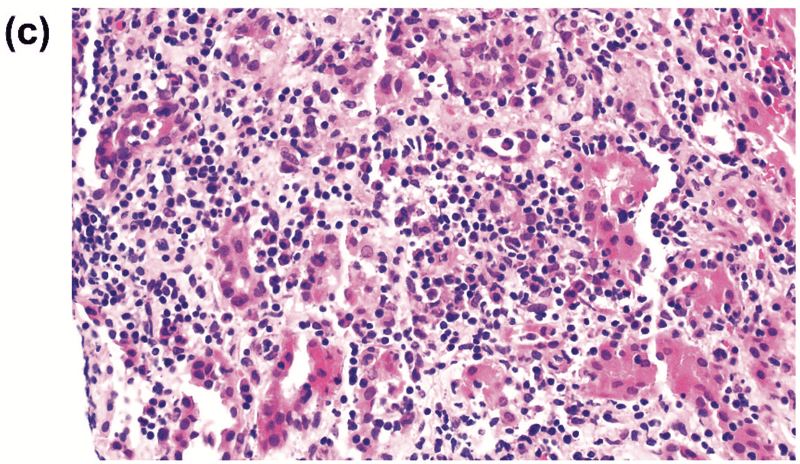
腎生検で好酸球を伴うリンパ球と形質細胞の浸潤、およびびまん性急性尿細管壊死を認めた(図C)。さらに、免疫組織化学的検査により、硬化、毛細管内増殖、クレッセントを伴わない軽度のメサンギウムIgA沈着が認められた(図D)。 AINの基礎となる全身性疾患を示すすべての検査項目は陰性であった
ステロイド療法により2週間以内に回復した
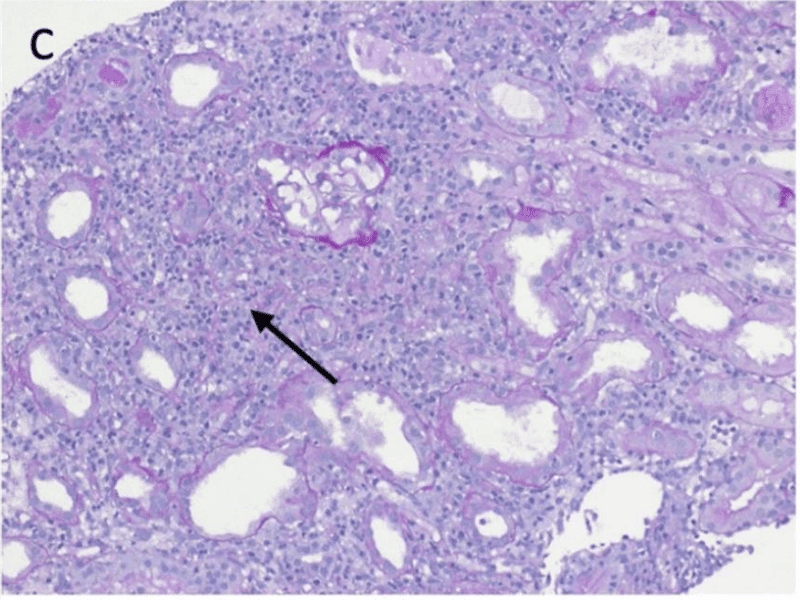
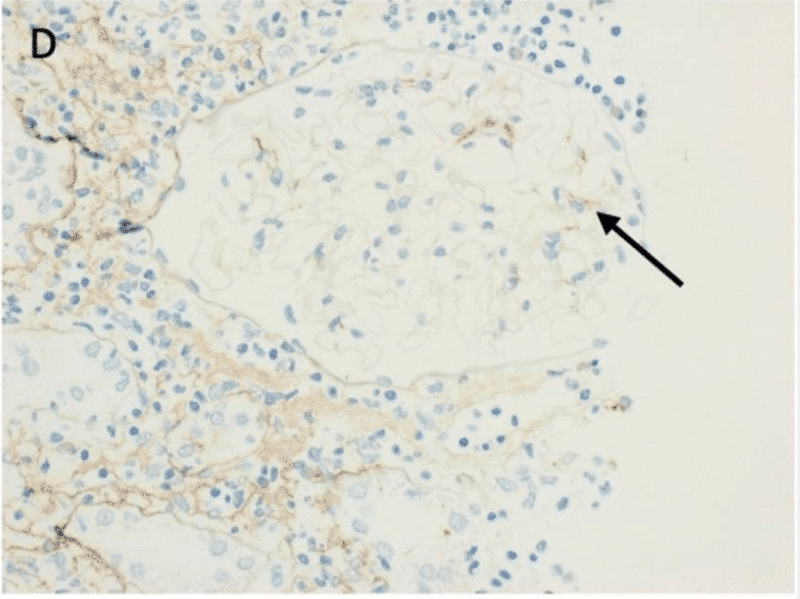
診断は、急性腎障害AKINステージIIIを伴う間質性腎炎
ワクチン接種後の急性腎障害AKI _____________急性尿細管間質性腎炎
症例 25才女性
既往なし, 薬歴に異常なし
COVID-19の症状は否定された.鼻咽頭ぬぐい液によるSARS-CoV-2 RT-PCRは陰性,SARS-CoV-2ヌクレオキャプシド抗体の補足分析も陰性
3回目のBNT162b2ワクチン接種後3週間目に,疲労感と全身倦怠感のため,かかりつけ医で初期血清クレアチニン濃度が11.7mg/dlで急性腎不全を発見され,当院腎臓内科に入院した.
尿検査で血尿,糖尿,蛋白尿(アルブミン/クレアチニン比(ACR)58 mg/g,蛋白/クレアチニン比(PCR)235 mg/g)がみられた.
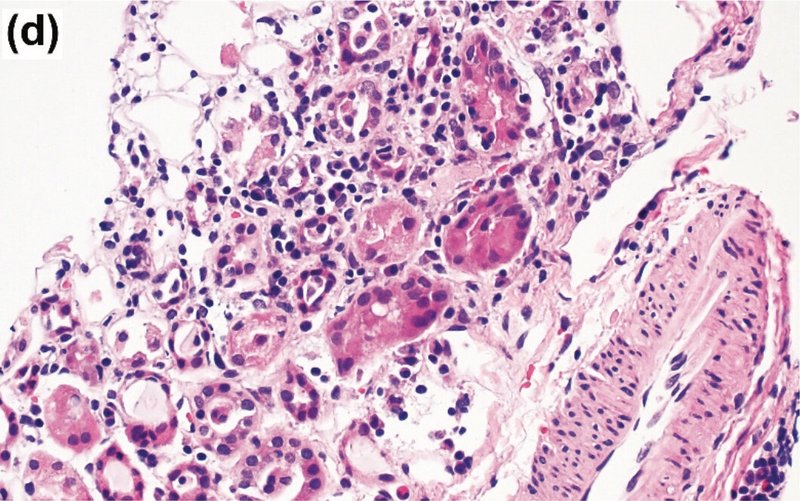
腎生検の結果、びまん性の急性尿細管壊死(図E)とわずかな好酸球増多(図F)を伴う重度の局所的破壊性間質性腎炎が認められた
AIN の病因の関連する全身性疾患に関連するすべての検査値は陰性であった
ステロイド療法にて数日で排泄性腎機能が漸次回復した.
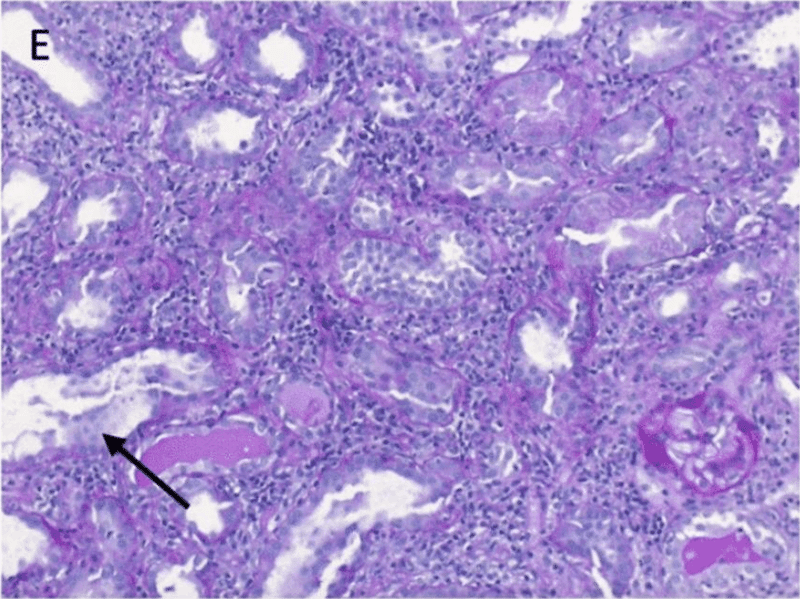
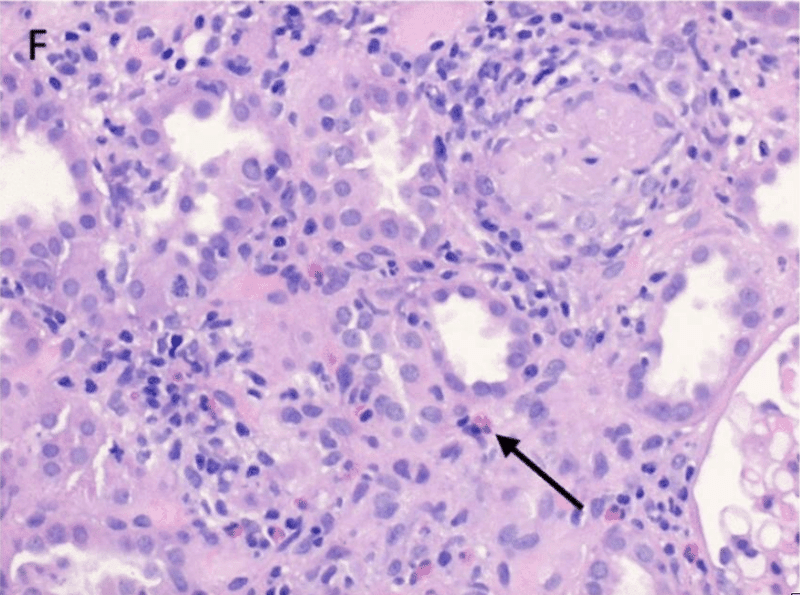
診断は、急性腎障害AKINステージIIIを伴う間質性腎炎
ワクチン接種後の急性腎障害AKI _____________急性尿細管間質性腎炎
症例. 44才女性
基礎疾患なし
漢方薬や医療用医薬品を用いた咳嗽なし
接種直後からのワクチンに関連する腕の痛み、発疹、頭痛、発熱などの急性副作用なし
BNT162b2ワクチン1回目接種から48時間後に突然の頭痛,発熱(38.4℃),悪心嘔吐,脱力感,下肢痛を訴えた
救急外来でヘモグロビン6.6 g/dl,LDH 2100 U/L,血清クレアチニン値2.1 mg/dl, 白血球増加(12.300 WBC/ml),CRP上昇(96.2 mg/dl)がみられ入院となった.クレアチンホスホキナーゼは正常範囲。
直接クームス試験陽性以外,溶血検査はすべて正常であった.
尿検査では,白血球尿,微小血尿,腎性蛋白尿(蛋白量:10.1 g/day)が検出された.尿培養では微生物所見は検出されなかった。
血清学的検査では補体は正常で,抗核抗体(ANA),抗好中球細胞質抗体(ANCA)は陰性であった.HIV、C型肝炎、B型肝炎の血清検査も陰性であった。さらに,感染巣は検出されず,炎症指標は疾患の退縮と並行して改善した.
腹部超音波検査では肝脾腫は認められず,両側の腎臓の大きさ,実質の厚さは正常範囲内であった.
入院翌日、無尿経過、血清クレアチニン値6.5mg/dlまで進行、代謝性アシドーシスの増加により急性血液透析(HD)が施行された。貧血のため赤血球懸濁液2単位を投与した
3回のHDの後、腎生検の結果、糸球体は保たれているものの、尿細管間質領域に広範な炎症と時折好酸球を検出した(図1)
ステロイド治療を実施した
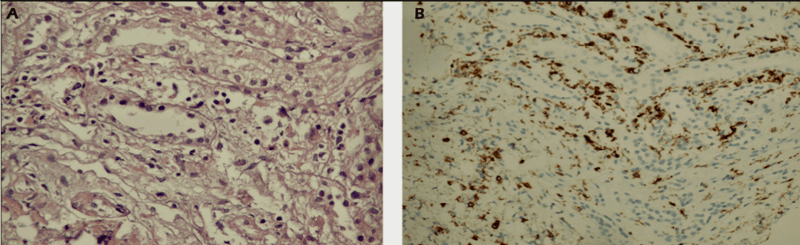
および間質性炎症細胞の CD45 染色 (×200 IHK) (B)
診断は急性腎障害をきたした急性尿細管間質性腎炎(ATIN)
ワクチン接種後の急性腎障害AKI _____________急性尿細管間質性腎炎
症例 17才男性
既往歴:なし。過去数か月間、ワクチン接種後に生じた発熱に対してアセトアミノフェンを1回服用した以外は、ハーブティーを含め一切の服用を否定していた。心肺症状も否定した
2021年11月8日にBNT162b2ワクチン2回目接種し、翌日,筋肉痛と38℃の発熱があったため,2021年11月10日にCOVID-19のPCR検査を実施し結果は陰性であった
2021年11月11日以降、心窩部痛と吐き気のため食事に支障をきたし、近隣の病院救急外来を受診し、血清Cr値 3mg/dLの腎不全を指摘された
2021年11月13日、腎不全と持続する胃腸障害のため、当院に転院した
初診時、血圧150/85mmHg、心拍数75回/分、呼吸数20回/分、体温36.9℃、室温での末梢酸素飽和度100%。体重95kg(99%以上)、身長178cm(75~90%)、BMI30.0kg/m2(99%以上)
心窩部圧痛と肋骨過角圧痛は両側とも陽性であった
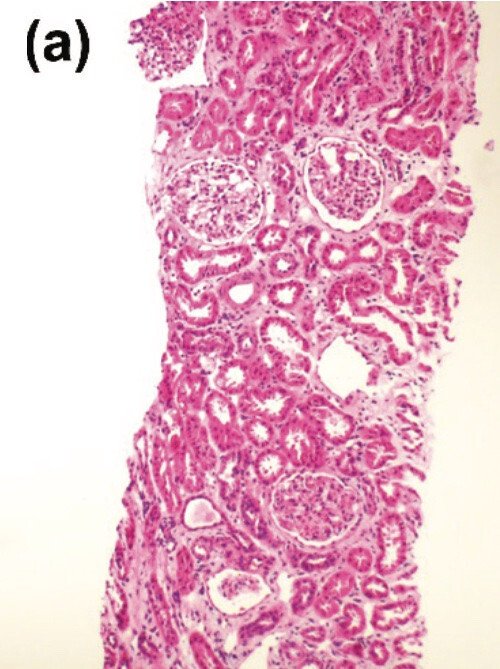
注:少し足突起の剥離が見られると思います。ご意見ありましたらコメントにお願いします
診断は、急性腎障害をきたした急性尿細管間質性腎炎(ATIN)。最初の小児症例である
ワクチン接種後の急性腎障害AKI _____________急性尿細管間質性腎炎
症例 12才男性
既往歴:なし、過去数ヶ月、ワクチン接種後に発生した嘔吐に対してトリメブチンとドンペリドンを3日間投薬した以外は、ハーブティーを含め一切の服用を否定していた。心肺機能の症状は否定した。慢性腎臓病や高血圧の家族歴はなかった
患者は2021年12月24日にCOVID-19ワクチンの2回目の接種を受けた。翌日から、吐き気、1日4回程度の胃液を伴う嘔吐、経口摂取不良が出現した。食欲不振と嘔吐が続くため、近くのクリニックを受診。血液検査を実施し、2022年1月11日にCr値2.28mg/dLの異常値を指摘された
2022年1月17日、3週間続く食欲不振、吐き気、嘔吐、7kgの体重減少に続き、Cr値2.28mg/dLの腎不全で当院を受診し入院した
入院時:血圧139/87mmHg、心拍数127回/分、呼吸数20回/分、体温36.7℃、室温での末梢酸素飽和度97%、体重56.3kg(50~75パーセンタイル)、身長148.9cm(10~25パーセンタイル)、BMI25.4kg/m2(90~95パーセンタイル)、心窩部圧痛は陽性で、costovertebral angleの圧痛を認めず。急性期病態と脱水を呈していた
静脈血ガス分析で代謝性アシドーシス(pH 7.261,HCO3- 16.3 mmol/L), アニオンギャップ17.7あり。血清中C3,C4は正常範囲内、であった.ANA,c-ANCA,p-ANCAはすべて陰性で,IgG,IgA,IgMはそれぞれ2,834,557,250 mg/dLであった.PT 1.29INR、aPTT 31sであった。Dダイマーは0.91 mg/L FEU,LDH 157 IU/Lとそれぞれ高値であった.クレアチンキナーゼMBアイソザイム,トロポニンIなどの心酵素は,プロ脳性ナトリウム利尿ペプチド237.6 pg/ml(正常範囲0~125 pg/ml)を除き正常範囲内であった.
尿の顕微鏡所見では,白血球が10-19/高出力視野(HPF),鋳型が21/低出力視野(LPF)以上の膿尿が認められた.スポット尿PCRは1.95 g/g-Cr,スポット尿カルシウム:Cr比は0.19であった.24時間採尿時の蛋白尿 861mg/day。尿中NAG:Cr 32.61 IU/g-Cr,β2MG値は2.85 mg/Lであった.
胸部&腹部レントゲン検査では特に所見はなかった。2日目の腎臓超音波検査では,腎臓の大きさは正常で,わずかにエコーが増加し,腎動脈抵抗値は正常範囲であった.心電図検査では非特異的なST異常を伴う洞性不整脈を認めた.胃・十二指腸内視鏡検査では胃・十二指腸の粘膜に異常はなかった.
入院5日目の腎生検で、免疫蛍光法によるIgG, IgM, IgA, C3, C1q, C4, fibrinogen, kappa, lambda軽鎖は陰性であった.糸球体の大きさと細胞数は正常であった.尿細管は高度な壊死,尿細管破裂,脱落を示し,間質には好中球,好酸球,単核球の浸潤がみられた.血管は異常なし。糸球体基底膜の厚さは正常であり,比較的滑らかな輪郭を呈していた.電子密度の高い沈着物は観察されなかった。上皮細胞のfoot processはわずかな局所的な浸潤を示した(図2)
入院10日目にステロイド内服治療を行ったところ、腎不全は著明に改善した
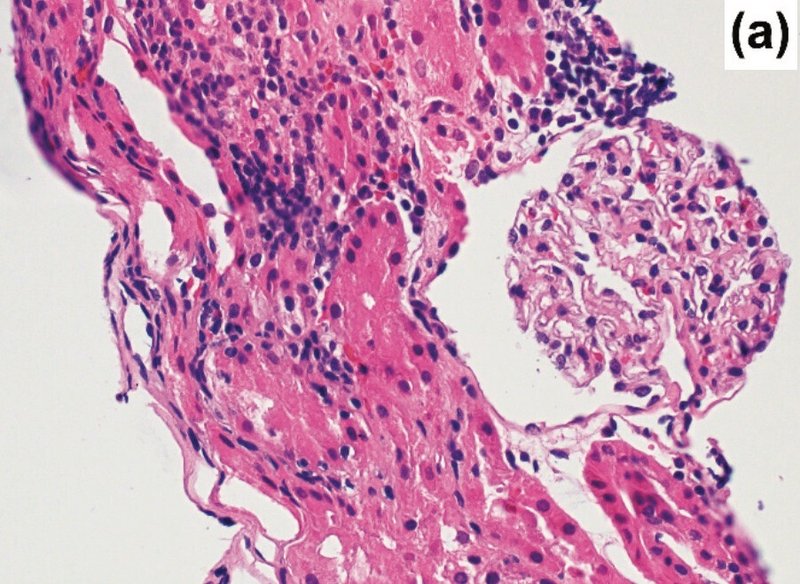
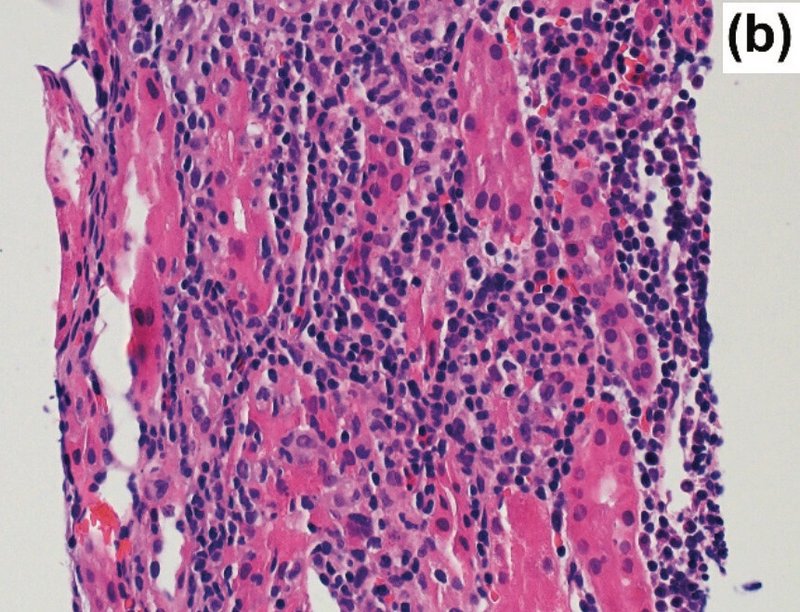
診断は、急性腎障害をきたした急性尿細管間質性腎炎(ATIN)。最初の小児症例である
一つ前の症例と同じ論文です↓
ワクチン接種後の急性腎障害AKI_____________半月体型壊死性糸球体腎炎
症例. 78才女性 腎臓限定性ANCA関連血管炎(AAV)
基礎疾患:2型糖尿病、高血圧、発作性心房細動の病歴があるが、ワクチン接種前のルーチン検査は正常。Scr 0.77 mg/dL,尿検査で血尿と蛋白尿が認められなかった
COVID-19の既往歴なし
BNT162b2初回接種後に、吐き気、嘔吐、下痢を発症したが、自然に改善。
初回接種16日後, 血清クレアチニン値(Scr)1.31 mg/dL,尿検査で血液(3+)、高倍率視野あたり99個の赤血球(RBC)、7個の白血球(WBC)、蛋白 100 mg/dL タンパク。
初回接種22日後, 2回目のBNT162b2を接種した
2回目接種後,再び悪心,嘔吐,下痢の症状が出現し,新たに嗜眠が出現した.
初回接種から28日後に来院,血清クレアチニン値 3.54mg/dL,尿検査は血液(3+),赤血球数56/高視野,WBC数13/高視野,蛋白100mg/dL (蛋白尿& 顕微鏡的血尿)。
腹部・骨盤のCTで急性期の異常なし
尿顕微鏡検査で、高倍率視野あたり1-2個の粒状キャスト、少数の腎尿細管上皮細胞、赤血球(10%以上異形)多数、少数の白血球が認められた
尿中アルブミン-クレアチニン比は2.05 g/g
抗MPO抗体価の上昇(力価:1.1AI、正常値:0.2AI以下)。補体レベルおよび他の血清学的検査に異常はなかった.
ステロイド治療を始める
腎生検で,光学顕微鏡で中等度の間質性炎症を伴う半月体型壊死性糸球体腎炎を認めた(Fig.1).免疫蛍光法ではpauci-immune glomerulonephritisが確認された.
腎限局型MPO-AAVと診断され、リツキシマブの投与を開始し、改善した
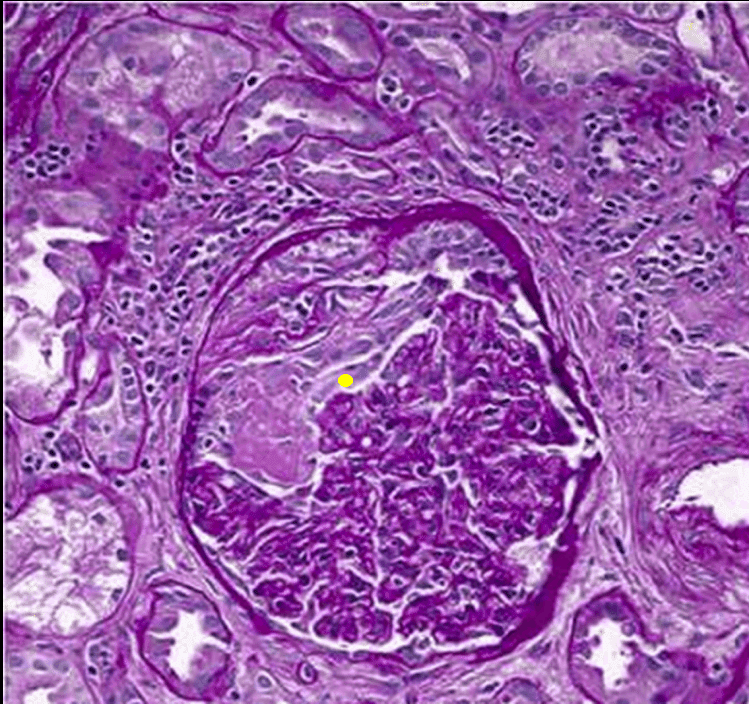
黄色い点のある部分と同様の色調の領域です
このような組織検査所見の場合には非常に急速に腎機能が失われていく恐るべき病気になります。このかたの場合には免疫抑制剤を使用して進行が止まり、腎機能の改善が見られました
使用された薬剤はステロイドとリツキシマブです
診断は、腎限局型MPO-AAVで、中等度の間質性炎症を伴う半月体型壊死性糸球体腎炎
もっと詳しく読みたい人は下記へどうぞ
ワクチン接種後の急性腎障害AKI________IgA腎炎
症例 54才女性
既往歴:溶連菌感染後のIgAN (2006年に腎生検で診断)。肥満(BMI 31.6),高血圧,GERDを合併していた.COVID-19の感染歴はなかった。エナラプリル20 mg/日,ヒドロクロロチアジド12.5 mg/日,プロプラノロール120 mg/日を服用中であった
ベースラインのクレアチニン値(Cr)は1.2(eGFR 46 mL/min/1.73m2)であった。尿検査では,2+蛋白,3+血液,赤血球(RBC)15/高倍率視野(HPF)が陽性であった.総尿蛋白/Cr比は1.03であった
2回目のモデルナワクチン接種2日後に肉眼的血尿が出現し,2日後に自然消退した.
診察時:体温36.5℃,血圧122/88mmHg,心拍数78拍/分.下肢の浮腫を認めず、身体所見に異常なし
ワクチン接種後約1週間でCrが3.04(eGFR16mL/min/1.73m2)に上昇し、尿検査では1+蛋白、3+血、赤血球50/HPFを認めた。総尿蛋白/Cr比は0.67であった。腎臓超音波検査は異常なし
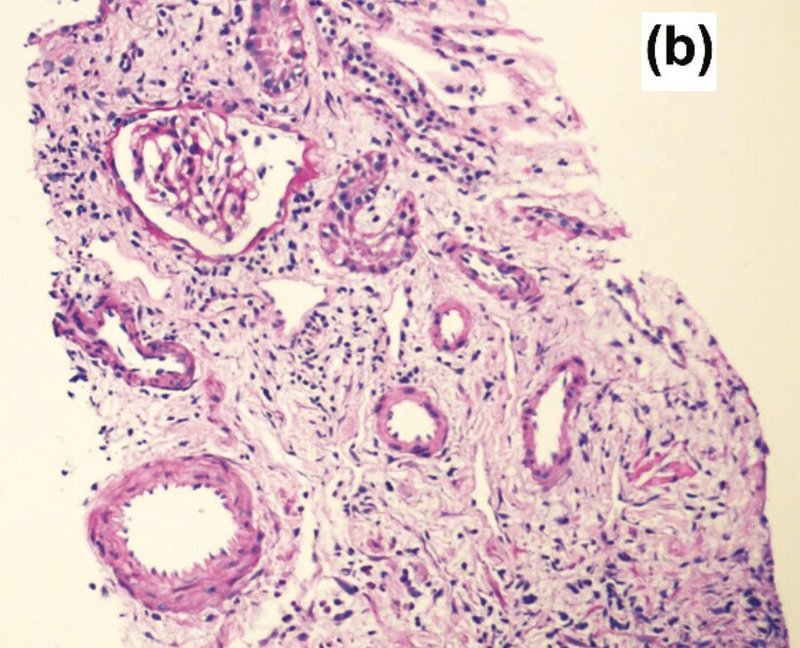
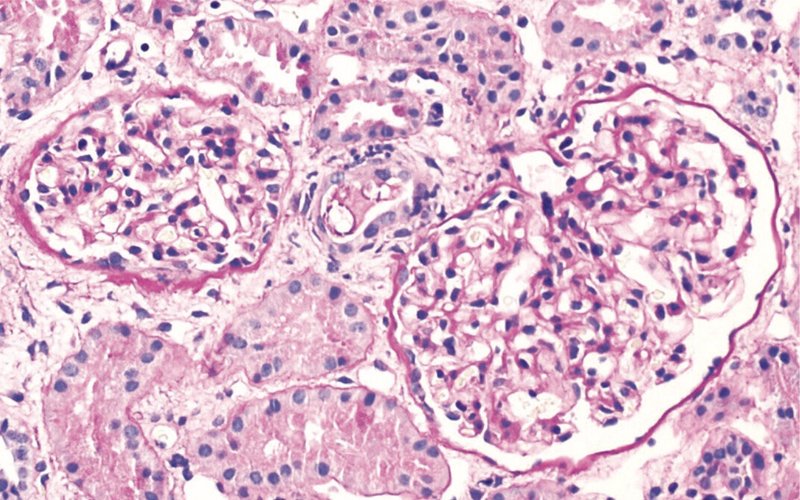
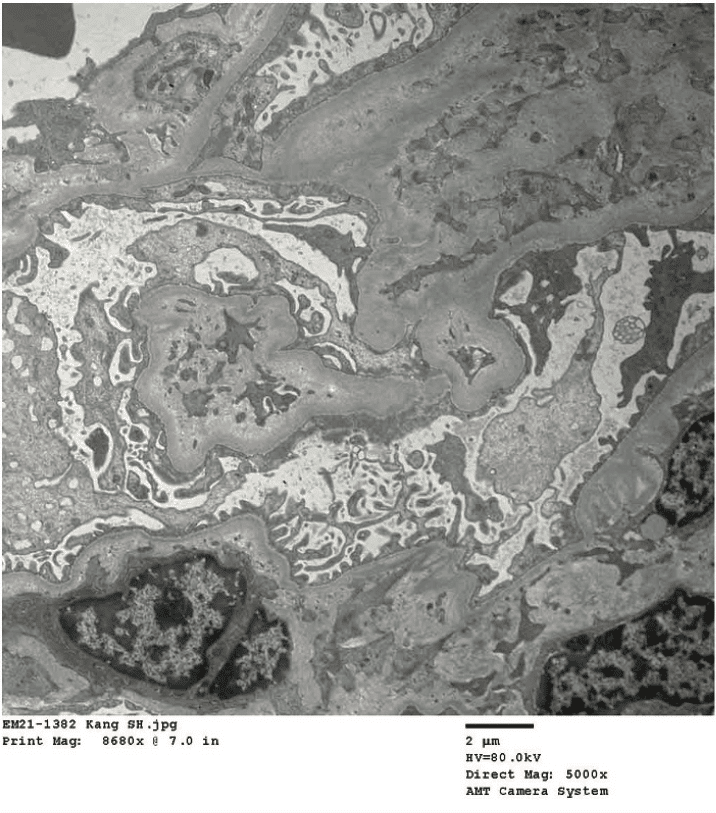
腎生検では軽度の間質性線維症と三日月形成のない尿細管萎縮を認めた(図1a)メサンギウムに弱いIgA染色を認めた(Fig.1b)。IgG染色は陰性であった(Fig.1c)。電子顕微鏡ではメサンギウムに電子密度の高い沈着物を認めた(図1d)
病歴と腎生検結果からIgAN再発と診断され、ステロイド療法にて軽快した
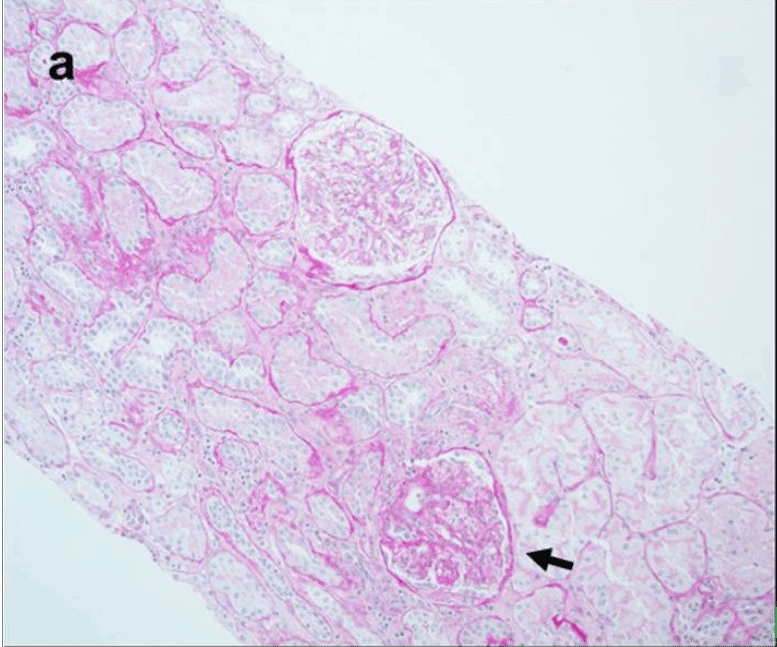
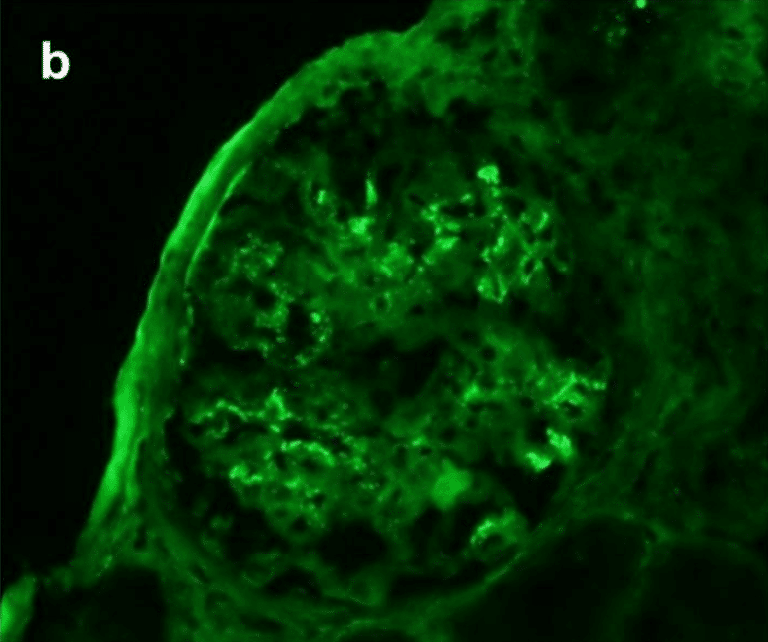
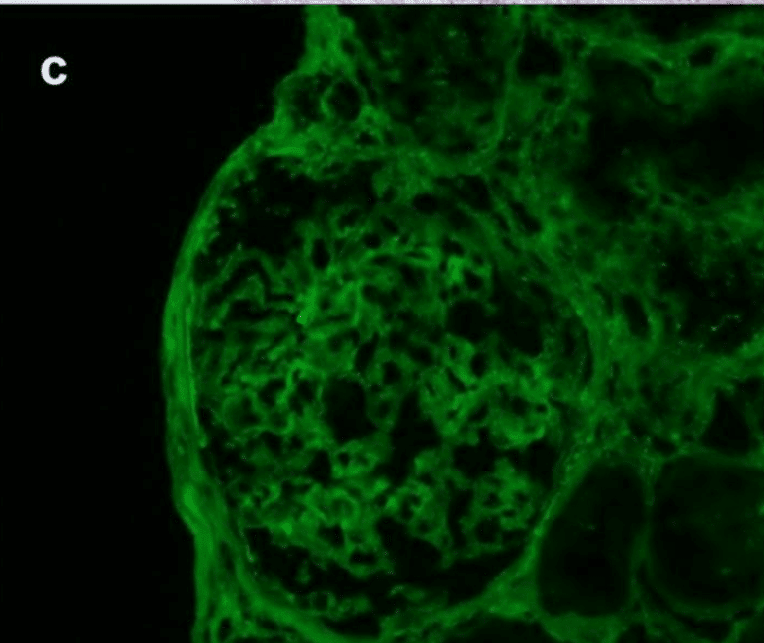
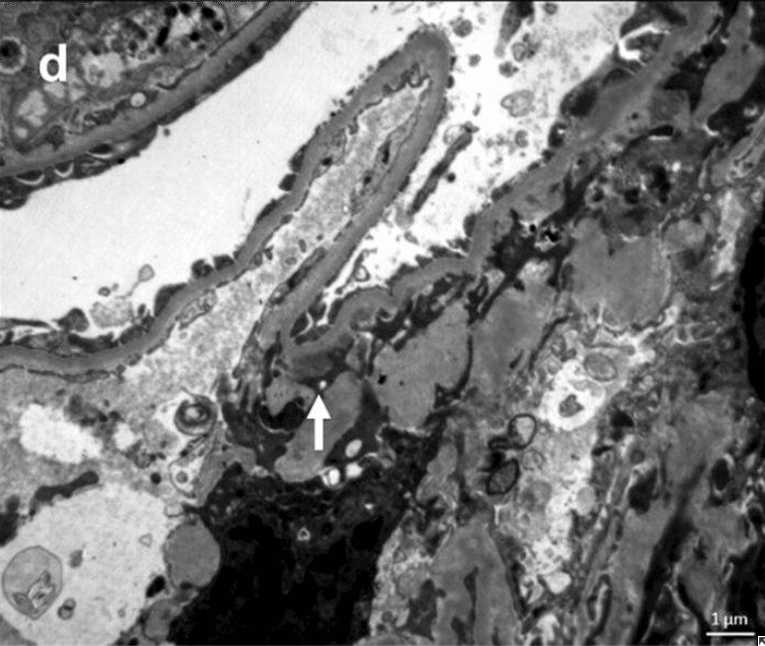
診断は、IgA腎症の再発
ワクチン接種後巣状壊死性糸球体腎炎_______MPO-ANCA関連血管炎
症例 84才男性
既往歴:脳梗塞(後遺症なし)、早期大腸癌(発症3年前に内視鏡的粘膜切除術が奏功)
2021年5月22日に1回目、6月12日に2回目のBNT162b2ワクチン接種を行った。2回目接種1日後に、頭痛、微熱、倦怠感、咳を自覚しロキソプロフェンナトリウムによる治療を行ったが解熱せず、2週間後に、持続する発熱、倦怠感、咳で当院に来院した。
これまでの尿検査で異常なし。直近の2019年12月12日の尿検査も正常。
入院時:頸部リンパ節腫脹
初回の臨床検査:クレアチニン1.22mg/dL(ベースライン1.17mg/dL、3年前)、血中BUN23.1mg/dL、CRP 18.4mg/dL 、白血球数12600/μL、ヘモグロビン12.5g/dL。尿検査は,蛋白1+(0.19 g/g/Cr),血液3+[赤血球(RBC)100個以上/高倍率視野].尿細胞診では赤血球、好中球、好酸球が認められ、悪性腫瘍の所見はなかった
腹部超音波検査では、水腎症の徴候は認められなかった
胸部CTでは2年前に発見された肺の下葉を侵す間質性肺炎の増悪が検出された.
抗MPO-ANCA 112.8 U/mL (陽性)
腎生検の結果、巣状壊死性糸球体腎炎と腎小葉間動脈に血管炎を認めた
MPO-ANCA関連血管炎と診断され、ステロイド治療が行われた
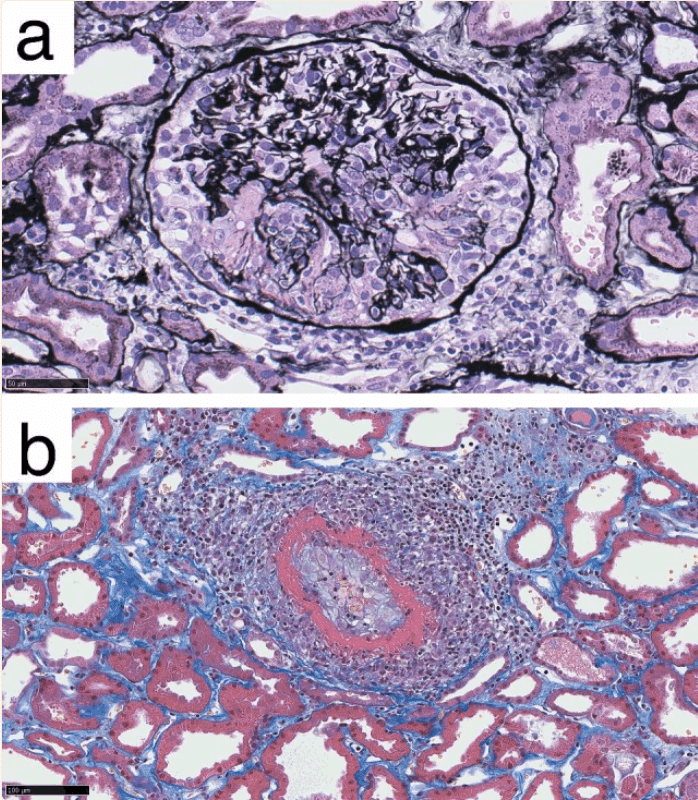
b 腎小葉間動脈に顕著な内皮の腫脹を伴うフィブリノイド壊死を示す。マッソントリクローム染色
ワクチン接種後の急性腎障害AKI_____________MPO-ANCA血管炎によるpauci-immune crescentic glomerulonephritis
症例 72才男性
既往歴:前立腺肥大症があり,タムスロシンで治療中であった.アレルギーはなかった.過去にインフルエンザワクチンを接種しており,合併症はなかった.ワクチン接種の2カ月前に行われた定期検査では腎機能は正常であった
現病歴:患者は入院の6週間前にBNT162b2ワクチンの初回接種を受けており,初回接種後に症状を示さなかった。初回接種から3週間後に2回目の接種を受けた.半日後に38℃の発熱があり,間欠的な発熱,進行性の疲労感,食欲不振を呈した.この症状が2週間続いたため,近医を受診した.
近医にて血清クレアチニン値5.0mg/dL,CRP高値,軽度の貧血,尿検査では顕微鏡的血尿と蛋白尿が認められた.胸部X線撮影では肺炎は認められず,SARS-CoV-2 PCR反応も陰性であった.水分補給と抗生物質による治療を行ったが,貧血は悪化し,CRPは上昇したままであり,発熱も持続し、MPO-ANCAが陽性で.急性腎不全となり当院に入院となる
血圧 116/59mmHg、脈拍 100回/分、体温は37.2℃。呼吸困難や血痰はなかった。肺にラ音は聴こえなかった。入院時の臨床検査では,腎機能,尿検査項目の改善は認められなかった.MPO-ANCAの力価は著明に高値。胸部CTでは,結節性陰影がわずかに認められ(図1)、Birmingham Vasculitis Activity Score(BVAS)は18の広範な疾患活動性を示していた
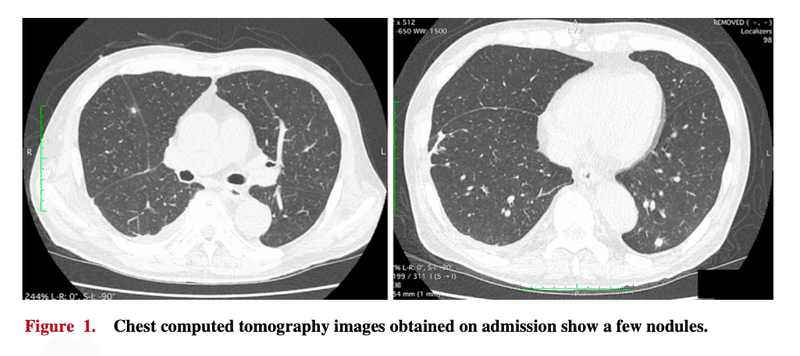
臨床的に急速進行性糸球体腎炎と診断し、副腎皮質ステロイドのパルス投与,間欠的血液透析を開始した.PSL治療後6日目の腎生検の結果、ほぼすべての糸球体に細胞性半月体、分節性壊死、ボーマン嚢の破壊、さらに小血管のフィブリノイド壊死と血管内皮細胞の増殖,間質性線維化,尿細管の萎縮が認められた(図3)
免疫蛍光染色でIgG,IgA,IgM,C3cは陰性であった.MPO-ANCA血管炎によるpauci-immune crescentic glomerulonephritisと診断した
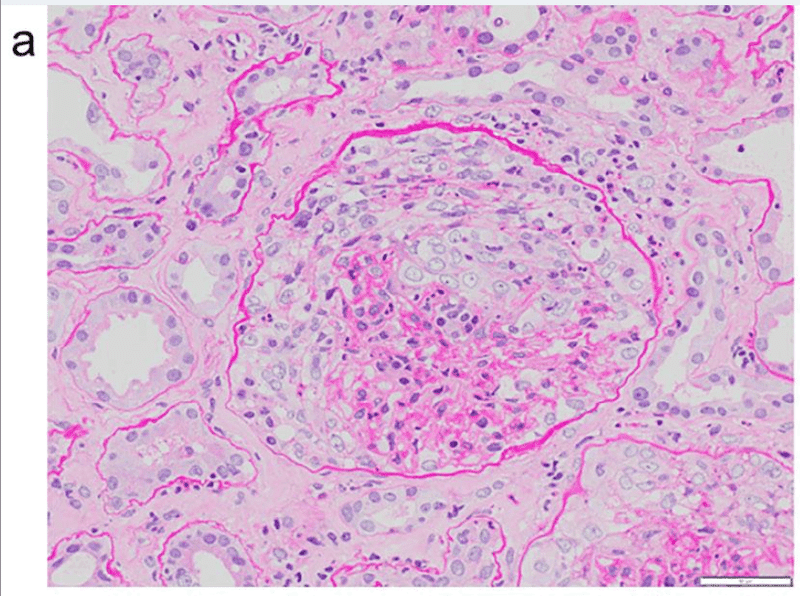
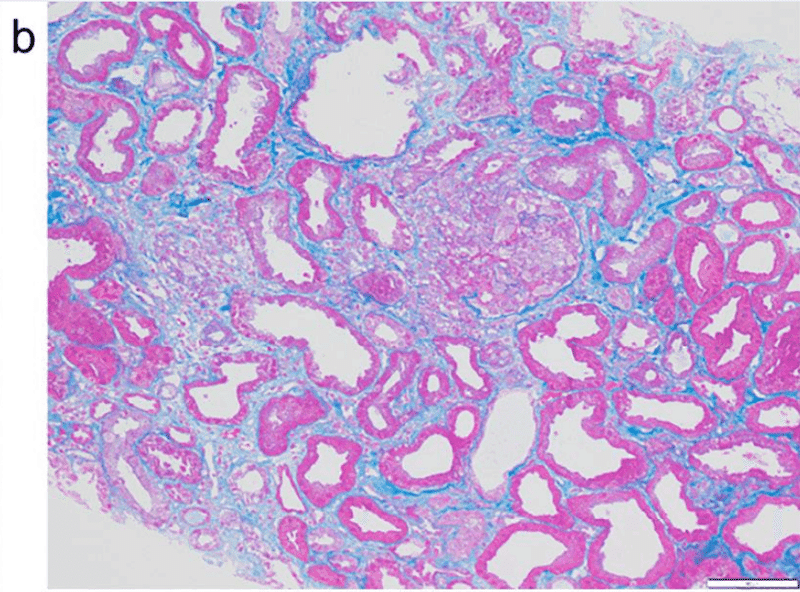
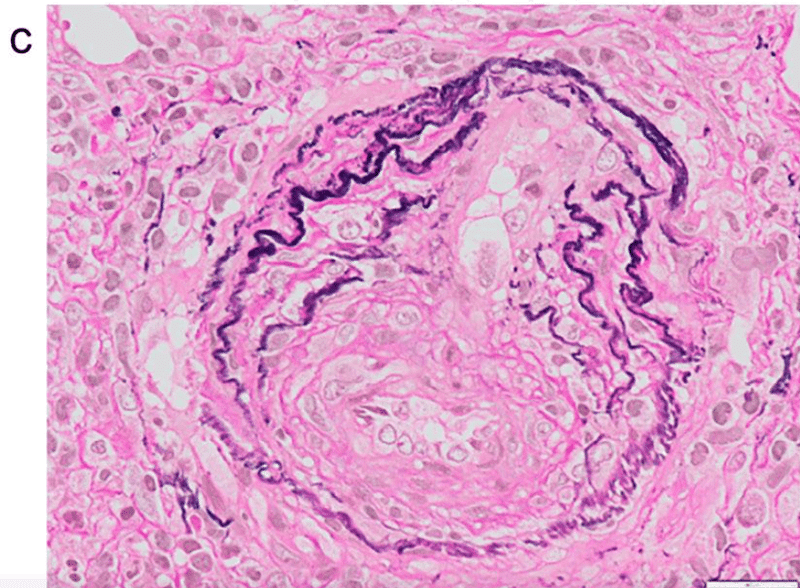
rituximab(375mg/m2)投与を開始した入院1週間後に腎機能が改善し,入院11日後に血液透析を中止した.サイトメガロウイルス関連肝炎と血小板減少のため,リツキシマブを2回投与した.全身症状は消失し,血清クレアチニン値は2.2 mg/dLと安定し,胸部CTの結節性陰影は縮小した.退院時のBVASは7であった.
ワクチン接種後IgA腎症の発症 < IgA血管炎
症例 50歳男性
基礎疾患:季節性アレルギー, 4か月前に入院を必要としない軽度のCOVID-19感染症
薬物療法なし
6週間前にBNT162b2 ワクチン初回接種。
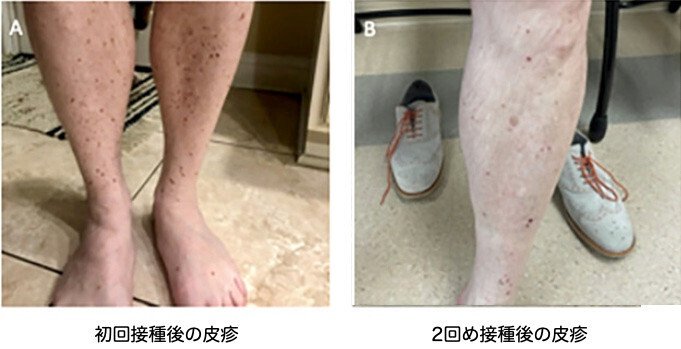
初回接種2週間後に下腿に皮疹を発症した(図1)。フルオシノニド0.05%クリームを1日2回、1~2週間患部に塗布で皮疹は消退した
初回接種から3週間後、2回目接種。その2日後、発疹が再び出現し、下腿の同じ部位だけでなく、大腿部、前腕背部、下腹部、上背部、臀部にも紫色の非白斑性丘疹と水疱が発生し、より重症化した。さらに筋痛を併発した。肉眼的血尿なし
皮膚生検でIgA-優位の白血球破砕性血管炎が検出された (論文に写真なし)
2週間の副腎皮質ホルモン剤内服終了後,尿検査で蛋白尿を認めたので、腎臓内科受診した
血圧122/81mmHg, 血清クレアチニン0.9 mg/dL [2回め接種2週間後], 尿蛋白/クレアチニン比1.1g/ (UPCR)1.1g/日[2回め接種3週間後]、血清補体 正常,血清学的検査 陰性, 尿沈渣に棘細胞+ (棘細胞写真 Fig 1CD ブログへ)
下肢に治癒性丘疹を認めたが、それ以外の身体所見は正常。尿検査で蛋白尿
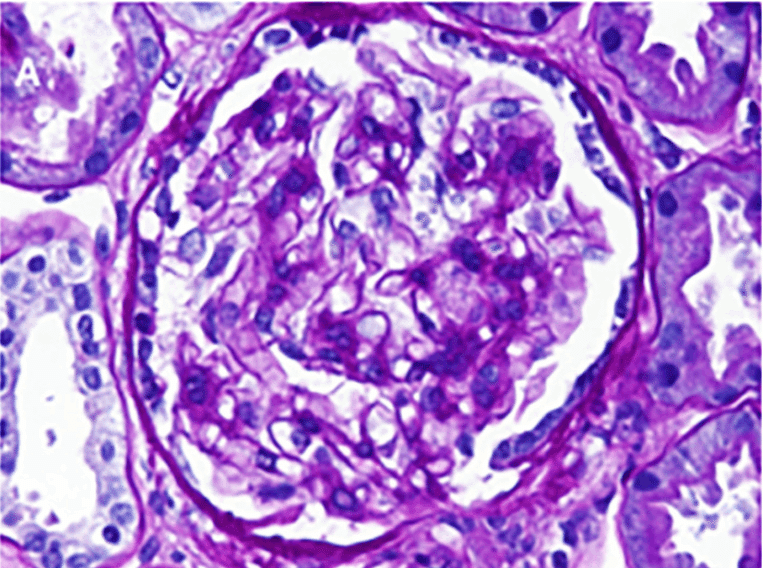
腎生検の結果、メサンギウムの増殖とIgA抗体の沈着を確認し、IgA腎炎と診断された (図2AB)
*図2Bは紫斑性皮疹
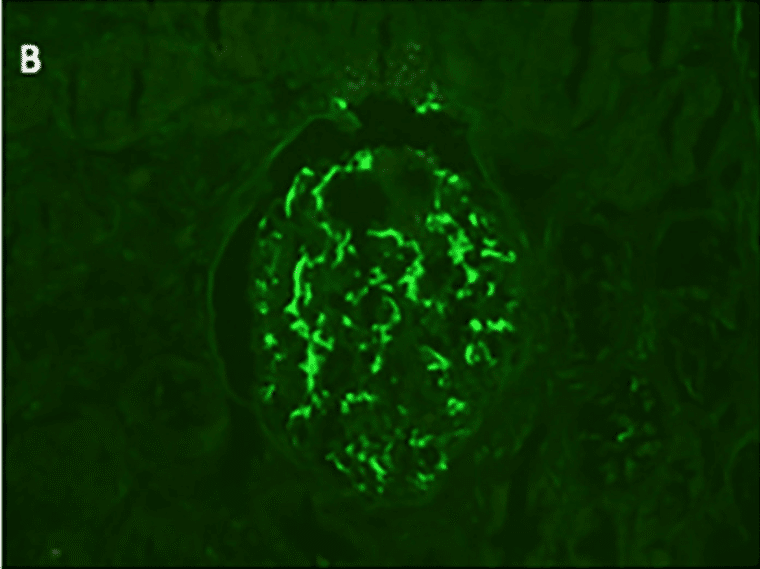
ワクチン接種後IgA腎症 < IgA血管炎
症例 76才男性
既往歴 10年前に白血球破砕性血管炎を発症し,免疫抑制療法を受け,無投薬で寛解している。当時,両下肢に触知可能な紫斑性皮疹を呈し,腹痛,関節痛,蛋白尿,腎機能低下など他の全身性血管炎徴候は認めなかった.皮膚生検では,免疫蛍光染色は行われなかったが,白血球破砕性血管炎が認められた.皮膚病変が高度で進行性であったため,プレドニゾロン(20 mg/日)を2週間内服し,アザチオプリン(25 mg/日)を6カ月間内服した
COVID-19感染や最近の呼吸器,泌尿器,消化器疾患の既往はなく,mRNAワクチンの初回接種から2回目までの症状は否定された.
BNT162b2 ワクチン2回目接種の10日後に両下肢に突然発症した紫斑性皮疹で皮膚科外来を受診した
平熱,その他のバイタルサインの異常なし
両下腿に分布する出血性丘疹小水疱病変が認められた(図1a)
血清クレアチニン値 1.06 mg/dL(eGFR 60 mL/min/1.73 m²)で、この時は尿検査は行わなかった
皮膚生検で白血球破砕性血管炎を認めた(図1b)
ステロイド経口治療で、皮膚病変は徐々に軽快し始めた
2回目接種から30日後にびまん性腹痛と下痢を訴えた。
2回目接種から45日後に末梢性浮腫の悪化のため腎臓内科を受診し、入院となった
血圧140/80mmHg以外はバイタルサインに異常はなかった.
両下肢に多発性紫斑病性皮疹を伴う3+前胸部pitting edemaを認めた
血清クレアチニン 1.06から1.42 mg/dLに増加し(eGFRは60から48 mL/min/1.73 m²に減少)、血清アルブミンは3.8から2.7 g/dlに減少した
ネフローゼ範囲の蛋白尿,尿検査では蛋白4+,赤血球(RBC)/高出力視野(HPF)10-19,白血球(WBC)/HPFが認められ,スポット尿蛋白/クレアチニン比(UPCR)は9.01 mg/mgであった.
B型肝炎表面抗原とC型肝炎ウイルスに対する抗体の検査は陰性,C3とC4は正常な基準範囲内,抗核抗体,抗抽出性核抗原抗体,抗好中球細胞質抗体,抗粒体基底膜抗体の検査は陰性であった.
COVID-19(鼻咽頭ぬぐい液)のPCR検査は陰性であった.腎超音波検査では,腎臓の大きさは正常であり,腎実質のエコーも正常であった.
2回目接種から45日後の腎生検で合計27個の糸球体が確認され,そのうち4個はグローバルな硬化を,10個は細胞性または線維性のクレセントを,2個はセグメント的な硬化を示した.単核細胞の浸潤と間質の線維化を伴う局所的な重度の尿細管萎縮が皮質領域の約10%未満に認められた.免疫蛍光顕微鏡では、メサンギウムのIgA染色が優勢で、部分的に末梢染色が認められ、IgA腎炎と一致した(図2a)。電子顕微鏡では、中程度の量のメサンギウム沈着とポドサイトが認められ、局所的な足突起の消退が見られた(Fig.2b)
ネフローゼ症候群を呈するIgA血管炎と診断し,ステロイド療法にて軽快した
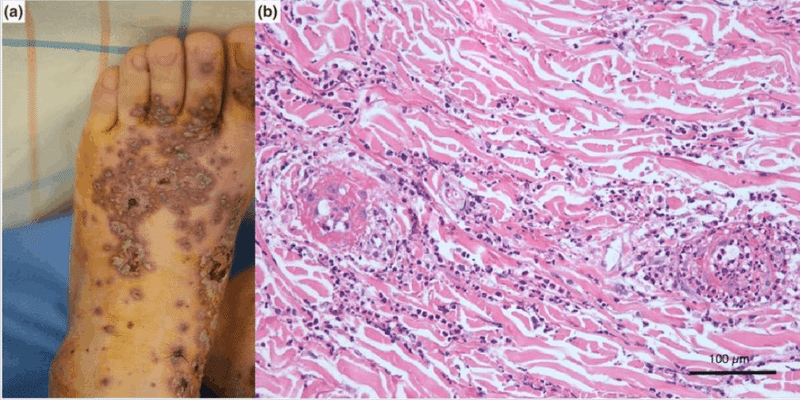
図1b. 皮膚生検で白血球破砕性血管炎を認めた
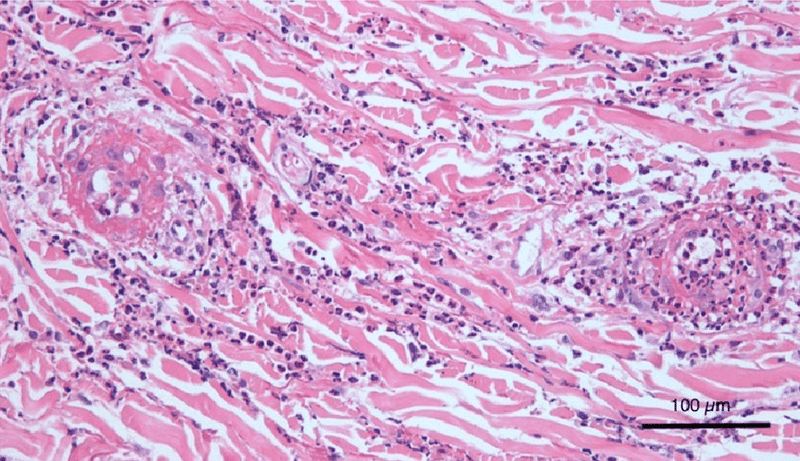
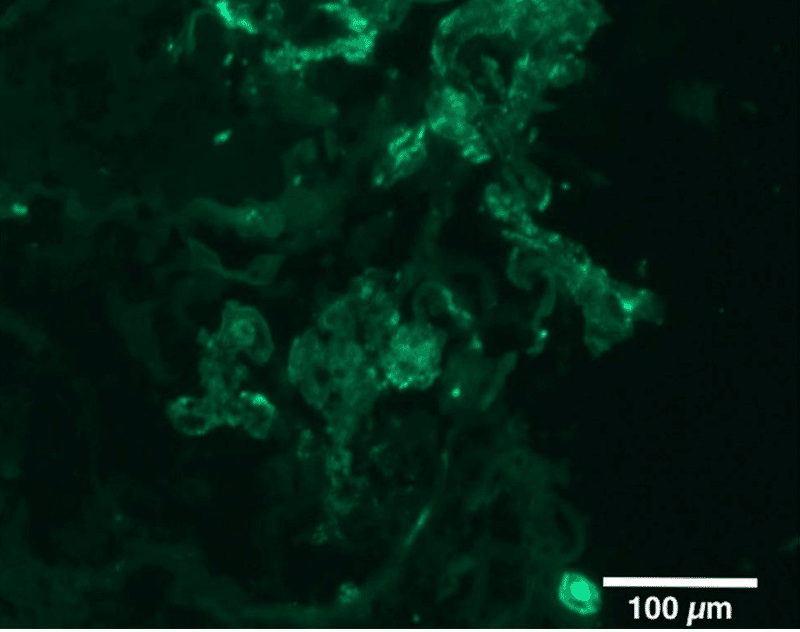
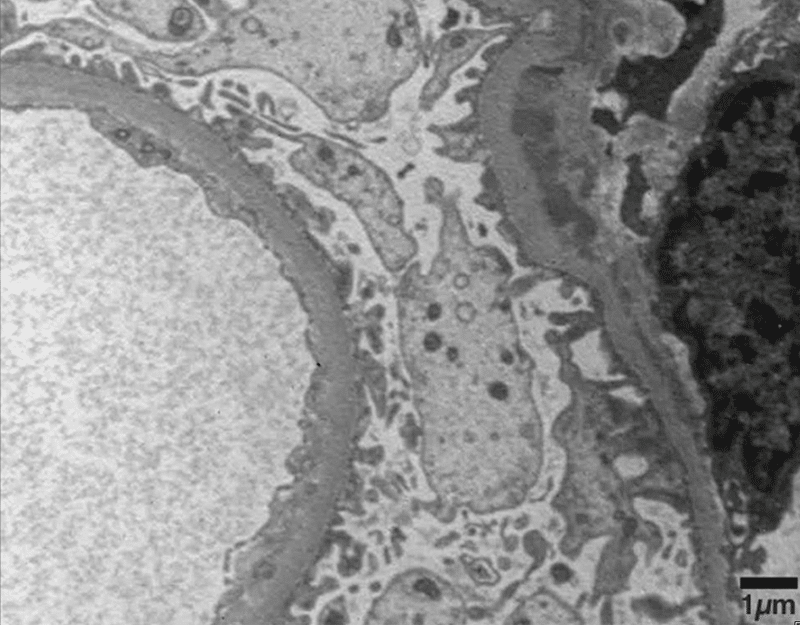
ワクチン接種後IgA腎症の再燃
症例 38才女性 2人
2人とも、以前にIgA腎炎と診断されている。モデルナの新型コロナウイルスワクチン接種前に二人とも蛋白尿は1g/日未満で、腎機能は十分に保たれていた。2回目のワクチン接種の数時間後、両者とも体の痛み、頭痛、疲労から発熱、悪寒に至る全身症状を呈した。全身症状が現れてから8時間から24時間の間に,2人の患者は肉眼的血尿を認めたが,3日後に消失した.血清クレアチニンは増加しなかったが、1名の患者で蛋白尿が増加した
ワクチン接種後IgA腎症の再燃
症例 52才女性
2017年にIgA腎症を発症。22回目のBNT162b2ワクチン接種後24時間以内に肉眼的血尿を発症した。ステロイドを含む免疫抑制剤を使用せずに、1週間以内に再度検査を行ったところ、血尿は消失し、蛋白尿も改善した。2年前のShingrixワクチン (帯状疱疹ワクチン) 初回接種後にも肉眼的血尿があった
ワクチン接種後IgA腎炎の一過性肉眼的血尿 (一時的に症状が悪くなった)
症例 22才男性 腎機能正常のIgA 腎症 患者。 2回目のモデルナ mRNA-1273 ワクチン接種2日後に肉眼的血尿が再発し、散発的に蛋白尿の増加、関節痛、腹痛、蕁麻疹を伴っていた。症状は自然消退した.ワクチンによる抗スパイク蛋白抗体は上昇しなかった
症例 41才女性 腎移植後のIgA 腎症 患者。 初回の BNT162b2 ワクチン接種2日後に肉眼的血尿が再発し、血清クレアチニンが一過性に上昇した。症状は自然消退した.ワクチンによる抗スパイク蛋白抗体は上昇しなかった
症例 27才女性 血液透析中のIgA 腎症 患者。2回めの BNT162b2 ワクチン接種2日後に肉眼的血尿が再発した。症状は自然消退した.ワクチンによる抗スパイク蛋白抗体は上昇した
ワクチン接種後IgA腎症の再燃
症例 46才女性
既往 4年前に血尿と蛋白尿を精査し、腎生検を行いIgA腎症(IgAN)と診断された。2年前の扁桃摘出術とステロイドパルス療法による治療で、IgANは再発なく完全に消失した。
高熱,筋肉痛,肉眼的血尿を主訴に腎臓内科クリニックを受診した.。COVID-19の初回接種後,症状はなかった.BNT162b2 ワクチン2回目接種12時間後に高熱、筋肉痛、肉眼的血尿を認めた。臨床検査では,著明な蛋白尿(尿検知棒:3+)と血尿(100個以上/高出力野)が認められ,血清クレアチニンは正常であった.発熱と蛋白尿は2週間以内に自然消退したが,顕微鏡的血尿は持続した.
ワクチン接種後IgA腎症 (小児)
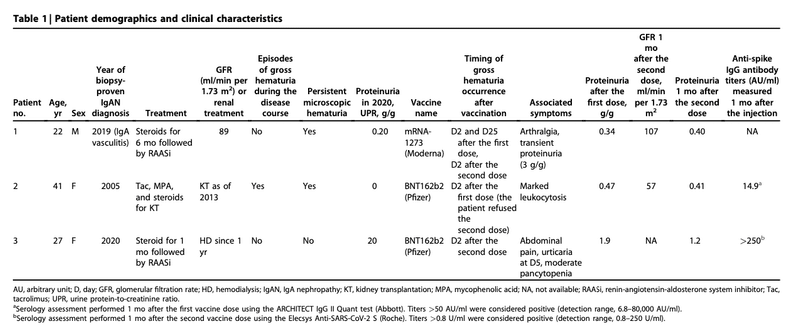
症例1. 15才男性
基礎疾患:微小血尿の既往が6ヵ月ある。COVID-19感染の既往はなく,他の感染後の肉眼的血尿もなかった.腎臓疾患の家族歴はなかった
BNT162b2 ワクチンの2回目接種の1日後に肉眼的血尿, 発熱と筋肉痛を認めた
入院時:体温37.7℃,脈拍72回/分,血圧115/64mmHg,肋椎角圧痛はなかった.血清クレアチニン0.97 mg/dL、推定糸球体濾過量(eGFR)92 mL/min/1.73 m2、尿検査で多数の赤血球と中程度の蛋白尿を認めた。CTにて腎臓の形態的な異常は認められなかった
腎生検は,肉眼的血尿の発現から7日後に実施した.
IgA腎炎と診断され、Oxford MEST-C分類はM1E0S0T0C1であった。肉眼的血尿は6日以内に無治療で自然消退したが,顕微鏡的血尿と蛋白尿はその後持続した.
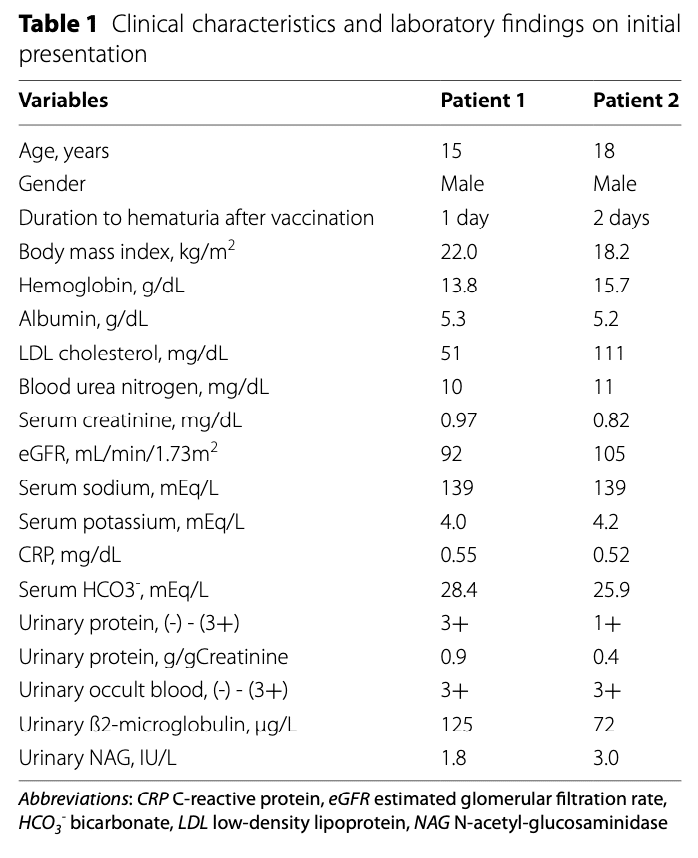
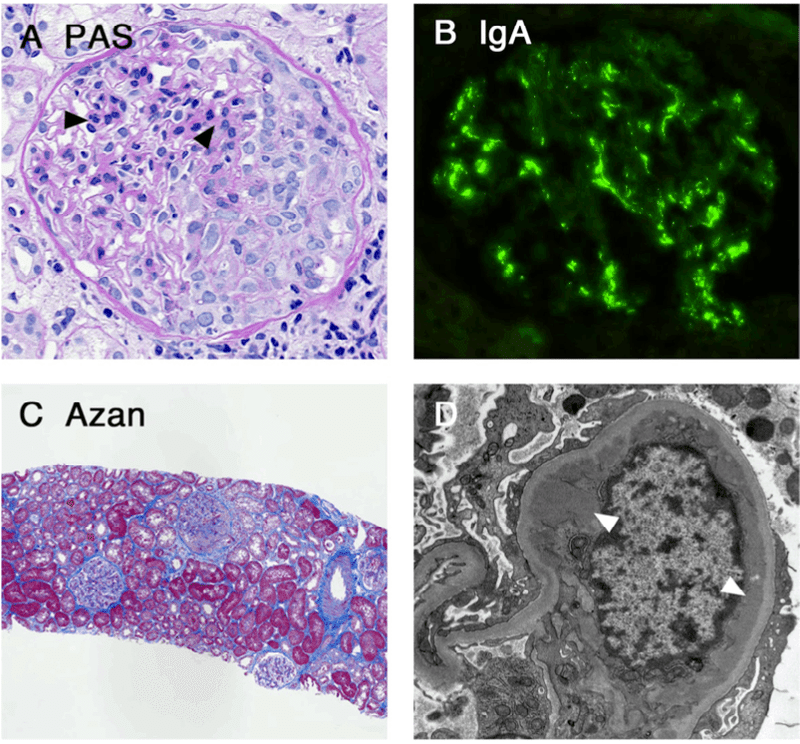
症例2. 18才男性 (症例1の兄)
基礎疾患:顕微鏡的血尿の既往が3年ある,COVID-19感染症の既往はなく,他の感染症後の肉眼的血尿もなかった.腎臓疾患の家族歴はなかった.
BNT162b2 ワクチンの2回目接種後2日目に肉眼的血尿を呈し,発熱と全身倦怠感もあった
入院時:体温38.6℃,脈拍83回/分,血圧131/76mmHgで,肋椎角の圧痛はなかった.血清クレアチニン0.82 mg/dL、eGFR 99 mL/min/1.73 m2、尿検査では多数の赤血球と軽度の蛋白尿が認められた. CTで腎臓の形態的な異常は認められなかった
肉眼的血尿の発現から3ヵ月後に腎生検を施行した
IgA腎炎と診断され,Oxford MEST-CスコアはM1E0S0T0C0であった.肉眼的血尿は無治療で7日以内に自然消退し、顕微鏡的血尿と蛋白尿も徐々に消失した
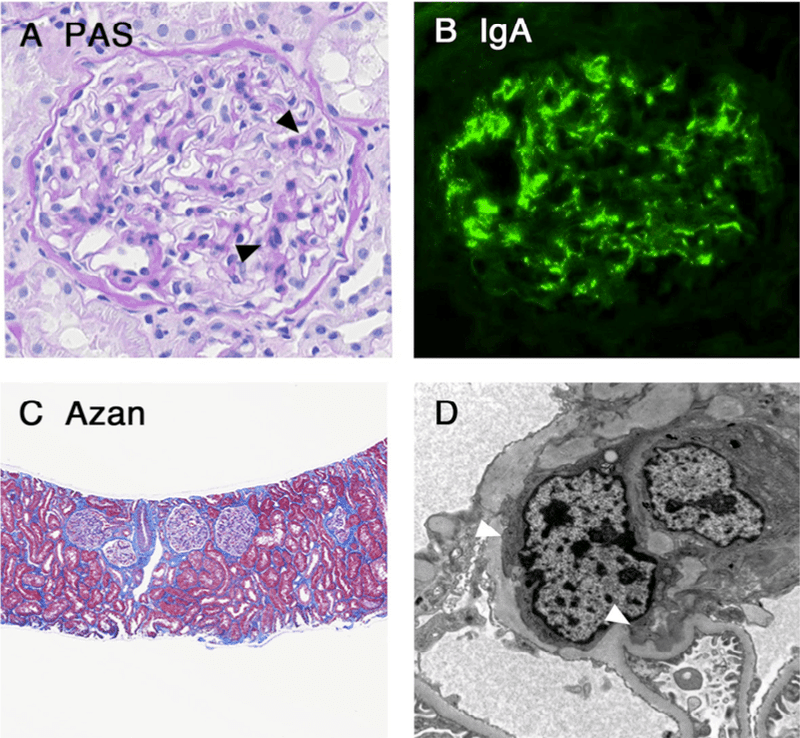
http://fujita2011.livedoor.blog/archives/51851372.html
ワクチン接種後ネフローゼ症候群 (小児)
症例. 15才男性
基礎疾患なし。学校検尿に異常なし。アレルギー歴なし
BNT162b2初回接種翌日,37.3℃の発熱と注射部位の軽度の腫脹あり。
接種4日後、眼瞼浮腫
接種8日後、下肢末梢浮腫
接種16日後、尿検査で尿蛋白4 +
接種後19日後、体重は45kgから49.7kgに増加し,血圧は106/62mmHg,脈拍は69拍/分。眼瞼と下肢の浮腫,腹部の膨満がみられた.
血清アルブミン1.6 g/dL,クレアチニン0.64 mg/dL,推定糸球体濾過量(eGFR)116.62 ml/min/1.73 m2,BUN 7 mg/dL,血清ナトリウム141 mEq/L,カリウム 3.9 mEq/L,塩素106 mEq/L,総コレステロール335 mg/dL, 補体C3およびC4は正常範囲内。
尿検査で,尿蛋白4+,尿沈渣赤血球<1/high-power field,初期尿蛋白-クレアチニン比7.71 g/g cre
血清および血漿中のSARS-CoV-2スパイク蛋白の受容体結合ドメインに特異的な抗SARS-CoV-2 S血清測定結果は111 U/mL (positive ≥ 0.8 U/mL, Elecsys®) .
胸部X線検査で両側に胸水貯留。超音波検査では腎臓の大きさは正常であったが,腸管壁の浮腫と腹水あり。ネフローゼ症候群と診断し、ワクチン接種後21日目から日本の小児ネフローゼ症候群ガイドラインに基づき、プレドニゾロン(PSL)1日60mgの投与を開始した。投与12日目に完全寛解を達成し,高血圧,AKI,血栓形成などの合併症は発症しなかった..
ワクチン接種後AKI_______微小変化病および急性間質性腎炎(小児)
症例1. 14才男性
基礎疾患:なし。COVID-19感染の既往はなく,鼻咽頭スワブによるSARS-CoV-2 RT-PCR反応は陰性であった. 患者は薬の服用を否定した.
現病歴:BNT162b2 ワクチンの初回接種の5日後に両下肢浮腫を発症した.
高血圧,ネフローゼ症候群(蛋白尿4±9g/g,アルブミン2g/dL,コレステロール257mg/dL),急性腎不全(クレアチニン2mg/dL)を指摘されたが尿沈渣検査は陰性であった.浮腫は徐々に悪化した.
ワクチン接種後10日目に無尿となり,血清クレアチニンのピーク値は9 mg/dLとなった.メチルプレドニゾロンを1日3回パルス投与し,その後プレドニゾロン1日60 mgを経口投与した.3週間血液透析を受けた(Fig.1a)。C3/C4、ANA、ANCA、B型肝炎表面抗原、C型肝炎ウイルス抗体など二次性糸球体疾患の評価は陰性であった。腎臓病理検査では,光学顕微鏡で18個の異常のない糸球体を認め,免疫蛍光染色は陰性であった.電子顕微鏡では,MCDと一致するびまん性の足底突起の浸潤を認めた.びまん性の尿細管損傷と間質性炎症細胞の浸潤が認められた(図1b-d)
5週間の副腎皮質ステロイド治療後,患者は部分寛解した(クレアチニン0.53 mg/dL,蛋白尿0.9 g/gクレアチニン).
Elecsys®(Roche Diagnostics, Basel, Switzerland)を用いたSARS-CoV-2スパイク蛋白の受容体結合ドメインに特異的な免疫グロブリン総量は5.6 U/mL(陽性≧0.8 U/mL)でワクチンに対する抗体反応であることが確認された.
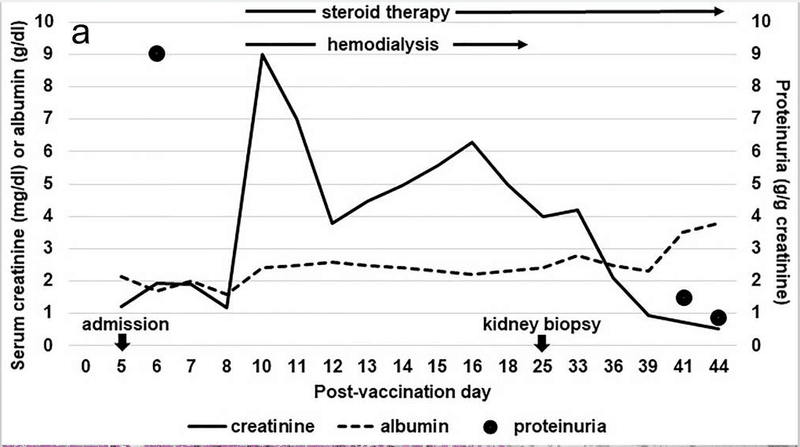
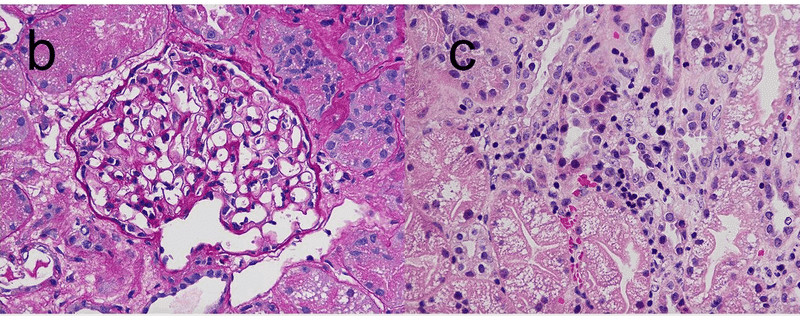
図1c びまん性の急性尿細管損傷と間質性炎症細胞浸潤(原倍400倍)
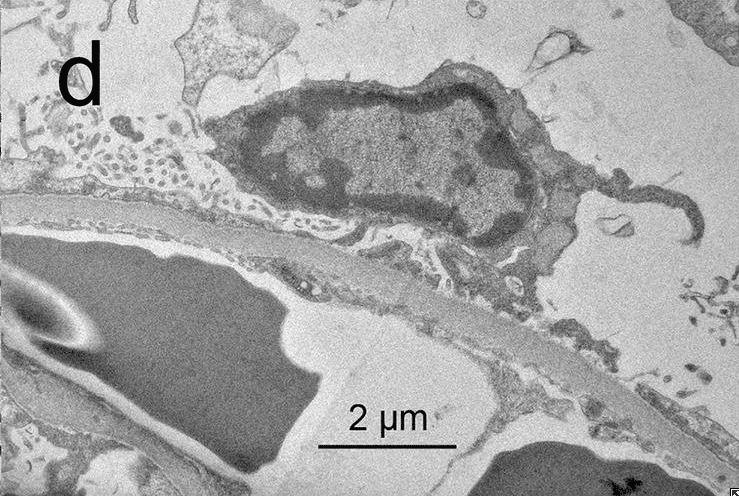
もう一つ、COVID-19ワクチンと糸球体腎炎の関係を調べたレポートも記事にしました
IgAN患者では循環血中ガラクトース欠損IgA1が増加していることが知られており、おそらくmRNA COVID-19ワクチン接種による免疫系のバイスタンダー活性化が、免疫複合体の形成とそれに続く糸球体傷害のトリガーとして作用している可能性が考えられる
ワクチン接種後のMCDの発症には時間がかかることから、細胞性免疫の役割が示唆されています。29 COVID-19mRNAワクチンは、 免疫化後7日目にピークとなるTfh反応の増強を誘発する。Tfh細胞によるMCDの発症への寄与の可能性は、MCD患者においてTfh細胞の循環サブセットが増加し、これらの集団の頻度がステロイド治療が成功した患者で減少するという観察により示唆されています40。これらの知見と、Tfh反応と相関する時点での発症が報告されていることから、おそらくmRNAワクチンによるTfh細胞集団および/または関連するサイトカインプロファイルの変化が、ポドサイトの損傷とネフローゼ症候群およびMCDの発症を促進する可能性があるのでしょう
自己抗体を介した糸球体疾患の後発症例は、ワクチン関連自己免疫の誘導によるものと思われる。ワクチン関連自己免疫は、抗原特異的および非特異的なメカニズムによって起こると仮定されている。ワクチンによる自己免疫の抗原特異的な引き金は、分子模倣による二次的なものであると考えられている。すなわち、SARS-CoV-2スパイクタンパク質のような非自己抗原にさらされた場合、配列の相同性が十分であれば、宿主組織に対する反応が誘発される可能性があるということである。SARS-CoV-2スパイクタンパク質は、いくつかのヒトタンパク質と相同性を有しており、ワクチン接種後に標的外免疫攻撃を受ける可能性がある[41]。模倣仮説と一致して、ヒト肺胞サーファクタント関連タンパク質とSARS-CoV-2スパイク糖タンパク質の相同配列が、宿主免疫攻撃とCOVID-19感染で見られるその後の肺病理に寄与することが提案されている[42]。同様に、宿主タンパク質によるウイルス抗原の擬態は、中枢神経系における免疫攻撃に寄与し、COVID-19における神経学的合併症を悪化させることが提案されている[43]
ワクチン接種による自己免疫の抗原非特異的機序は、バイスタンダー活性化によって起こると考えられている。このモデルでは、ワクチンで刺激された免疫応答が細胞損傷を引き起こし、通常は隠されている自己抗原が露出し、それが宿主免疫によって認識されるのであろう。あるいは、このモデルでは、自然免疫応答がサイトカインシグナルをアップレギュレートし、抗原提示細胞による自己抗原提示が自己反応性T細胞の可能性を高めるかもしれない。これらのメカニズムのいずれかが、ワクチン接種に反応した糸球体疾患の発症に寄与していると考えられるが、おそらくそれぞれ異なる疾患表現型が生じる.
欧州腎臓学会-欧州透析・移植学会の免疫腎臓学ワーキンググループは、最近、自己免疫性腎臓病患者におけるCOVID-19ワクチンの使用に関する勧告を発表し、既知の禁忌のないすべての個人への接種を支持している[50]。しかし、これらの勧告は、1つのワクチンプラットフォームによるワクチン接種が他のワクチンよりも望ましいかどうかについては助言していません
ここから先は
¥ 100
この記事が気に入ったらサポートをしてみませんか?
