多剤耐性菌による尿路感染症患者に対する糞便微生物移植の早期経済評価について
多剤耐性菌による尿路感染症患者に対する糞便微生物移植の早期経済評価について
https://pubmed.ncbi.nlm.nih.gov/37062804/

オリビア・ダイブロ・ベクら、Infect Dis Ther. 2023.
詳細を表示
アブストラクト PubMed PMID
引用する
アブストラクト
はじめに 多剤耐性菌(MDRO)の腸管キャリッジを根絶するための糞便微生物叢移植(FMT)の使用は、症例報告や小規模なケースシリーズで説明されている。数は少ないが、これらの患者は、患者の併存疾患と健康状態の両方を悪化させる可能性のある再発性感染症に苦しんでいる。本研究では、MDRO関連尿路感染症(UTI)に対するFMTが、入院と関連コストを削減するという仮説を立てた。
方法 2015年から2020年にかけてFMTのために紹介された患者のコホートにおいて、UTIを伴うMRDOキャリッジの除菌のために連続的に紹介されたすべての患者を選択しました。病院関連コストを算出するため、早期経済評価を行った。全体の研究コホートはClinicalTrialsに登録され、研究識別子はNCT03712722であった。
結果は以下の通り: MDROによる尿路結石患者5名を連続的に組み入れました。そのうち4名は腎移植患者であった。患者の追跡期間は中央値126日(範囲60-320)であり、各患者の追跡期間は最初のUTIからFMTまでの日数と一致させた。病院費用については、入院日数が87%、月間病院費用が79%減少した。
結論 FMTはUTIの発生を減少させるのに有効であり、病院コストの顕著な減少を媒介した。この戦略は費用対効果に優れていることが示唆された。
試験登録 ClinicalTrials, study identifier NCT03712722.
キーワード 早期経済評価、糞便微生物移植、病院コスト、MDRO、多剤耐性。
© 2023. The Author(s).
参考文献
Serra-Burriel M, Keys M, Campillo-Artero C, et al. 多剤耐性菌が成人の医療関連感染の経済的・臨床的アウトカムに与える影響:系統的レビューとメタアナリシス。PLoS ONE. 2020;15(1): e0227139. - DOI - PubMed - PMC
ダドゴスターP. 抗菌薬耐性:その意味とコスト。Infect Drug Resist. 2019;12:3903-10. - DOI - PubMed - PMC
Al Midani A、Elands S、Collier S、Harber M、Shendi AM. 腎移植レシピエントにおける尿路感染症の影響:4年間の単一施設の経験。Transpl Proc. 2018;50(10):3351-5. - DOI
(WHO) WHO. 世界各国の状況分析:抗菌薬耐性への対応。ジュネーブ: WHO; 2015.
Baunwall SMD, Lee MM, Eriksen MK, et al. 再発性Clostridioides difficile感染症に対するFaecal microbiota transplantation: an updated systematic review and meta-analysis. EClinicalMedicine. 2020;29-30: 100642. - DOI - PubMed - PMC
16件の参考文献をすべて表示
関連データ
ClinicalTrials.gov/NCT03712722
助成金支援
8056-00006B/Innovationsfonden
NNF22OC0074080/Novo Nordisk Fonden(ノボ ノルディスク ファンデン
ama apa mla nlm
メインコンテンツへスキップ
検索
カートに入れる
ログイン
ホーム
感染症・治療
記事
PDFをダウンロード
ブリーフレポート
オープンアクセス
発行:2023年4月16日
多剤耐性菌による尿路感染症患者に対する糞便微生物移植の早期経済評価について
オリビア・ダイブロ・バエック
カミラ・K・ヒェルミツレフ
...
クリスチャン・ロドベリ・ハバス
作家を表示する
感染症・治療(2023)この記事を引用する
10 Altmetric(アルトメトリック
メートル法詳細
アブストラクト
はじめに
多剤耐性菌(MDRO)の腸管キャリッジを根絶するための糞便微生物叢移植(FMT)の使用は、症例報告や小規模なケースシリーズで説明されています。数は少ないが、これらの患者は、患者の併存疾患と健康状態の両方を悪化させる可能性のある再発性感染症に苦しんでいる。本研究では、MDRO関連尿路感染症(UTI)に対するFMTが入院と関連コストを削減するという仮説を立てました。
方法
2015年から2020年にかけてFMTに紹介された患者のコホートにおいて、UTIを伴うMRDOキャリッジの除菌のために連続的に紹介されたすべての患者を選択した。病院関連コストを算出するため、早期の経済評価を実施した。全体の研究コホートはClinicalTrialsに登録され、研究識別子はNCT03712722であった。
結果
MDROによる尿路結石を発症した患者5名を連続的に対象とした。患者のうち4人は腎移植患者であった。患者の追跡期間は中央値126日(範囲60-320)であり、各患者の追跡期間は最初のUTIからFMTまでの日数と一致させた。病院費用については、入院日数が87%、月間病院費用が79%減少した。
結論
FMTは尿路結石の発生を減少させるのに有効であり、病院コストの顕著な減少を媒介した。この戦略は費用対効果に優れていることが示唆された。
試験登録
ClinicalTrials、研究識別子NCT03712722。
グラフィカルアブストラクト
原稿を作成中ですか?
よくある失敗を回避する
主なまとめポイント
糞便微生物叢移植(FMT)は、臨床感染症につながる多剤耐性菌(MDRO)の腸内キャリッジを根絶する可能性がある。
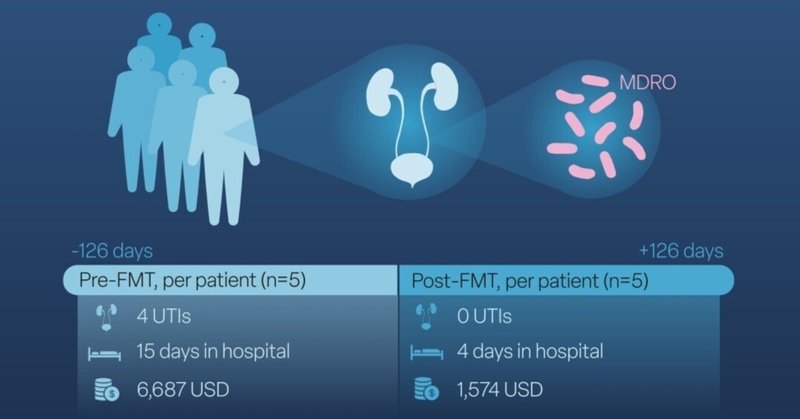
尿路感染症(UTI)の原因となるMDROに対してFMTを受けた連続入院患者5人の病院費用を調査したところ、入院日数は87%減少し、月間病院費用は79%減少したと算出された。
MDROキャリッジを根絶するためのFMTは、感染症発生件数と病院コストの両方を削減する費用対効果の高い戦略である可能性があります。
デジタル機能
この記事は、記事の理解を容易にするために、図解抄録を含むデジタルフィーチャーを掲載しています。この記事のデジタルフィーチャーを見るには、https://doi.org/10.6084/m9.figshare.22341232 にアクセスしてください。
はじめに
多剤耐性菌(MDRO)は、尿路感染症(UTI)の原因となることが多く、頻繁な入院、薬剤使用、患者の死亡率による病院コストの増加を引き起こしている [1, 2] 。免疫抑制療法は感染感受性をさらに高める可能性があり、固形臓器レシピエントがMDROに汚染されると特に脆弱になります [2, 3]。世界保健機関(WHO)が重要な課題として取り上げている抗菌薬耐性に関連する健康上の負担は、新しいより良い治療法を求めています[4]。
糞便微生物叢移植(FMT)は、健康なドナーからレシピエントに完全な腸内微生物叢を移植することです。FMTは再発性Clostridioides difficile感染症に高い効果を示し[5]、小規模なケースシリーズでは、FMTがMDR関連再発性UTIに苦しむ患者の臨床転帰を改善する可能性を示唆しています[6, 7, 8, 9, 10] 。現在、実験的な最後の手段とみなされているが、FMTは、MDROによるUTIの頻度を減らし、UTIの原因菌の抗生物質感受性を改善する可能性がある[7]。
経済評価は、意思決定者が代替的な介入のコストと結果を測定するのに役立つため、希少な医療資源の優先順位付けに有用な情報を提供することができる [11] 。配分効率に関する適切な情報を提供するために、経済評価は、利用可能な最善の臨床的・経済的証拠、できれば無作為化比較試験のデータに基づいていなければならない。確かなエビデンスに基づかない、すなわち無作為化臨床試験から実施される初期の経済評価は、不確実性とさらなる研究の潜在的利益に対処することを条件に、新興技術の価値を示し、さらなる研究開発の決定を導くことができる[12]。MDRO 関連尿路結石に対する FMT の早期経済効果を評価した先行研究はない。
今回の単施設コホート研究では、MDROに起因するUTI患者に対するFMTの早期経済評価を行うことを目的とし、UTI数、入院日数、病院接触回数、病院関連費用を測定し、FMTの潜在的利用を導く。
方法
これは、2015年から2020年にかけてデンマークの公立消化器科紹介センターで実施された、コホート研究の患者を含むサブグループ解析である。クロストリジオイデスディフィシル感染症の再発で紹介された患者に加えて、腸管MDROキャリア状態および尿培養でMDROの増殖が認められた尿路結石の病歴によりFMTに紹介された患者を連続的に含めた。すべての患者は、徹底的にスクリーニングされた1人のドナーから少なくとも1回のFMTを受け[13]、大腸内視鏡またはカプセルのいずれかによって投与された。本コホートは、当院でFMTに紹介された全患者のサブグループであり、全体のコホート研究はClinicalTrials.gov(研究識別子NCT03712722)に登録されています。
定期的なフォローアップは、FMT後1週間および8週間に全患者を対象に実施された。患者固有のデータ収集は、比較を可能にするため、FMT前(pre-FMT)とFMT後(post-FMT)の期間を同じにし、各患者の可能な限り長いフォローアップ期間を含むようにした。FMT前の期間は、最初のMDRO関連UTIからFMT当日までの期間とした。FMT後の期間は、FMT治療からFMT前の期間と同じ長さのフォローアップ期間までの期間と定義した。
入院および外来通院にかかる費用の推定には、デンマークの診断関連グループ(dkDRG)料金表を使用した。デンマークでは、すべての退院と治療経過にdkDRGを割り当てる必要があり、デンマークのすべての病院をカバーしています。dkDRGの関税は治療コースの平均コスト推定値であり、関税は患者の一次診断、二次診断、年齢、性別、病院との接触または入院期間に基づいて、患者に対する償還を表している。
患者あたりの尿路結石数、入院日数、病院との接触回数などの臨床的健康アウトカムは、電子患者記録を確認することで特定された。デンマークでは、電子患者ファイルには病院との接触に関連するすべての情報が保存されている。すべての病院接触は評価され、月平均コストに計算された。FMTの費用は、どの期間も費用として含まれていない。
臨床的健康結果の比較には対のt検定を適用し、FMT前とFMT後の期間の費用の比較にはウィルコクソン符号順位検定を適用した。臨床的健康結果は中央値と範囲、費用は平均値と95%信頼区間(CI)で報告された。p値<0.05は統計的に有意であるとみなされた。すべてのデータは、Research Data CaptureシステムであるREDCap 9.1.8 (www.redcap.au.dk)からエクスポートされました。統計検定は、STATA/MP 16.0 (STATA Corp.)を用いて実施した。2020年12月31日からの為替レート1DKK=0.1649USDを適用した。
ベースケースの結果の頑健性は、一元的な決定論的感度分析を用いて評価された;1つは最も安価な患者を除外し、もう1つは最も高価な患者を除外したものである。
本試験は、ヘルシンキ宣言に記載されている原則に従って実施されました。すべての患者は、日常的な臨床治療に従って治療を受けた。すべての患者は、中央データベースへの登録に書面によるインフォームドコンセントを行い、連続したコホートを構成している。本研究は品質改善研究として実施され、医療記録へのアクセスはオーフス大学病院の理事会によって承認された。さらに、すべての患者は、この報告書の公表について、書面による具体的なインフォームドコンセントを提供した。データ収集はオーフス大学病院の理事会によって承認され、実験的な治療が行われず、生物学的物質も収集されなかったため、デンマークの法律に従い、地域倫理委員会の承認は必要なかった。本プロジェクトは、デンマークデータ保護庁(Central Denmark Region)に登録された(j.no. 1-16-02-224-16)。
結果
2015年から2020年の間にFMTに紹介され、主な適応症がClostridioides difficileであった患者(合計306人)の連続コホートにおいて、MDRO関連UTIを患う連続紹介患者5人も含まれました。このサブグループは、男性4名と女性1名で構成され、年齢中央値は70歳でした(表1)。5人のうち4人は腎臓移植患者であり、プレドニゾロン、タクロリムス、ミコフェノール酸モフェチルの3種類の免疫抑制治療を受けていた。5人全員がいくつかの併存疾患を抱えており、シャルソン併存疾患指数スコアの中央値は6(範囲4~9)であった。5人の患者のFMT前後の個々の整列期間は60~320日で、中央値は126日であった。
表1 多剤耐性菌(MDRO)保有による二次的な尿路感染症(UTI)により糞便微生物叢移植(FMT)の対象となった患者の臨床的特徴
フルサイズテーブル
患者1人あたりのUTI数は、FMT前が4(範囲1~9)、FMT後が0(0~1)で、FMT治療後に4(1~8)のUTIの減少(p = 0.031)に相当しました(表1、表2)。患者1人当たりの入院日数は、FMT前の中央値15日(12-47日)からFMT後の中央値4日(0-7日)に減少し、FMT治療後は患者1人当たり中央値13日(8-40日)に減少した(p = 0.030)(Table 2)。入院、外来受診、電話連絡、救急外来受診からなる病院接触回数は、中央値28(3-33)から中央値11(4-12)に低下し、患者1人当たり21(1-24)の病院接触回数減少に相当した(p = 0.045)(表2)。
表2 多剤耐性菌関連尿路感染症患者5名における、糞便微生物移植前(FMT前)と後(FMT後)の臨床的健康アウトカム、病院コスト、感度分析
フルサイズテーブル
FMT前期の患者1人当たりの月平均コストは6687米ドル(95% CI 1996-11,379)、FMT後期は1574米ドル(95% CI 0-3920)であった。その結果、FMT前の集団と比較してFMT後の集団では、患者1人当たりの月平均費用が5113米ドル(95% CI 1386-8841, p = 0.043)減少していることがわかった(表2)。
感度分析では、最も安価な患者を除外しても、最も高価な患者を除外しても、臨床的な健康結果は変わらないことが示された(表2)。しかし、費用については、いずれの感度分析でも統計的に有意な差は見られなかった。
考察
この単施設コホート研究では、MDRO関連尿路結石に対してFMTを実施した患者における病院関連費用の早期経済評価を実施した。その結果、患者一人当たりの総病院費用、患者一人当たりの尿路結石数、入院日数、院内接触回数が統計的に有意に減少することがわかった。5人の研究参加者に限られるが、入院と病院関連費用の両方において統計的に有意な減少が見られたことは、均一で顕著な有益な効果を示している。FMTの適用は、5人中4人の患者が免疫抑制療法を受けたにもかかわらず、MDRO関連UTIの数と入院日数の両方が減少することと関連した。
いくつかの小規模な研究では、ESBL産生大腸菌や多剤耐性肺炎桿菌など、腸内にMDROを保有する患者に対するFMTの使用を調査した[6、7、9、10]。これらの研究と同様に、我々は患者あたりのUTIの数が著しく減少していることを発見しました。最近の研究では、FMT後の入院日数が大幅に減少したことが示されている[10]。本研究の結果と合わせると、UTIの減少が入院や病院との接触の減少につながり、集団の臨床的健康の改善を示すが、必ずしもMDROを根絶するわけではない、という仮説が成り立つ[14]。
本研究では、病院との接触を評価するために DRG タリフを使用した。特定の患者のコストは平均的なコストと異なる可能性があるため、マイクロコストアプローチを使用することで、コスト推定の精度を向上させることができたと考えられる。我々は、より正確な推定が、この初期の経済評価の結論を変える可能性は低いと考えている。費用対効果を評価する際には、FMTの適用に直接関連する費用を考慮する必要がある。我々は以前、FMTサービスの初期開発段階において、ドナーの募集とスクリーニング、実験室での処理、およびドナーの糞便の臨床応用に関連する総コストを算出し[15]、最近、FMTサービスの完全開発段階における最新のコスト推定を発表した[16]。本研究では、FMTのコストは開発レベルや適用方法によってかなり異なるため、病院コストの計算に含めなかった。大腸内視鏡 FMT 1 回あたりの総費用 3519 米ドルと、本研究で削減された患者 1 人あたりの月間病院費用 5113 米ドルを比較すると、FMT の使用は非常に費用対効果が高いことがわかる。カプセル化された製剤の使用など、FMTの適用が改良されれば、治療効果がさらに向上する可能性があり、将来の患者コホートでコスト評価が行われる必要がある。
MDROキャリアの状態は、FMTの治験適応であることに変わりはない。これらの患者におけるFMTの使用に関する高レベルのエビデンスを得ることは、患者が少数かつ不均一であるにもかかわらず、経済的負担が大きいため困難である。最近の多施設共同無作為化臨床試験は、患者の組み入れが不十分であったため、早期に中止された[14]。本研究に含まれる患者は、MDRO関連UTIのすべての患者を代表するものではない可能性があるが、我々の小さな患者サンプルで示されたFMTの著しい医療経済的利益は、FMTが費用対効果の高い選択肢である可能性を裏付けている。いずれにせよ、FMTによって得られる個々の患者の健康上の利点は、患者に合わせたレジメンの開発につながるはずです。また、臨床的な有意な改善は、QOLの改善の可能性を示しており、今後の研究では、FMTが健康関連のQOLや社会的な追加コストに与える影響について評価する必要がある。
結論
MDROキャリッジを根絶するためにFMTを使用することで、UTIの発生と関連する病院費用が顕著に減少した。この戦略は費用対効果に優れていることが示唆された。
参考文献
Serra-Burriel M, Keys M, Campillo-Artero C, et al. 多剤耐性菌が成人の医療関連感染の経済的・臨床的アウトカムに与える影響:系統的レビューとメタアナリシス。PLoS ONE. 2020;15(1): e0227139.
記事CAS PubMed PubMed Central Google Scholar
ダドゴスターP. 抗菌薬耐性:その意味とコスト。Infect Drug Resist. 2019;12:3903-10.
記事CAS PubMed PubMed Central Google Scholar
Al Midani A、Elands S、Collier S、Harber M、Shendi AM. 腎移植レシピエントにおける尿路感染症の影響:4年間の単一施設の経験。Transpl Proc. 2018;50(10):3351-5.
記事CAS Googleスカラー
(WHO) WHO. 世界各国の状況分析:抗菌薬耐性への対応。ジュネーブ: WHO; 2015.
グーグル・スカラー
Baunwall SMD、Lee MM、Eriksen MK、他 再発性Clostridioides difficile感染症に対する便微生物移植:最新の系統的レビューとメタアナリシスです。EClinicalMedicine. 2020;29-30: 100642.
記事 PubMed PubMed Central Google Scholar
Stalenhoef JE, Terveer EM, Knetsch CW, et al. 多剤耐性グラム陰性菌に対する糞便微生物叢移植:微生物学的失敗を伴う臨床的成功。オープンフォーラム Infect Dis. 2017;4(2):ofx07.
記事 グーグル スカラ
Tariq R、Pardi DS、Tosh PK、Walker RC、Razonable RR、Khanna S. 再発性クロストリジウム・ディフィシル感染症に対する糞便微生物叢移植は、再発性尿路感染症頻度を減少させる。Clin Infect Dis. 2017;65(10):1745-7.
記事CAS PubMed Google Scholar
Biehl LM, Cruz Aguilar R, Farowski F, et al. 再発性尿路感染症を有する腎臓移植レシピエントにおける糞便微生物叢移植の実施。Infection. 2018;46(6):871-4.
記事 PubMed Google Scholar
Grosen AK、Povlsen JV、Lemming L、Jørgensen SMD、Dahlerup JF、Hvas CL. 尿路感染症を再発した腎移植レシピエントから、糞便微生物移植により広域βラクタマーゼ産生Klebsiella pneumoniaeを根絶した。Case Rep Nephrol Dial. 2019;9(2):102-7.
記事 PubMed PubMed Central Google Scholar
Ghani R, Mullish BH, McDonald JAK, et al. 脱コロニーではなく疾病予防:多剤耐性菌に汚染された患者への糞便微生物移植のモデル。Clin Infect Dis. 2021;72(8):1444-7.
記事 PubMed Google Scholar
ドラモンド MF. ヘルスケアプログラムの経済的評価のための方法。第4版. オックスフォード; 2015.
グーグル スカラー
Love-Koh J. 初期の経済モデルはどの程度有用か?Health Technologiesの問題と約束」に対するコメント: 初期の医療経済モデリングの役割". Int J Health Policy Manag. 2020;9(5):215-7.
PubMed Google Scholar
Jørgensen SMD、Erikstrup C、Dinh KM、Lemming LE、Dahlerup JF、Hvas CL. 献血者における糞便提供者の募集: 観察コホート研究からの結果。Gut microbes. 2018;9:540-50.
PubMed Central Google Scholar
Huttner BD, de Lastours V, Wassenberg M, et al. 多剤耐性腸内細菌科細菌のキャリッジを根絶するための5日間の経口抗生物質のコースと糞便移植:無作為化臨床試験。Clin Microbiol Infect. 2019;25:830-8.
記事CAS PubMed Google Scholar
Dehlholm-Lambertsen E, Hall BK, Jorgensen SMD, et al. 再発性クロストリジウム・ディフィシル感染症に対する糞便微生物移植によるコスト削減効果. Ther Adv Gastroenterol. 2019;12:1756284819843002.
記事 グーグル スカラ
Baunwall SMD, Andreasen SE, Hansen MM, et al. Clostridioides difficile感染症の初回および2回目のエピソードに対する糞便微生物移植-著者らの回答-. Lancet Gastroenterol Hepatol. 2023;8(2):112-3.
記事 PubMed Google Scholar
リファレンスのダウンロード
謝辞
本研究の参加者に感謝する。
資金提供について
Christian L. HvasとLianna Hammekenは、Innovation Fund Denmark (j.no. 8056-00006B)からプロジェクト資金を受け取った。Christian L. Hvasは、Novo Nordisk Foundation(助成金番号:NNF22OC0074080)からプロジェクト資金を得た。本誌の迅速なサービス料は、著者らの資金で賄われている。
著者名
すべての著者は、国際医学雑誌編集者委員会(ICMJE)の著者資格の基準を満たし、データの完全性に責任を持ち、本論文の掲載を承認しています。
著者貢献度
Olivia D. Baek、Camilla K. Hjermitslev、Line Dyreborg、Simon M. D. Baunwall、Katrine L. Høyer、Nina Rågård、Lianna H. Hammeken、Johan V. Povlsen、Lars H. Ehlers、Christian L. Hvasが研究の構想および設計に寄与した。資料作成、データ収集、分析は、Olivia D. Baek、Camilla K. Hjermitslev、Line Dyreborgが行った。原稿の第1稿は、Simon M. D. BaunwallとKatrine L. Høyerが執筆した。原稿の重要な修正と補足データの収集は、Katrine L. HøyerとNina Rågårdによって行われた。グラフィカルなプレゼンテーションは、Nina Rågårdが行った。すべての著者が原稿に重要な意見を提供した。すべての著者が最終原稿を読み、承認した。
開示事項
Olivia D. Baek, Camilla K. Hjermitslev, Line Dyreborg, Simon M. D. Baunwall, Katrine L. Høyer, Nina Rågård, Lianna H. Hammeken, Johan V. Povlsen, Lars H. Ehlers and Christian L. Hvas は利益相反を宣言しない.Lars Holger Ehlersは、原稿執筆中に所属機関をDanish Centre for Healthcare Improvements, Department of Clinical Medicine, Aalborg University, Aalborg, DenmarkからNordic Institute of Health Economics, Aarhus, Denmarkへ変更した。
倫理指針の遵守
本研究は、ヘルシンキ宣言に記載されている原則に従って実施された。すべての患者は、日常的な臨床治療に従って治療を受けた。すべての患者は、連続コホートを構成する中央データベースへの登録に書面によるインフォームドコンセントを提供した。本研究は品質改善研究として実施され、医療記録へのアクセスはオーフス大学病院の理事会によって承認された。さらに、すべての患者は、本報告書の公表について、具体的なインフォームド・ライセンスを書面で得た。データ収集はオーフス大学病院の理事会によって承認され、実験的な治療が行われず、生物学的物質も収集されなかったため、デンマークの法律に従い、地域倫理委員会の承認は必要なかった。本プロジェクトは、デンマークデータ保護庁の中央デンマーク地域(j.no. 1-16-02-224-16)に登録されました。
データの利用可能性
本研究で生成され、分析されたデータセットは、合理的な要求があれば、データ保護指令の要求に従って匿名化した上で、対応する著者から入手可能である。
著者情報
著者ノート
Olivia Dybro Baek, Camilla K. Hjermitslev, Line Dyreborg: equal contributions.
著者と所属
オールボー大学デンマーク医療改善センター臨床医学科(デンマーク・オールボー市
オリビア・ダイブロ・ベク、カミラ・K・ヒェルミツレフ、ライン・ダイレボルグ、リアナ・H・ハンメケン&ラーズ・H・エーラス
オーフス大学病院 肝臓・消化器科(Palle Juul-Jensens Boulevard 99, 8200, Aarhus N, Denmark
サイモン・M・D・バウンウォール、カトリーネ・L・ホイヤー、ニナ・ローゴード、クリスチャン・ロドベルグ・ハヴァス
オーフス大学病院腎臓内科(デンマーク、オーフス市
ヨハン・V・ポヴルセン
対応する著者
オリビア・ダイブロ・バエクまたはクリスチャン・ロドベルグ・ハヴァス宛に通信してください。
その他の情報
出版社ノート
シュプリンガー・ネイチャーは、出版された地図や機関名における管轄権の主張に関して中立を保っています。
権利と許可
オープンアクセス この記事は、クリエイティブ・コモンズ 表示-非営利 4.0 国際ライセンスの下でライセンスされています。このライセンスは、原著者と出典に適切なクレジットを与え、クリエイティブ・コモンズのライセンスへのリンクを提供し、変更を加えた場合にそれを示す限り、あらゆる媒体や形式での非商業的な使用、共有、適応、配布および複製を許可します。この記事に掲載されている画像やその他の第三者の素材は、素材へのクレジット表示で別段の指示がない限り、記事のクリエイティブ・コモンズ・ライセンスに含まれています。素材が記事のクリエイティブ・コモンズ・ライセンスに含まれておらず、あなたの意図する使用が法的規制によって許可されていない場合、または許可された使用を超える場合、あなたは著作権者から直接許可を得る必要があります。このライセンスのコピーを見るには、http://creativecommons.org/licenses/by-nc/4.0/。
転載と許可
この記事について
この記事を引用する
Baek, O.D., Hjermitslev, C.K., Dyreborg, L. et al. 多剤耐性菌による尿路感染症患者に対する糞便微生物移植の早期経済性評価. Infect Dis Ther (2023). https://doi.org/10.1007/s40121-023-00797-y
引用元:ダウンロード
2023年1月14日受理
2023年3月27日受理
2023年4月16日発行
DOIhttps://doi.org/10.1007/s40121-023-00797-y
この記事を共有する
以下のリンクを共有した人は、このコンテンツを読むことができるようになります:
共有リンクを取得する
コンテンツ共有イニシアティブ「Springer Nature SharedIt」により提供されます。
キーワード
初期の経済評価
糞便微生物移植術
病院費用
エムディーオー
多剤耐性
1,000万件以上の科学文献を指先で確認できる
スイッチ版
アカデミック版
コーポレートエディション
ホーム
インプレスム
法務情報
個人情報保護方針
カリフォルニア州プライバシーステートメント
Cookieの使用方法
Cookieを管理する/私のデータを販売しない
アクセシビリティ
よくあるご質問
お問い合わせ
アフィリエイトプログラム
ログインしていない - 118.8.198.0
所属していない
シュプリンガー・ネイチャー
© 2023 Springer Nature Switzerland AG. シュプリンガー・ネイチャーの一部です。
この記事が気に入ったらサポートをしてみませんか?
