幼児期ハウスダスト暴露と喫煙と肺気腫発症の関連
幼児期ハウスダスト暴露と喫煙と肺気腫発症の関連
Fung, Nok Him, Quynh Anh Nguyen, Catherine Owczarek, Nick Wilson, Nadeem Elahee Doomun, David De Souza, Kylie Quinn, ほか. 「Early-life house dust mite aeroallergen exposure augments cigarette smoke-induced myeloid inflammation and emphysema in mice」. Respiratory Research 25, no. 1 (2024年4月13日): 161. https://doi.org/10.1186/s12931-024-02774-6 .
背景
縦断的研究により、幼少期の喘息が閉塞性肺疾患(COPD)や喘息-COPD重複症(ACO)のリスク因子であることが特定されました。これらの状態では、持続的な気流制限がより積極的に発展する可能性があります。しかし、幼少期の喘息とCOPD/ACOとの間の因果関係はまだ確立されていません。本研究は、幼少期の喘息とCOPDの自然史をモデル化し、病気の進行を促進する細胞/分子メカニズムを調査することを目的としています。
方法
3週齢の若いC57BL/6マウスに対して、ハウスダストダニ(HDM)抽出物を用いてアレルギー性気道疾患を確立しました。その後、マウスは8週間にわたりタバコの煙(CS)とHDMに曝露されました。肺の気泡拡大(肺気腫)は平均線間隔法によって測定されました。フローサイトメトリーを用いて肺免疫細胞の表現型を調べました。肺組織にはバルクRNAシークエンシングが実施されました。気管支肺胞洗浄液中の揮発性有機化合物(VOC)が分析され、病気特有のバイオマーカーをスクリーニングしました。
結果
慢性的なCS曝露は肺気腫を誘発し、HDM暴露によって著しく増加しました。肺気腫の変化の増加は、好中球、間質性マクロファージ、好酸球、リンパ球などの免疫細胞の肺への浸潤が増加することと関連していました。
トランスクリプトーム解析により、HDMまたはCS単独で誘発された病気特有の変化がHDM-CS群でも保存されていることが確認され、さらにMmp12、Il33、Il13の濃縮およびマクロファージの代替的な活性化の拡大と一致する遺伝子発現が明らかになりました。
VOC分析では、CS曝露により増加した4つの化合物が、逆説的にHDM-CS群で減少していることが特定されました。
結論
初期のアレルギー性気道疾患は、CSに曝露されたマウスの肺気腫の病理を悪化させ、肺トランスクリプトームを著しく変化させます。
序文要約:
喘息と慢性閉塞性肺疾患(COPD)は、異なる病理学的・免疫学的特徴を示す気流障害を特徴とする慢性肺疾患です。
COPDは肺気腫、慢性気管支炎、または遠位気道の線維化改造による固定的な気流障害によって特徴づけられます。
喘息は可逆的な気道過敏性であり、吸入ステロイドや気管支拡張薬に非常に反応が良いです。
これらの臨床特徴は、診断と治療を複雑にする喘息-COPD重複症(ACO)として患者に重複することがあります。
ACOの起源は明らかではないが、「ダッチ仮説」により喘息とCOPDは共通の起源を持つ可能性が支持されています。
縦断研究により、幼少期の喘息は後にCOPDを発症する重要なリスク因子とされ、早期の肺機能障害と男性が重要な予測因子とされます。
研究により、幼少期の不利な出来事(例:喘息、早産)は成人期に至るまでの肺機能の持続的かつ加速された低下を引き起こし、攻撃的な形のCOPDを発症する可能性があることが示されました。
動物モデルを用いた前臨床研究では、ACOのモデル化のためにCOPDとアレルギー性喘息の確立されたモデルが組み合わされました。
この研究の主な目的は、幼少期の喘息が成人後のCOPD発症に及ぼす影響を調査し、転写体分析を通じてその病理生理学的メカニズムを明らかにすることでした。
早期にHDMアレルゲンに挑戦されたマウスは成人期のCS(タバコの煙)曝露によりより悪化した肺気腫を発症しました。
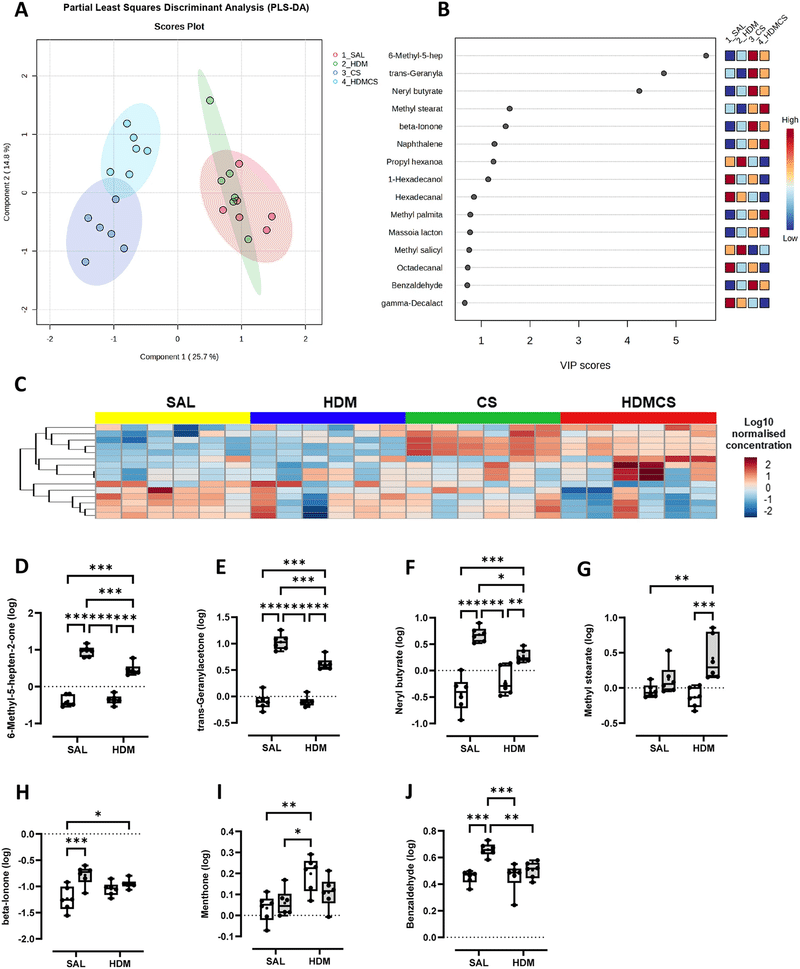
Discussion要約
幼少期の喘息は成人後のCOPDリスクを増加させる、特に喫煙者において。
研究では、HDM(ハウスダストマイト)曝露による早期のアレルギー性気道疾患が、マウスのCOPD発症を加速させるかどうかを調査。
HDMとCS(タバコの煙)に同時に曝露されたマウスは、CSのみに曝露されたマウスに比べて、肺気腫と肺のリモデリングが悪化。
肺リモデリングはLm値の増加、ECM遺伝子Ecm2と細胞接着分子2(Cadm2)のダウンレギュレーション、ムチン遺伝子Muc5acのアップレギュレーションによってサポートされた。
RNAシーケンスとqPCR分析により、CSに曝露されたマウスの肺気腫がCOPD感受性遺伝子Mmp-12の発現上昇とともに現れることが明らかになった。
CSとHDMの二重曝露は、さらに肺の空間拡大とリモデリングを拡大し、Mmp12の発現を増加させた。
このモデルは、COPDの病理生理をさらに調査し、エンドタイプ特異的治療法を開発するために使用できる。
この記事が気に入ったらサポートをしてみませんか?
