記事抜粋146
本文はこちら:記事抜粋146 | LinkedIn
Previously, 記事抜粋145 | LinkedIn
[1] 2020年の記事だが:波乗りする電子: 流れに沿うという法則を破る電子 | 沖縄科学技術大学院大学(OIST)


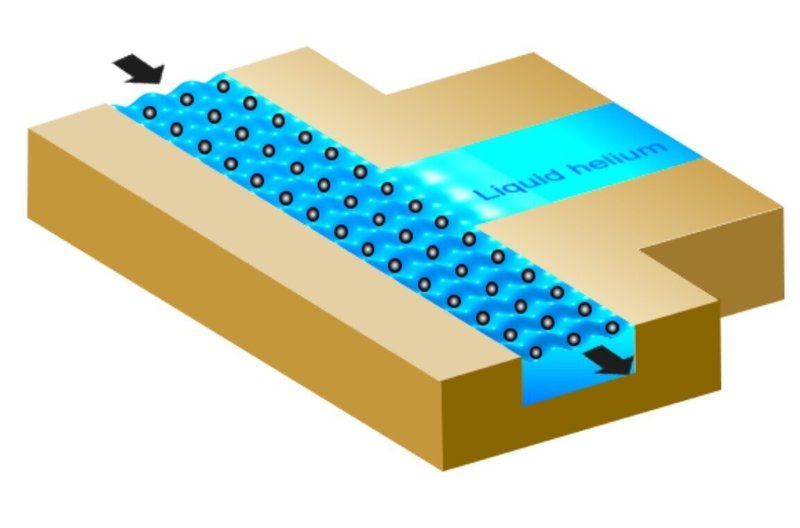
「しかしながら、電子が固体ではなく液体上にある場合、オームの法則が破られる可能性があります。私たちはこのことを実験で測定したいと思いました。」と、コンスタンチノフ准教授は説明します。
高温超電導の研究で1986年のノーベル物理学賞を受賞したミューラー(ベドノルツと共同受賞。ちなみに、2005年の箱根の学会で、俺は本人と気づかずにベドノルツと一緒に昼飯を食いながら雑談していた。午後一の基調講演で初めて気づいた。何しろ、1986年の写真ではバルデラマのような頭髪をしてらしたから・・・。)が電子ドープしたSrTiO3の超電導相転移はXY型ではないかと言っている。
だから俺は疑似二次元として、ポーラ論直径相当の膜厚の電子ドープSrTiO3単結晶薄膜で実験していたんだね:Vacuum Polarization, and Polariton (2018). IBMに先にやられてしまったが(IBMは高密度レーザーで誘起分子のexciton-polaritonを一気に励起して室温Bose-Einstein凝縮を2008年に報告した。超電導ではなく超流動だったが。)、2005年に紫外線照射による電子励起と同時に特定は超の遠赤外線照射による特定格子振動を励起することで一瞬なら室温超電導もできるかもしれないよって話をしていた。
ま、そんなこと言ってたら日本じゃ邪魔されますわ(笑)。
で、代わりにやったのが酸素センサ(笑)。ま、こっそりお話したシンクタンクの人に「なんかやらせてあげられないか経済産業省に話をしてみるけど、実用性も少し考えてね。」とは言われてました。
結果は、研究者が予測した通りのものとなりました。 リプル・ポーラロンは、オームの法則ではなく、運動量保存の法則に従い、左の電子の溜池から右の電子の溜池まで、まっすぐノーベル物理学賞
固体内の話をすると、これが粒界の存在が望ましくない理由なんだね:Vacuum Polarization, and Polariton (2018).
[2] 商品説明だが:ショットキーバリアダイオードの構造、特徴、用途 【Analogista】
ショットキーダイオードは金属と半導体を接合して作られています。
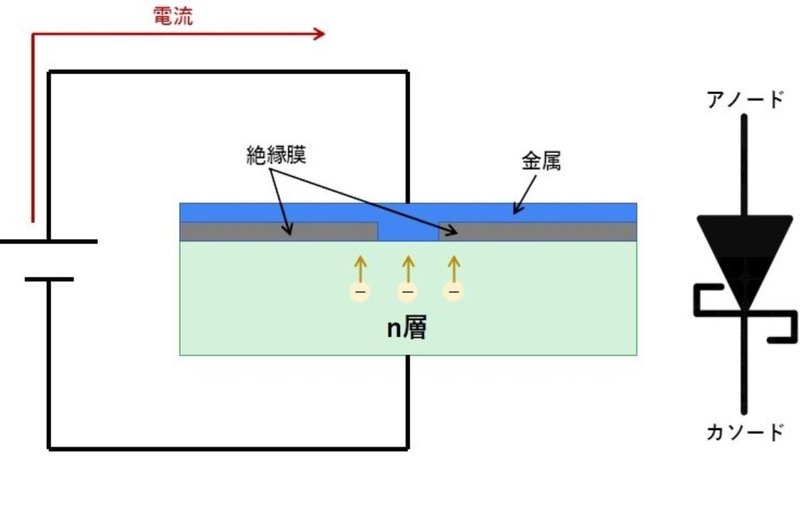
pn接合ダイオードと違い、ショットキー障壁を用いて整流動作を行います。
金属とn型半導体を接触させた際のエネルギーバンド図を見てみましょう。
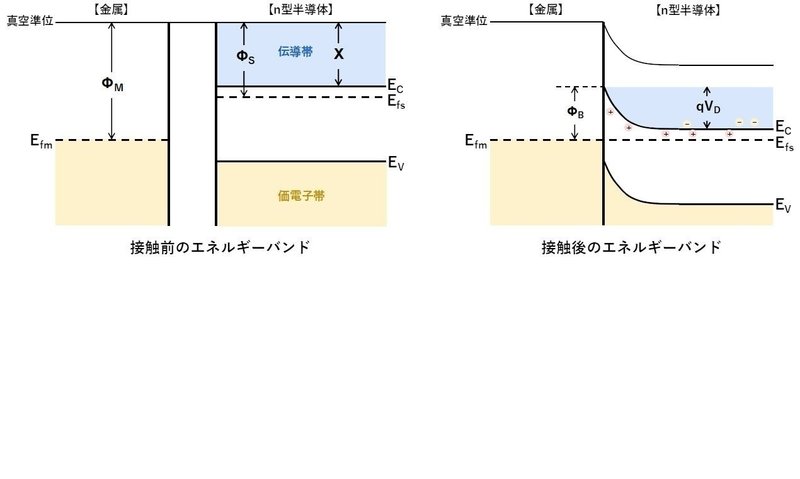
金属とn型半導体を接触させるとキャリアが両方の領域を行き来できるようになり、平衡状態に達してフェルミ準位が一致します。
フェルミ準位が一致するのは平衡状態に達したときな。
非平衡状態では一致していないのな:Fermi Level (2018).
このとき、半導体の伝導帯は金属の伝導電子より高いエネルギーを持っているため、電子が金属側へ移動して半導体はプラスに帯電しています。
その結果、伝導帯の底:Ecは低下してqVDの曲がりが生じます。
次に、金属-半導体間に順方向電圧:Vを印加した場合を考えます。
ΦBは材料の組み合わせで決まるため、バイアスを印加しても変化しません。
しかし、半導体側の障壁:qVDはqVだけ低くなりq(VD – V)となります。
一方、金属側の障壁の高さは変わらないため、金属側から半導体側への電子の移動量は変化しません。
結果、半導体側から金属側にだけ電子が流れることになるので、金属(アノード)から半導体(カソード)へ電流が流れることになります。
このように、ショットキー接合はpn接合と異なり多数キャリアの移動によって電流が流れます。
pn接合ダイオードの問題であった少数キャリアの蓄積が起こらないため、高速応答ができるという特徴を持ちます。

ショットキーバリアダイオードの長所と短所について解説していきます。
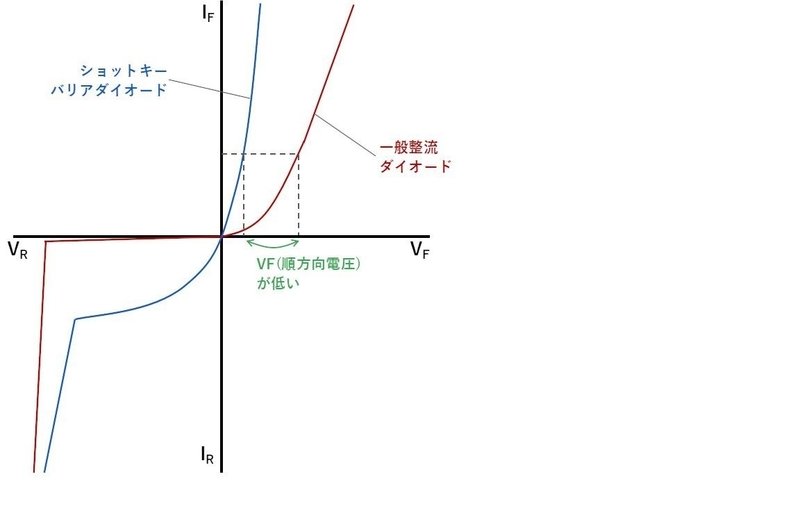
下図のVI特性のグラフの通り、ショットキーダイオードはpn接合ダイオードに比べ順方向電圧がかなり小さくなります。
順方向電流によって変化しますが、極端に電流が大くなければ0.4V程度です。
したがって、導通時の電力損失を低く抑えられるというメリットがあります。
応答速度が速い
ファストリカバリダイオードと比べても応答時間(逆回復時間)が短いという特徴を持ちます。
サイズにも依りますが、数nsでオン→オフに完全に切り替わります。
そのため、数百kHz〜数MHzのスイッチング回路で使うことができます。
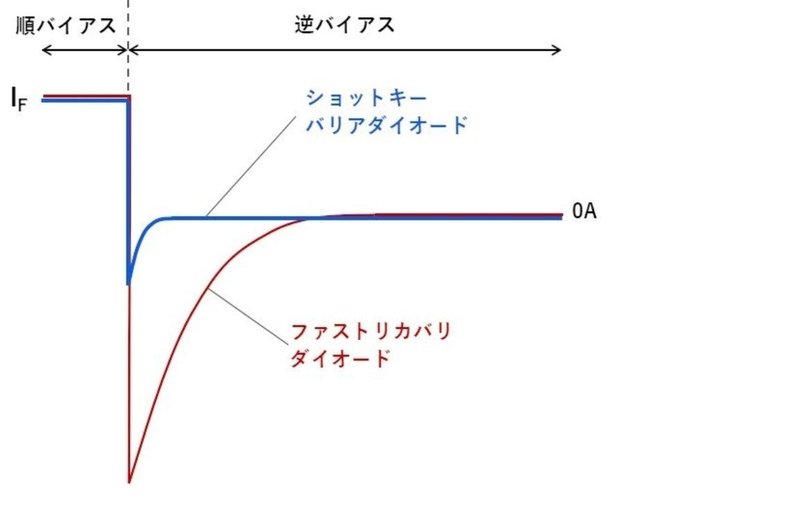
ショットキーダイオードのデメリットは漏れ電流(逆方向電流)が大きいことです。
特に高温で急激に増加するため、次に説明する熱暴走が起こらないように注意する必要があります。
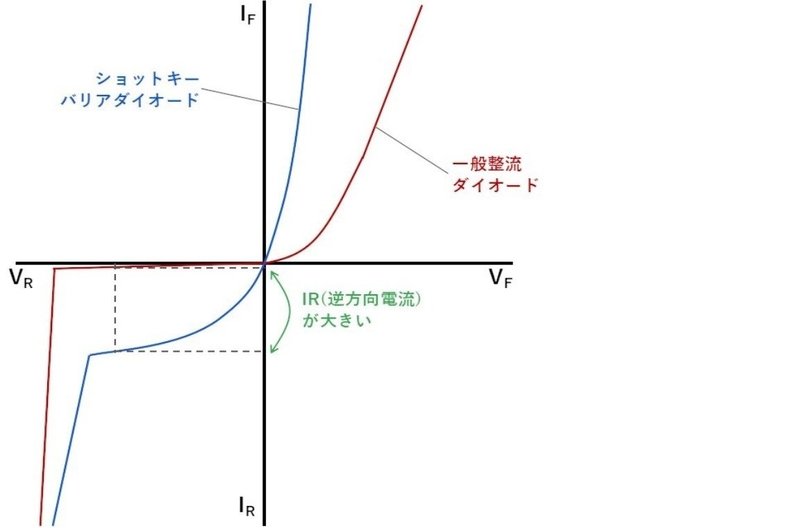
逆方向電流が大きく立ち上がってるところはSiショットキーダイオードの場合thermionicなんだが・・・。
最初のバンドダイアグラムに戻って浅いドナー準位だけでなく深いまだイオン化されていないドナー準位が有る場合はショットキーバリアが薄くなれるからトンネリング電流が流れ得るんだよ:Fermi Level (2018). Intentionally inserted oxygen depleted (Ba/sub 0.5/Sr/sub 0.5/)TiO/sub 3/ layers as a model of DC-electrical degradation | IEEE Journals & Magazine | IEEE Xplore
ReRAMの動作原理はたぶんこれなんだが。フィラメントが貫通しない薄い絶縁層を設けたほうが動作が安定するが、ここはトンネリングできるんだね。
熱暴走とは、ショットキーダイオードの温度と逆方向電流が収束せず上昇し続ける現象です。
逆バイアス電圧が大きいと逆方向電流も大きくなるため、逆バイアス時の電力損失が大くなります。
損失によりダイオードの温度が上昇し、逆方向電流が増加します。
電流増加によりさらに損失が増加、温度が上昇して逆方向電流が増えるというサイクルが発生します。
熱暴走が起こらないよう、使用環境温度の最大温度、最大電圧条件での逆方向電流、電力損失が十分小さいことを確認する必要があります。
バッテリラインの断線時などにバッテリ側に逆流しないようにするため、機器の電源の入口にショットキーダイオードを用いて逆流を防止します。
逆バイアス時のリーク電流が問題ないレベルかを確認しておきましょう。
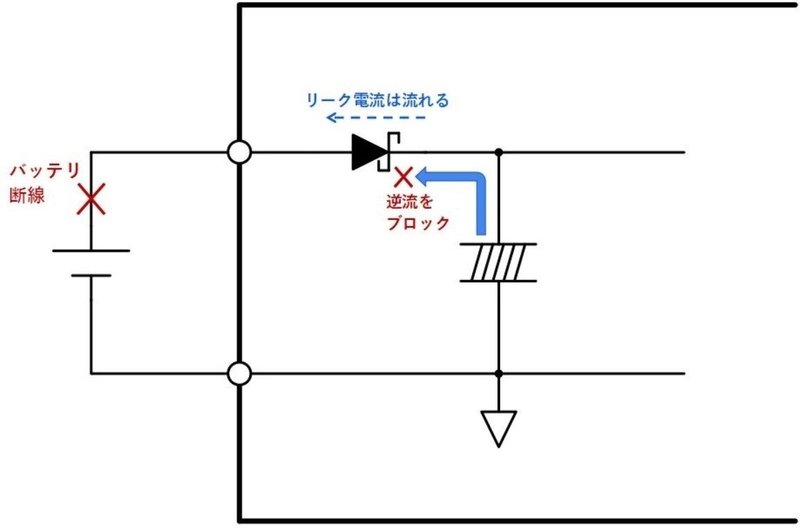
負電圧に弱いLSIを守るため、負電圧が印加される可能性がある端子とGND間にショットキーダイオードを挿入し、-VF以下になるようにLSIの端子を保護します。
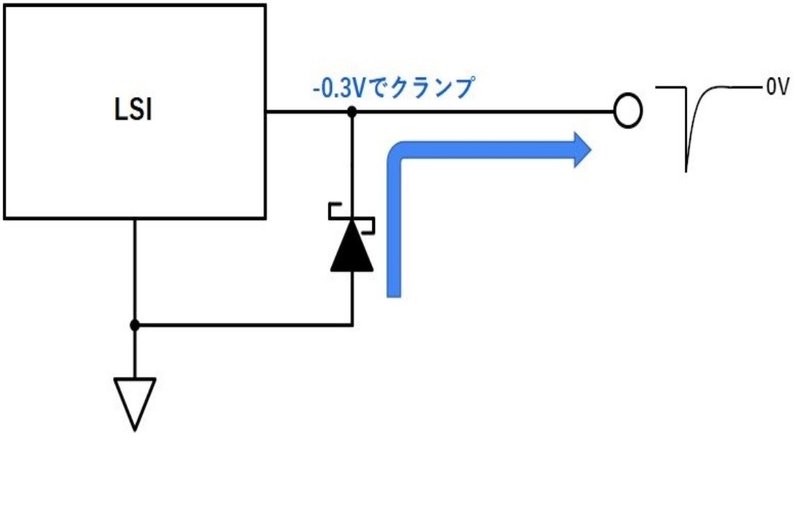
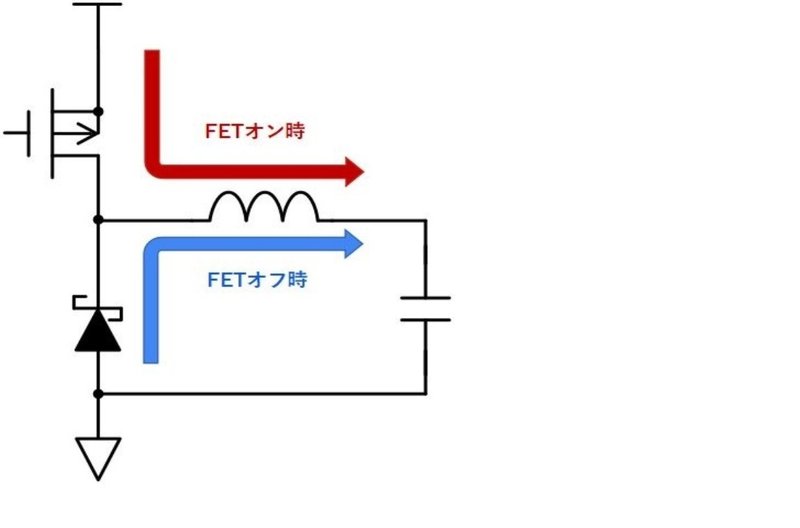
数百kHz〜数MHzのスイッチング周波数で動作させるDCDCコンバータ(スイッチングレギュレータ)で使われます。
逆回復時間が短いので、スイッチング切り替わり時の逆回復電流を小さく抑えることができるので、ノイズ低減効果もあります。
[3] 一昨年の記事だが:EV向け固体電池が本格量産へ、電解質は半固体が主流 | 日経クロステック(xTECH) (nikkei.com)

これじゃ、ほとんど樹脂のイオン伝導度で性能が決まってしまうわね・・・。抵抗が高いからジュール熱で温度が上がってPEOが使い物になる60℃くらいになって動作してんだけど・・・。
電解質のすべてに固体材料を用いた電気自動車(EV)向けの全固体電池もしくは、液体材料と固体材料を組み合わせた半固体電池の本格量産が間近かに迫ってきた(図1、表1)。
ということで、酸化物/高分子コンポジット型は高分子に電解液を含ませたゲル(半固体と言ったりもするね)にする場合が多いんだが、電解液のイオン伝導度で性能が決まっているのね。電解液をそのまま使ったほうが性能はいいわな。
Electrochemical Impedance Analysis for Li-ion Batteries (2018)のここ、参照:
*1: Lithium ion diffusion in the intercalation materials
Microvoltammetric Studies on Single Particle Voltammetry of LiNiO2 and LiCoO2. In situ Observation of Particle Splitting during Li-ion Extraction/Insertion (1997): Micro-voltammetry for oxide particles of micrometer sizes has been applied to investigate Li+ ion extraction/insertion processes of LiCoO2 and LiNiO2 prepared by a citrate complex method. ... まあ、俺はこれを読んで「こんなに応答(懸念していたのは固体内拡散)が速いんならリチウムイオン電池は車載用にも使えるね」と思ってエレクトロニクスから浮気してしまったってわけだ、2年ほど。単一粒子だから周りに電解液が十分たくさんに有るからでもあるんだけどね。本質的には速いわけ。
High Resolution Cyclic Voltammograms of LiMn2-xNixO4 with a Microelectrode Technique (1998): Lithium-ion insertion/extraction at a single particle (10-30 μm in diameter) of LiMn2-xNixO4 (x = 0, 0.2, 0.5) was characterized by a microelectrode technique, in which a fine metal filament was manipulated to make electrical contact with the particle placed in 1 M LiClO4/PC+EC solution. By using this technique, we can evaluate the correct current-potential behavior of LiMn2-xNixO4 without any dilution due to an organic binder and a conductive additive. ... ワイヤに活物質をデポしてるからだいぶ活物質量は増えてるが十分に速い。
High-Speed voltammetry of Mn-doped LiCoO2 using a microelectrode technique (2000): The microelectrode technique was applied to investigate the electrochemical properties of LiCo1-xMnxO2 (x = 0, 0.01, 0.05, 0.2, or 0.5) synthesized using the citrate process. ... Mnドープで格子が広がってさらに固体内拡散が速くなる。
Effect of Hetero-contacts at Active Material Conductive Additives on Lithium Intercalation/Deintercalation of LiCoO2 (1998): The effect of heterocontacts at electroactive material conductive additives on electrochemical lithium intercalation/deintercalation to LiCoO2 have been investigated by using the pure and binder-free LiCoO2 thin film electrode and the pellet electrode of the pellet of LiCoO2 electroactive material powder, conductive additive and organic binder. It was found that the transport rate of lithium ion inside these pellet electrodes had quite different values in anodic and cathodic polarization, and it strongly depends on the amount of conductive additive and the material itself. These behaviors could not be explained by the penetration of the organic electrolyte solution and by the concentration gradients as a driving force of lithium ion transport inside the LiCoO2 lattice. Carbon conductive additive drastically increased the rate of lithium ion transport inside the pellet electrode and LiCoO2 active material. This effect was remarkably large in cathodic polarization than that in anodic polarization.酸化側と還元側とで挙動が違うのは電解液のせいだと言ってるわけ。
Architectures of Positive Electrodes for Rapid Charging/Discharging Performances of Lithium Ion Secondary Batteries (2003): ... LiMn2O4 active material had the maximum high charging/discharging rate of 720C at least. 容量が全部使えているわけではないが、720Cって5秒で充放電できますわってこと。
Express Charging/Discharging Lithium Ion Secondary Batteries (2008): It, kind of, says that the contact resistance between Al/ALF3/carbon and the positive active material particle is lower than between Al/ALF3 and the positive active material particle since the carbon/the positive active material particle contact is quasi-ohmic -- some of d-electrons near the carbon are eliminated into the particle, then, holes are doped. Au and Pt are better than carbon, however, costly (but good for verification experiment).xn-- -73t8ipc1
gf5h5eo407ajzrq90f4jxbfc8a.Electrochemical performance of single Li4Ti5O12 particle for lithium ion battery anode (2019): ... Li+ extraction (discharge) was faster than Li+ insertion (charge) because of the difference in Li+ diffusion into the single Li4Ti5O12 (LTO) particle, thereby exhibiting remarkable discharge capacity retention (>80%) even at 1,000C and 10 °C. ... 容量が全部使えているわけではないが
、1,000Cって3.6秒で充放電できますわってこと。Express Charging/Discharging Lithium Ion Secondary Batteries (2008): Positive active materials particles directly deposited onto Au or Pt without binder exhibited faradaic response at e.g., 360 C for LiCoO2, 36,000C for LiMn2O4 and LiFePO4, and 600C for graphite. 容量が全部使えているわけではないが、
36,000Cって0.1秒で充放電できますわってこと。
*2: But only with the enough amount of lithium ions near the active-material particles.
Express Charging/Discharging Lithium Ion Secondary Batteries (2008): So, the lithium ion diffusion in the intercalation materials is fast enough.
*1の話を仁科がまとめている。
電解液量の話として俺が補足しておいたのが以下: I am going to explain what Nishina wanted to say: (i) The electrode porosity in which an electrolyte solution is reserved is, e.g., 30 vol%, then the cathode density becomes 3.5 g/cm^3. The weight ratio of the positive active material (theoretically 5 g/cm^3) is, e.g., 94%, then after 50% deintercalation (e.g., 136 mAh/g for the reaction, LiCoO2 -> 0.5 Li+ + Li0.5CoO2), 16.8 mmol/cm^3 of lithium ions are required in order to re-intercalate to become LiCoO2. (ii) Available Li+ in the 1 mol/L of the electrolyte solution that is reserved in the electrode pore is only 0.3 mmol/cm^3 (1.8% of 16.8 mmol/cm^3); thus, in order to refill the Li+ ion into Li0.5CoO2, the offshore Li+, which is reserved in the separator that has only 0.3-0.4 mmol/cm^3 of Li+ (40% of porosity is assumed), is required. (iii) When the electrode thickness is 100 um and the separator thickness is 25 um, the offshore Li+ can only supply 0.6% of 16.8 mmol/cm^3. (iv) Thus, Only 1.8% + 0.6% = 2.4% of Li+ is available in the electrolyte solution. (v) Under the rocking-chair scheme, this is still OK at a relatively low C rate, since the extracted Li+ from the cathode comes back from the anode (unfortunately, less than 100%, though.). (vi) However, the enough amount of Li+ is not supplied to the active materials at a high C rate because of the concentration polarization in the liquid-based electrolyte.
The higher porosity (the more Li+ in the electrode), the reaction occurs in a more homogeneous manner: 空孔率が高くて電解液が電極の中にたくさん有ったほうが均一に(速く)反応が起こるって言ってんの。
まあ、早い話が「ゲルなんか使う気にならねえ」って話なんだよ。やるんなら硫化物全固体電池をやっちゃえと・・・。
by T. H.
LinkedIn Post
[1] Materials/Electronics
[2] Electrochemistry/Transportation/Stationanergy Storage
Electrochemical Impedance Analysis for Li-ion Batteries (2018).
Progresses on Sulfide-Based All Solid-State Li-ion Batteries (2023).
Electrochemical Impedance Analysis for Li-ion Batteries 2 (2023).
[3] Power Generation/Consumption
Electric-Power Generation, Power Consumption, and Thermal Control (2020).
Electric-Power Generation, Power Consumption, and Thermal Control 2 (2023).
[4] Life
[5] Life Ver. 2
[6] 経済/民主主義
Published Articles' List (2004-2005, 2008-2011, 2015)
この記事が気に入ったらサポートをしてみませんか?
