
2021東京大学入試問題二次試験 化学 第2問解答解説
2021東京大学入試問題 化学 第2問の解答解説です。最難関レベルの勉強をしっかりしていれば,比較的取り組みやすかった問題だと思います。
資料
問題などはこちらから
I 水素吸蔵合金 圧平衡定数

まず,水素吸蔵合金が出てきて少し警戒するものの,吸蔵が始まる直前までは普通に気体の問題として解けばよい。とにかく序盤はリード文をサッと読んで全体像をつかみたい。
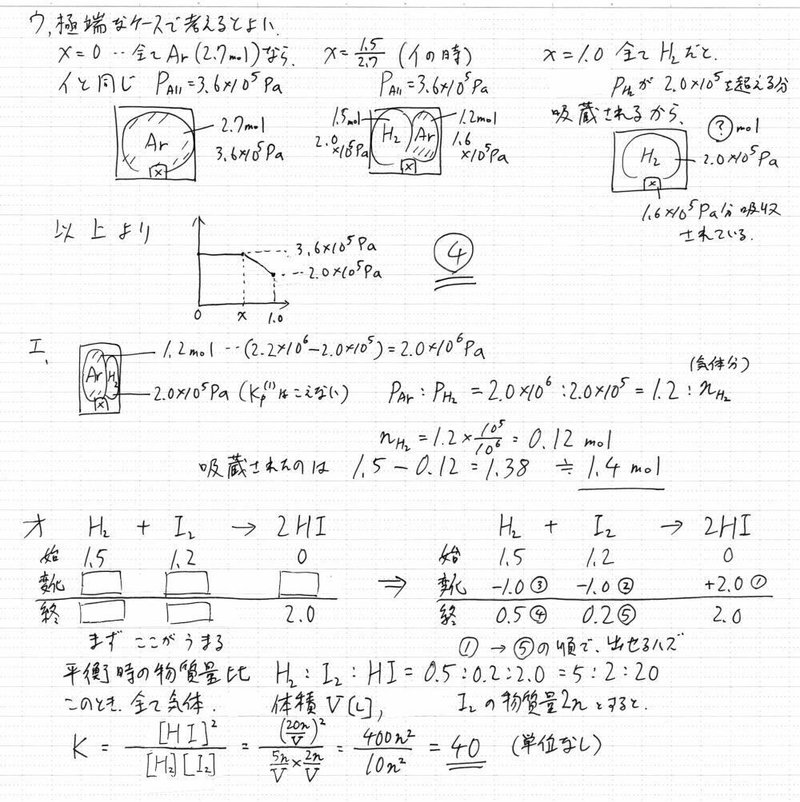
ウ でグラフ問題となるが,幸い選択なので詳しく考える必要はない。選択のグラフは「極端なケースを考えて」プロットするのが近道。水素0,水素のみ,のケースを考えると,「端っこ」が決まるのですぐにグラフを絞り込める。
エ では,吸蔵が始まるが,「平衡」になっている間は水素の分圧が固定なので,必然的に物質量がそのままのArの分圧も求まり,吸蔵されてしまった分の水素の物質量も求まる。
オ 以降は,「吸蔵の平衡」の前半に「ヨウ化水素の平衡」の話題も入ってきて考えることが増える。とはいえ,オの時点では普通に平衡定数を求めるだけ。

カ では,物質量が変化するのでは?という心配事項があるものの,式2を見ると,温度そのまま,圧力が変わってもルシャトリエの原理を考えたときに「圧力変化を和らげる方向の平衡移動」は起きないことがわかる。(右辺に行っても左辺にいっても分子数は変化しないので)というわけで,オの時点で求めている物質量費をそのまま使って分圧を求めればよい。ここでも吸蔵スタート時なので平衡が始まった時。すなわち水素の分圧はいっしょ。
キ では,水素が吸蔵されて減ってしまうので物質量が変化し,式2の平衡も動く。このためオの物質量は使えない。水素は平衡なので分圧はさっきと一緒。残りのヨウ素,ヨウ化水素の分圧を合計したものが全圧になる(※)
ここで,温度が変わらないからオの平衡定数は変わらないのでそのまま使える。一応濃度の平衡定数と圧平衡定数の関係をちょっと整理してから求めにいこう。二つの式を連立させつつ,ヨウ化水素だけ求めればいいので一次方程式に持って行けばおしまい。計算量が多いように見えるが,しっかり整理すればそれほど時間はかからない。
II アミノ酸 酵素 反応速度
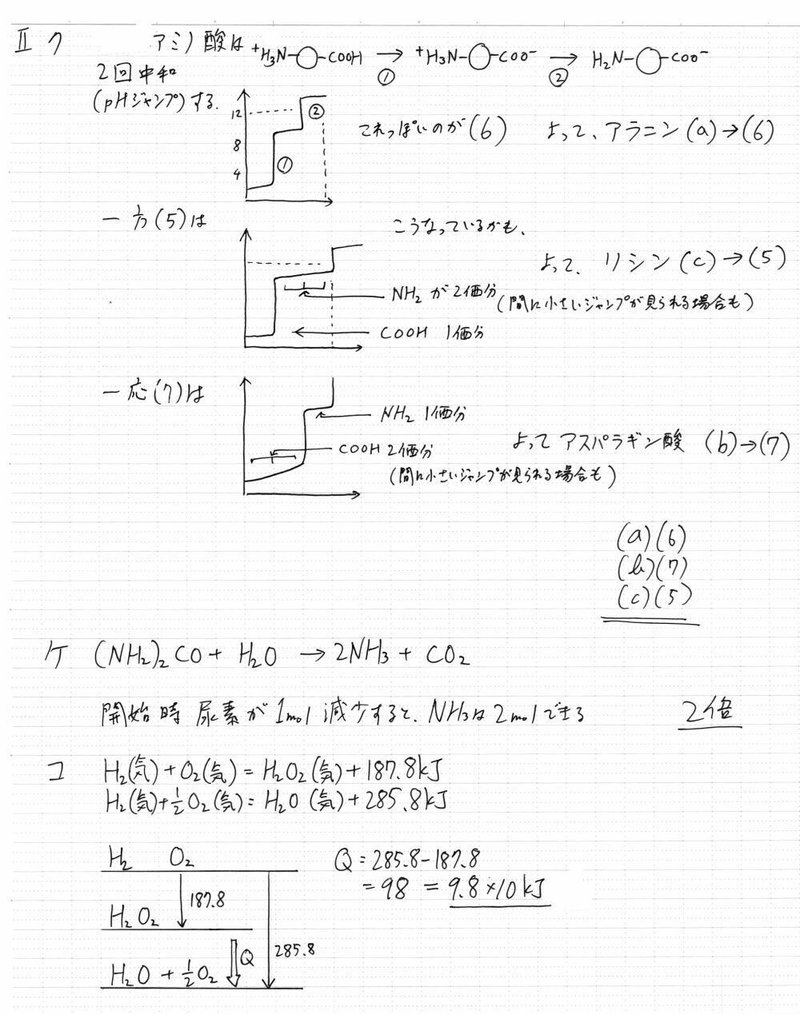
II では,同じ第2問でも話題がまた変わる。まずクの滴定曲線は,実際にアミノ酸の滴定曲線を問題演習などを含め何度か見かけていないと選びにくい。表記しているグラフが,滴定曲線の一部(?)のような形になっているのもなかなか意地悪ではある。基本的にアミノ酸は大きなpHジャンプを2回する。(カルボキシル基と,アミノ基)ただ,アスパラギン酸(COOHが2つある)やリシン(NH₂が2つある)では,その分,「その官能基に相当する分」の反応に用いる酸や塩基が多くなる。実際の実験や,もちろんほかの問題などでは,「2つのうち1つ分」のところで(すなわち半分のところで)小さなpHジャンプがみられる場合もある。ただ,このグラフだとそこは確認できない。
ケ の式は,あまりなじみなくてもすぐ作れる。速度も,問い方に少し癖があるものの,結局のところ物質量比のことである。
コ も,基本的には共通テストレベル。サービス問題と思っていい。一応,エネルギー図を書くと間違いが少ないとは思う。

サ は,あまりピンとこない人にとっては捨て問になったかもしれない。アレニウスの式自体は,結構難関クラスの二次試験では頻出なので練習しておきたいものである。やり方は色々ありそうだが,煩雑になりそうな数値を一度文字で置いてしまってから整理するとスムーズ。ここでのR(気体定数)はJ(ジュール)の方を使うのを忘れないように。(カタラーゼなしのEaの単位など,kJで表されていることからも,この式ではJを用いるということがわかる。)もちろん,kJに変換するのを忘れると大変。単位には気を付けよう。
シ は,直感で行ってもいいが,丁寧に考えるとこんな感じか。pH自体が対数関数だが,それを水素イオン濃度に戻すなら指数関数という話になる。よって速度自体もpHの指数関数というわけだ。
所感
というわけで,東大2021第2問。読む量はそれなりにあるが計算量としてはあまりない。比較的スムーズに取り組めたかもしれない。逆に言えば,細かいミスを生まないように,丁寧に整理して解けたかによって差がついた問題かもしれない。
