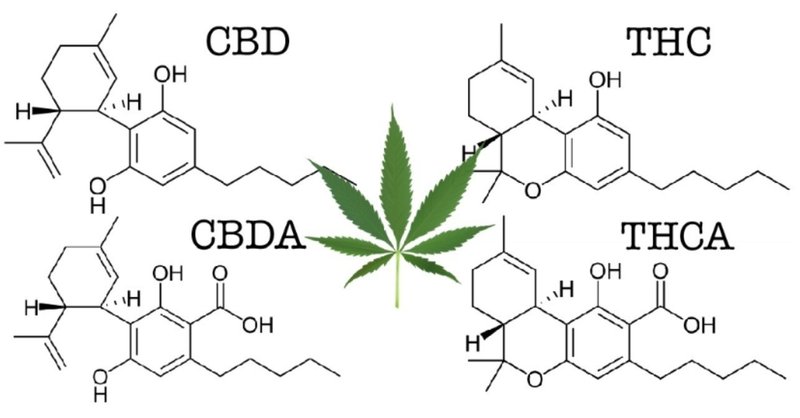
生の大麻(カンナビノイド酸)の健康効果
免責事項:この記事には、医療や医薬品に関する情報が含まれていますが、執筆者は医療の専門家ではなく、内容は医学的アドバイスを目的としているものではありません。執筆者は利用者がこの記事の情報を用いて行う一切の行為について、何らの責任を負うものではありません。Mechoulam博士の研究発表
「大麻研究の父」と呼ばれるイスラエルの有機化学者Raphael Mechoulam博士は、2019年9月23日、カリフォルニア州パサディナで開催された医療大麻カンファレンス(CannMed2019)の会場で、88歳にして新たに安定した化学合成バージョンのCBDA(カンナビジオール酸; cannabidiolic acid)やTHCA(テトラヒドロカンナビノール酸; tetrahydrocannabinolic acid)などのようなカンナビノイド酸(cannabinol acid)を創る手順を開発し、製薬会社にライセンス可能であると発表した。この研究はアメリカに本拠地を置く、2017年に設立されたMechoulam博士を中心とする研究チームのスタートアップ企業、EPMによって行われた。NBC Newsによると、今回の発見によって安定した一定の性質の合成カンナビノイド酸を創ることが可能になり、CBDAやTHCAなどの治療効果に関する研究の発展や製薬会社による乾癬、関節炎、不安症、炎症性腸疾患などへの創薬の可能性が期待されている。
カンナビノイド酸の特性と健康効果
生きている大麻植物の中では、CBDやTHCなどの植物性カンナビノイド(phytocannabinoid)は、CBDAやTHCAなどのような酸性カンナビノイド(acidic cannabinoid)とも呼ばれる、カルボキシ基(−COOHの構造を持ち、酸の性質を示す)を持つフェノールカルボン酸体として存在し、CBDやTHCなどの中性カンナビノイド(neutral cannabinoid; フェノール体、脱酸体)とはそれぞれ作用や性質が異なる。カンナビノイド酸は収穫後、熱や光、空気、時間の経過によって簡単に脱炭酸反応を起こし、二酸化炭素と中性カンナビノイドに分解する不安定な分子構造であるために、これまであまり研究されていなかったが、CBDAにはCBDの1,000倍強力な吐き気を軽減する効果がある[1]ことや、THCAには精神作用がほとんどなく、神経保護作用や抗がん作用などの可能性がある[2]ことなどがそれぞれ明らかにされており、向精神作用(ハイになる作用)がなく、加熱して吸入することでは得られない生の大麻の成分の健康効果に期待と注目が高まっている。
CBDA(カンナビジオール酸)
2017年12月に発表されたMechoulam博士らによる研究では、 CBDAと合成カンナビノイド酸であるカンナビジオール酸メチルエステル(HU‐580)は、[35S]‐GTPγS結合を刺激することにより、ヒトとラットの5‐HT1A受容体(セロトニン受容体)アゴニストの活性化を強化することがin vitroで示され、ラットの吐き気と不安症の徴候を抑制すること、HU-580はCBDAより効力が強く、吐き気と不安障害、5‐HT1A受容体活性化強化によって改善されるその他の障害の治療薬の可能性があることも明らかにされている[3]。この研究の中ではCBDAが乳がん細胞の(転移の一因となる)遊走を抑制する[4]ことやシクロオキシゲナーゼ-2(COX-2)ダウンレギュレーションを引き起こす[5]ことを示すエビデンスとして日本の研究者である竹田修三博士らの研究が引用されている。あまり知られていないが、日本の研究者たちは極めて制限された条件のもとで国際的に高く評価される大麻(アサ)の研究をしており、CBDAの治療効果に関する日本語で読める資料も公表されている。この資料では”Δ9-THCがCB受容体に作用し動脈硬化の進行を抑制することがマウスを用いた実験で確認された”ことが紹介されており、日本の研究者によって”CBDAはCOX-2選択的阻害作用を介して抗炎症作用を示すこと”や”CBDA はがん細胞 migration に抑制的に働く複数の因子を介して migration を抑制する可能性がある”ことなどが明らかにされた経緯やメカニズムなどについて詳細に解説されている[6]。
THCA(テトラヒドロカンナビノール酸)
THCの前駆体であり、新鮮な大麻植物(アサ)に含まれる精神活性のほとんどないTHCAの治療効果の可能性にはどんなものがあるだろうか?THCAは大麻の花穂や葉の腺状突起(トリコーム)で生合成され、蓄積される。詳しくいえば、THCAにはTHCA-A(Δ9-tetrahydrocannabinolic acid A; 2-carboxy-THC)とTHCA-B(Δ9-tetrahydrocannabinolic acid B; 4-carboxy-THC)の2つの異性体が存在する。このうち大麻は主にTHCA-Aを生合成する。THCAの精神活性はTHCの1/100程度[7]とも1/10,000程度[8]ともいわれており、脱炭酸によってTHCに変わりやすい不安定な性質のために計測が難しいようである[9]が、精神作用がほとんどないという点では概ね意見は一致している。一般にTHCAは生体内ではTHCに転換しないようであると考えられている[9]。THCAにはTHCのような精神作用がないため、治療用途の研究での注目が高まっている。THCAはオリーブオイル中(THCA-A 25°で10日後に78%)の方がエタノール中(33%のみ残留)より安定して存在する[11]。 最近の研究では、THCAは強力なPPARγ(ペルオキシソーム増殖剤活性化レセプターガンマ)アゴニストであり、神経保護作用の可能性、ハンチントン病その他の神経変性、神経炎症性障害への治療上の可能性などが示されており[12]、この発見はてんかん、腫瘍、抑うつの治療効果の主張を解明する可能性がある。またPPARγ刺激は、アストロサイトなどのような通常の細胞には毒性を及ぼさずにがん細胞を殺す可能性があることも報告されている[2]。
生の大麻ジュース
カリフォルニア州メンドシーノ郡の医師William L. Courtney氏は、カンナビノイド酸を豊富に含む新鮮な大麻の花や葉のジュースに治療効果があると主張しており、患者であり奥さんであるKristenさんはTHCA主体の大麻ジュースによってSLE(全身性エリテマトーデス)が劇的に回復したとして、この情報を拡める活動をしているが、彼らの主張は実証されておらず、誤解を招いているという意見もある。
未来への展望
今回のMechoulam博士の新しい発見はこのような逸話的報告にエビデンスをもたらすきっかけとなるだろうか?研究者たちの関心はカンナビノイドからカンナビノイド酸へと大きくシフトするかもしれない。知的財産と特許がかけられた化学合成の安定したTHC酸を創る技術が実用化されれば、日本でもハイにならずに一定の治療効果を得られる合法的なカンナビノイド系製剤として医療応用できる可能性は充分にある。しかし、天然のTHCAと違って長い目で見た場合にどんなリスクが潜んでいるのかはまだまだ未知であり、環境への負荷やコスト面での懸念なども気がかりである。大麻は最も古い栽培植物の一つであり、太古の昔から治療薬として利用されてきた長い歴史のある植物である。何事もはじめに現象ありき。メカニズムの解明はあとからついてくる。ヒトはエビデンスの不断の探求の果てに、大自然の神秘を改めて深く感じざるを得ないだろう。
参考文献
1. Rock EM, Parker LA. Effect of low doses of cannabidiolic acid and ondansetron on LiCl-induced conditioned gaping (a model of nausea-induced behaviour) in rats. Br J Pharmacol. 2013;169:685–692
[PMC free article] [PubMed] [Google Scholar]
2. Russo EB. Cannabis therapeutics and the future of neurology. Front Integr Neurosci. 2018;12:51. doi: 10.3389/fnint.2018.00051.
[PMC free article] [PubMed] [CrossRef] [Google Scholar]
3. Pertwee, R. G., Rock, E. M., Guenther, K., Limebeer, C. L., Stevenson, L. A., Haj, C., … Mechoulam, R. (2018). Cannabidiolic acid methyl ester, a stable synthetic analogue of cannabidiolic acid, can produce 5-HT1A receptor-mediated suppression of nausea and anxiety in rats. British journal of pharmacology, 175(1), 100–112. doi:10.1111/bph.
[PMC free article] [PubMed] [CrossRef]
4. Takeda S, Himeno T, Kakizoe K, Okazaki H, Okada T, Watanabe K et al (2017). Cannadidiolic acid‐mediated selective down‐regulation of c‐fos in highly agressive breast cancer MDA‐MB‐231 cells: possible involvement of its down‐regulation in the abrogation of aggressiveness. J Nat Med 71: 286–291. [PubMed] [Google Scholar]
5. Takeda S, Okazaki H, Ikeda E, Abe S, Yoshioka Y, Watanabe K et al (2014). Down‐regulation of cyclooxygenase‐2 (COX‐2) by cannabidiolic acid in human breast cancer cells. J Toxicol Sci 39: 711–716. [PubMed] [Google Scholar]
6. 竹田修三,「繊維型大麻草主成分カンナビジオールを基盤としたメディシナルケミストリー」, 日本薬学会 薬学雑誌 2013年 133巻 10号 p.1093-1101
Takeda, S. (2013): Medicinal chemistry and pharmacology focused on cannabidiol, a major component of the fiber-type cannabis. Yakugaku Zasshi, 133, 1093-1101. [ J-STAGE ] [ PubMed ]
7. 田浦太志, 正山祥生, 森元聡, 「大麻幻覚成分THCAの生合成研究」生物物理 2005 年 45 巻 4 号 p. 178-184 [ J-STAGE ]
8. 山本郁男, 「大麻文化科学考1−7) (その 8) 第8章 大麻の成分」北陸大学 紀要 第21号 (1997) pp .1〜20 [PDF]
9. McPartland JM, MacDonald C, Young M, et al. Affinity and efficacy studies of tetrahydrocannabinolic acid A at cannabinoid receptor types one and two. Cannabis Cannabinoid Res. 2017;2:87–95 [PMC free article] [PubMed] [Google Scholar]
10. Jung J., Meyer M. R., Maurer H. H., Neususs C., Weinmann W., Auwarter V. (2009). Studies on the metabolism of the Delta9-tetrahydrocannabinol precursor Delta9-tetrahydrocannabinolic acid A (Delta9-THCA-A) in rat using LC-MS/MS, LC-QTOF MS and GC-MS techniques. J. Mass Spectrom. 44 1423–1433. 10.1002/jms.1624 [PubMed] [CrossRef] [Google Scholar]
11. Citti C., Ciccarella G., Braghiroli D., Parenti C., Vandelli M. A., Cannazza G. (2016). Medicinal Cannabis: principal cannabinoids concentration and their stability evaluated by a high performance liquid chromatography coupled to diode array and quadrupole time of flight mass spectrometry method. J. Pharm. Biomed. Anal. 128, 201–209. 10.1016/j.jpba.2016.05.033 [PubMed] [CrossRef] [Google Scholar]
12. Nadal X., Del Río C., Casano S., Palomares B., Ferreiro-Vera C., Navarrete C., et al. . (2017). Tetrahydrocannabinolic acid is a potent PPARγ agonist with neuroprotective activity. Br. J. Pharmacol. 174, 4263–4276. 10.1111/bph.14019 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
この記事が気に入ったらサポートをしてみませんか?
