間違いだらけの不妊治療 体外受精編①
インターネットをみてみると、体外受精に関して本当にたくさんの間違った情報が流れています。また一部の企業は自分たちの製品を使ってもらうため、一部のクリニックは自分たちの病院へ患者さんを呼び込むために、エビデンス(根拠)の不確定な検査や治療をあたかも完成された治療のように書いていることもあります。
ここでは、きちんとしたエビデンスのある、間違いのない情報を実際に患者さんから聞かれた質問に沿って、説明していきたいと思います。
Q. 日本が世界で最も体外受精で妊娠率が低い国と言われていますが、本当ですか?
世界的な報告では、これまで日本は世界で最も多く体外受精を行っていて(文献1)、2018年に45~46万周期の治療周期を行っています(文献2)。ただ中国が2016年の中国全土の治療周期を約90万周期と報告し(文献3)、日本は世界で2番目に治療周期の多い国と予想されます。
一方で、日本は治療周期ごとの妊娠率が低い国として報告され、一部のマスコミなどが取り上げました(文献4)。これには、世界のデータ集計における統計の問題があります。世界的には妊娠率は、採卵周期ごとの妊娠率が基本的に計算されていました。つまり、採卵した周期に新鮮胚移植を行ったときの妊娠率で計算されていました。
日本の凍結技術は世界トップクラス
新鮮胚移植というのはもともと卵巣刺激をした周期で、胚移植をします。日本では、凍結技術が世界と比較してトップクラスで、そのため受精卵を凍結しても妊娠率が低下することがほとんどありません。そのため、日本では新鮮胚移植を行うと、凍結融解胚移植と比較すると少し胚移植ごとの妊娠率が低くなります。
日本では卵巣過剰刺激症候群を避けるため、強い卵巣刺激を行わない場合が多い
また連続で注射を行う高卵巣刺激法を行うと、卵巣過剰刺激症候群という卵巣が腫大し腹水がお腹に貯まり重症になると入院して治療が必要な合併症が起こる可能性があります。妊娠した場合には、その卵巣過剰刺激症候群はさらにひどくなり、母体の命にかかわる問題になるときには、せっかく妊娠したのに中絶を余儀なくされることがあります。そんな合併症は受精卵をすべて凍結(全胚凍結)して卵巣の状態が落ち着いてから胚移植を行えば、問題になることはほぼありません。
そのため日本では妊娠率と安全性を考え、全胚凍結をすることも多いです。2019年の日本の体外受精のデータでは、体外受精で出産した胎児の約9割が凍結胚で妊娠しています(文献5)。
凍結融解胚移植は周期ごとの妊娠とみなされない
世界的な統計では、新鮮胚移植での妊娠率が計上されているため、全胚凍結を行うと、その周期は妊娠していないという扱いにされ、凍結融解胚移植を多く行っている日本は見かけ上低い妊娠率となりました。
受精卵一個当たりの出産率で考えると日本の体外受精の成績は高い!
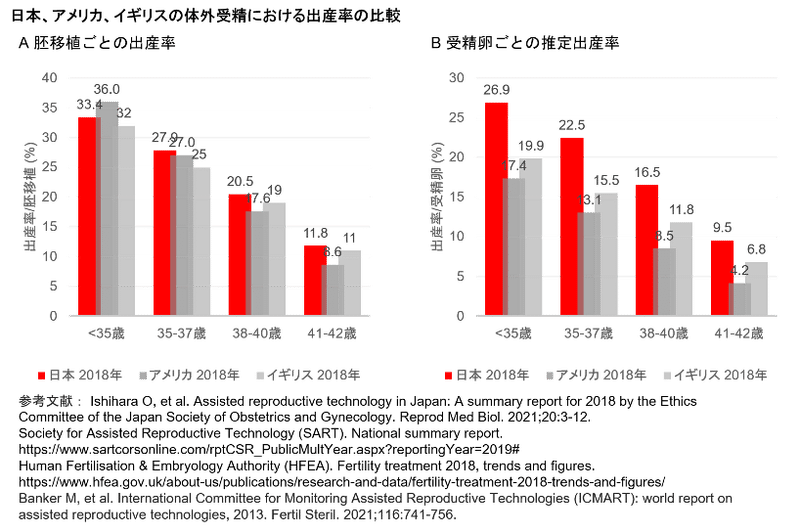
現在、アメリカやイギリスは体外受精のほとんどのデータをインターネットから確認することができるようになっています(文献6,7)。これらの成績から2018年の患者自身の卵子で体外受精を行った胚移植ごとの生産率を抽出し、2018年の日本の生産率の報告(文献2)と比較しました(図)(文献8)。どの年齢も3カ国で大きな差がないようにみえますが、アメリカやイギリスは2個以上の複数個で胚移植を行うことが多いのに対し、日本は1個での胚移植を中心で行っているため、受精卵ごとの推定される出産率を比較すると、日本は明らかに1個の受精卵当たりの出産率が、アメリカやイギリスより高いことがわかります(図)。1個の胚移植と2個以上の胚移植の比較については、この後の別の質問で答えていますので、ぜひ読んでみてください。
今後、世界のデータ集計や解析方法を変更する予定もあるようです。その時には、日本の体外受精のレベルの高さを理解してもらえるでしょう!
Q. 卵巣刺激をすると、たくさんの卵子がなくなるので、卵巣の中の卵子の数が低下するのが早まって、閉経も早まりますか?
通常排卵するときに卵胞は1個なのに対し、卵巣刺激を行うといくつもの卵胞ができるので、何か月分もの卵子が失われるのではないか? という情報がインターネットでも流れています。もとになったのはおそらくマウスの研究で何度も高卵巣刺激を行うと卵巣の老化が早まるという報告です(文献9)。
卵巣刺激は「消えていく予定だった卵子」を育てる技術
以前に説明しましたが、もともと1回の月経周期で、1個卵子が排卵するときに約30個の卵子が消えていきます。卵巣刺激はその消えていく予定だった卵子を、注射などで育ててあげる方法です。理論上は30個以上の卵胞を育てることがあれば、卵巣予備能の低下が早まりますが、そんなにたくさんの卵子数は、いくら卵巣刺激を強めても、普通の方ではできることはほとんどありません。
また最近の研究で卵巣刺激を繰り返したマウスの卵巣は老化が進まないこともわかっています(文献10)。
卵巣予備能が低い方が高卵巣刺激法を行えば、卵巣予備能の低下が早まる可能性はあるかもしれませんが、一般的に適度で卵巣予備能に見合った卵巣刺激であれば、卵巣予備能の低下が早まることはありません。
Q. 卵巣刺激やホルモン補充を行う不妊治療は、がん(悪性腫瘍)が発生しやすくなるのは本当ですか?
卵巣刺激を行うと通常よりも非常に高いエストロゲン状態になることがあり、エストロゲンに感受性のある悪性腫瘍(がん)の発生率を上げる可能性が気になる方もいるかと思います。
がんの発症リスクをあげることないと報告されています
いくつもの臨床研究をまとめて解析した報告(メタ解析)によると、エストロゲンと関係する乳がん、卵巣がん、子宮体がんの発症リスクを上げることはなく、子宮頸がんに関してはむしろ発症リスクが下がることがわかっています(文献11)。そのため基本的には心配する必要はありません。
すでに乳がんがある人の不妊治療は?
すでに悪性腫瘍がみつかっている方での不妊治療はどうでしょうか? 昔と違って乳がんなどの若くして発症する悪性腫瘍の治療による治癒率が向上したこともあり、乳がんがわかってから不妊治療を行ったり、抗がん剤で卵巣機能が下がる前に卵子凍結を行ったりすることも多くなりました。
その場合でも、レトロゾール(アロマターゼ阻害薬)という薬は乳がんの治療薬のひとつであり、かつ卵巣刺激としても使えるホルモン製剤があります。レトロゾールはエストロゲンをおさえる薬で、乳がんの治療薬といっても副作用はほとんどありません。内服をしながら注射をして卵巣刺激を行うと、エストロゲン値は低く保ったまま複数の卵子を採取することができます(文献12)。そのため、エストロゲン感受性のある悪性腫瘍をもつ女性でも、エストロゲン値をあまり高くせずに、比較的安全に卵巣刺激を行うことができるようになりました。
Q. 卵子の老化にかかわるミトコンドリアは、サプリメントで活性化できるのは本当ですか?
そもそも、ミトコンドリアってなんでしょう?
ミトコンドリアとは、細胞が増えるときなどにエネルギー源となるATP(アデノシン三リン酸)を主に作る細胞内の小さい器官です。卵子の中にもたくさん存在し、その数が卵子の老化と比例することがわかっています。そのためミトコンドリアを増やせば、卵子の老化を改善できます。
今は原則禁止されている方法ですが、高齢女性の卵子の中に、若い女性のミトコンドリアを多く含む卵子の細胞の一部を注入すると、卵子の老化が改善し、体外受精を行えばその妊娠成績が上がります(卵細胞質置換)。(文献[恵黒1] 13)ただこの治療は、卵子を提供した女性の遺伝子も一部子どもに引き継がれることもわかっています。したがって、2人の女性の遺伝子が混ざってしまうこともあり、現在は行うことはできません。
サプリメントでミトコンドリアを活性化させることができることは考えにくい…
そのミトコンドリアを活性化させるために、インターネット上ではさまざまなサプリメントが高額で売られています。個人的な意見を言えば、「卵子のミトコンドリアを活性化させる!」とうたっているサプリメントはどれも非常に怪しいです。サプリメントを内服して直接卵子の中までたどりつき、ミトコンドリアを活性化させることは非常に考えにくいです。
卵子の老化を抑えるサプリメントはあるの?
ただ卵子の老化を抑える可能性のあるサプリメントはいくつかあります。主にはアンチエイジングとして抗酸化作用のある、コエンザイムQ10やレスベラトロールなどです。コエンザイムQ10はミトコンドリアを構成するのに必要な成分で、レスベラトロールは赤ワインなどに多く含まれるポリフェノールの一種で、その天然ポリフェノールを凝縮したようなものです。どちらもミトコンドリアの合成を促進する効果があり、卵巣機能を改善する効果も多数の研究で報告されています(文献14,15)。
アンチエイジング効果のあるサプリメントは着床を阻害する可能性がある
アンチエイジング効果のあるサプリメントは、動物研究が多数行われてきたのですが、今までヒトでの妊娠成績を改善する報告が非常に少なかったのが現状です。一度の妊娠でたくさん出産する他の動物種と違って、ヒトの妊娠では卵巣だけでなく、受精卵を子宮の中に着床する段階が非常に繊細で重要です。
不妊治療を行っているときにむやみにアンチエイジング効果のあるサプリメントを持続的に内服していると、着床を阻害してしまっている可能性があります(文献16)。内服する場合には、医師と相談して内服方法に注意して使うことをお勧めします。
参考文献
1. Chambers GM, et al. International Committee for Monitoring Assisted Reproductive Technologies world report: assisted reproductive technology, 2014. Hum Reprod. 2021;36(11):2921-34.
2. Ishihara O, et al. Assisted reproductive technology in Japan: A summary report for 2018 by the Ethics Committee of the Japan Society of Obstetrics and Gynecology. Reprod Med Biol. 2021;20(1):3-12.
3. Bai F, et al. Assisted reproductive technology service availability, efficacy and safety in mainland China: 2016. Hum Reprod. 2020;35(2):446-52.
4. Adamson GD, et al. International Committee for Monitoring Assisted Reproductive Technology: world report on assisted reproductive technology, 2011. Fertil Steril. 2018;110(6):1067-80.
5. Katagiri Y, et al. Assisted reproductive technology in Japan: A summary report for 2019 by the Ethics Committee of the Japan Society of Obstetrics and Gynecology. Reprod Med Biol. 2022;21(1):e12434.
6. Society for Assisted Reproductive Technology (SART). National summary report.
(https://www.sartcorsonline.com/rptCSR_PublicMultYear.aspx?reportingYear=2019#)
7. Human Fertilisation & Embryology Authority (HFEA). Fertility treatment 2018, trends and figures.
8. 黒田 恵司. 【排卵誘発のすべてII ART編】卵巣刺激法の国際比較とその成績. 産婦人科の実際. 2021;70(13):1579-85.
9. Chao HT, et al. Repeated ovarian stimulations induce oxidative damage and mitochondrial DNA mutations in mouse ovaries. Ann N Y Acad Sci. 2005;1042:148-56.
10. Whang J, et al. Effects of Repeated Ovarian Stimulation on Ovarian Function and Aging in Mice. Dev Reprod. 2021;25(4):213-23.
11. Barcroft JF, et al. Fertility treatment and cancers-the eternal conundrum: a systematic review and meta-analysis. Hum Reprod. 2021;36(4):1093-107.
12. Oktay K, et al. Fertility preservation in breast cancer patients: a prospective controlled comparison of ovarian stimulation with tamoxifen and letrozole for embryo cryopreservation. J Clin Oncol. 2005;23(19):4347-53.
13. Barritt J, et al. Cytoplasmic transfer in assisted reproduction. Hum Reprod Update. 2001;7(4):428-35.
14. Tatone C, et al. Sirtuins in gamete biology and reproductive physiology: emerging roles and therapeutic potential in female and male infertility. Hum Reprod Update. 2018;24(3):267-89.
15. Xu Y, et al. Pretreatment with coenzyme Q10 improves ovarian response and embryo quality in low-prognosis young women with decreased ovarian reserve: a randomized controlled trial. Reprod Biol Endocrinol. 2018;16(1):29.
16. Kuroda K, et al. The actions of resveratrol in decidualizing endometrium: acceleration or inhibition?. Biol Reprod. 2020;103:1152-6.
この記事が気に入ったらサポートをしてみませんか?
