
私の最新研究をご紹介
私がこの5年間ほど費やして進めてきた研究の成果を、米国の科学誌Journal of Clinical Investigationで発表させてもらいました。
今回はその内容について、一般の方にもわかるように、噛み砕いた形で、少しご紹介させてもらいます。
放射線治療はがん治療の根幹をなすものの一つで、多くのがん種に対して行われています。しかし、いくつかのがん種では放射線治療が効きにくく、せっかく治療を行っても、すぐに再発を起こしてしまうことがあって、そのメカニズムの解明が待たれています。今回、私は神経膠芽腫という脳にできるがん(悪性脳腫瘍)の、放射線治療が効きにくいメカニズムを調べました。
神経膠芽腫は大変に悪性度が高く、手術・放射線・化学療法などを行って治療しても、ほぼ全例が再発してしまい、5年生存率はわずかに5%ほどと、大変に厳しい脳腫瘍です。
この神経膠芽腫が放射線でも倒されない理由の一つとしては、脳腫瘍内に通常の腫瘍細胞よりも、外からの攻撃に強い、「がん幹細胞」という特殊ながん細胞があって、それが再発に重要な働きをしていることがわかってきていました。
しかし、その神経膠芽腫にあるがん幹細胞(グリオーマ幹細胞:以下GSC)はどのようにして、放射線治療の攻撃から身を守っているのか、その詳細なメカニズムはまだわかっていませんでした。今回はそれを調べて、GSCを倒す方法を見つけたという研究になります。
我々は、まず神経膠芽腫の患者から採取したGSCと、マウスに作った神経膠芽腫から取ってきたGSCを使って、それに繰り返し放射線照射をあてていって、GSCがどう変化するのかを詳細に調べました。
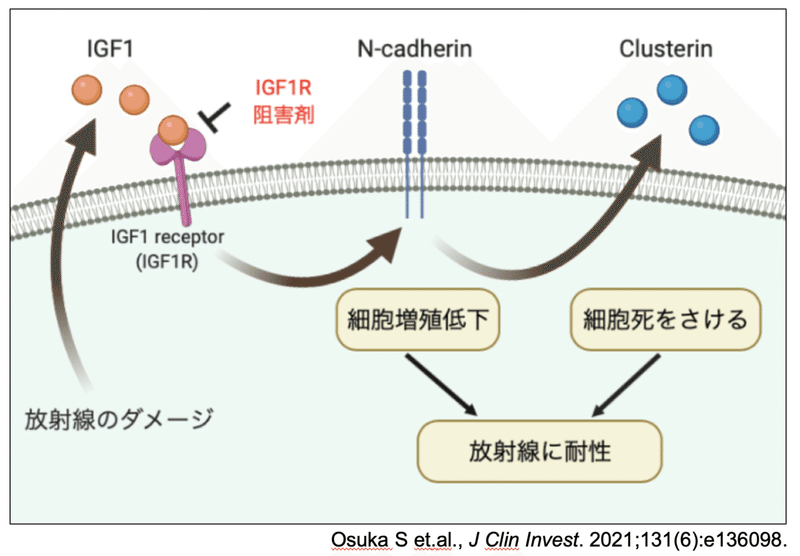
その結果、GSCは放射線照射を繰り返し受けるにつれて、N-cadherinという細胞表面にある分子を増やして、それに伴って、細胞が増殖する速度を遅くしていることを見つけました。
放射線治療は激しく増殖している細胞の方が、ゆっくりと増殖している細胞よりも効きやすい特徴があります。GSCは放射線治療を受けて危険だと感じると、このN-cadherinを介したシグナルで、一旦増殖をゆっくりにして、放射線治療のダメージを回避しているという、大変に巧妙な変化をしていることがわかりました。
また、N-cadherinの増加はClusterinという、死ぬのを防ぐシグナルも活性化していることがわかって、こちらも放射線による死をまぬがれる術として利用していることがわかりました。
最後に、このN-cadherinの増加はIGF1というものによって引き起こされていて、そのシグナルを阻害する薬剤(IGF1R阻害剤)を使うと、このメカニズムを止めて、放射線の効果を高められることを発見しました。
この発見は、細胞・マウスモデルを使った基礎研究段階の発見であるため、実際の患者さんの治療に利用するには、まださらなる研究が必要です。我々はこの発見に基づいて、神経膠芽腫患者さんを対象とした臨床研究を行うことを計画中です。
神経膠芽腫は大変に厳しい脳腫瘍であるため、何とかこの結果を将来の有効な治療に結びつけたいと思っていて、今後も研究を継続していこうと思っています。
最後に、この研究は私のボスであるアラバマ大学バーミンガム校のErwin Van Meir教授と、多くの共同研究者の支えで行えたものです。素晴らしいサポートに心から感謝をしたいと思います。
また、この論文は5年に及ぶ年月の中で、多くの苦難を受けつつ、それを乗り越えて、何とか結実することができたものです。途中には新型コロナの感染拡大によって、長期に研究室が閉鎖となってしまったりと、本当に心が折れそうになった時がありました。その中でも、常に私のことを励まし支えてくれた妻と子供達に、本当に心から感謝をして、ご紹介を終わりたいと思います。ありがとうございました。
もし、よろしければサポートをお願いいたします!いただいたサポートはがん情報発信の強化のために利用させてもらいます。
