タンパク質分析の革命 ~不可能を可能にした分析技術の発明と開発~
2002年のノーベル化学賞は「生体高分子の分析手法と構造解析の開発」に贈られました。
受賞したのは日本の田中耕一氏、アメリカのジョン・ベネット・フェン 博士、スイスのクルト・ビュートリッヒ博士の3名でした。
分野は分析化学ですね。
そして、関連の強い1991年のノーベル化学賞も合わせて解説します(こちらは後半でご紹介します)。

田中耕一(Wikipedia)、現在は株式会社島津製作所シニアフェロー、田中耕一記念質量分析研究所所長、田中最先端研究所所長などを務めています。

ジョン・ベネット・フェン (Wikipedia)、イェール大学の化学工学部在籍中に受賞理由となった研究成果を挙げる。2010年に亡くなられました(93歳)。

クルト・ビュートリッヒ (Wikipedia)、1998年に京都賞を受賞。81歳となった現在も研究を続けています。
この年、日本人が3年連続で化学賞を受賞し、しかも同年の物理学賞に小柴昌俊・東京大学名誉教授が受賞したこともあり、大きな話題になりました。
〇学部卒で博士を持たない会社員の田中さん(大学の専攻は化学系ではなかった)
〇素粒子物理の分野で数々の成果を挙げ、ウルフ賞やフンボルト賞のような権威ある賞も受賞し、ノーベル賞を期待されていた小柴さん(ウルフ賞受賞者の約半数はノーベル賞を受賞している。)
対照的な経歴の二人が受賞したので、強く印象に残っている方も多いと思います。
田中さんの経歴が大きくクローズアップされ、開発した技術とエピソードがメディアで何度も取り上げられました。
一方で、
〇この年のノーベル化学賞の全体像
〇他の受賞者はどんな研究を行ったのか
という部分には殆ど触れられませんでした。
他に受賞者が居た事を知らない方も多いんじゃないでしょうか。
では、受賞理由となった「生体高分子の分析手法と構造解析の開発」とはどんな研究で、どこが素晴らしいのか?
一つずつ見て行きましょう。
分析化学と質量分析
物質の分析には様々な手法があります。
分析化学は目立たない分野ですが、物質や材料の性質を深く理解し、客観的な計測手法の研究・開発や、データの信頼性向上・分析に関する課題解決を行う極めて重要な分野です。
分析化学が学問を発展させ、社会を豊かにしてきたと言っても過言ではありません。
分析化学の中でも高い精度を要求されるのが「質量分析」です。
物質の質量を測定することは重要です。
例えば、目的の物質が合成されているか、質量分析によって確かめます。
化学式から計算した理論値と実測値が同じであれば、目的の物質が合成されたと判断します(例外もあります)。
また、どんな物質が含まれているのか、質量分析で確認することもあります。
他には、含まれている元素の測定ですね。質量数によって測定試料に含まれている元素を調べます。それによって、不純物となる元素がどのくらい含まれているのかを知ることが出来ます(必要元素を調べることもあります)。
例えば、水質の分析などに使われています。
ちなみに、質量分析は英語でMass Spectrometryのため、MSと略して呼ばれます。読み方はエム・エスなんですが、日本人はマスと呼ぶ人が多いです。
質量分析の原理と問題点
質量分析はどのような方法で行われるのでしょうか?
カギとなるのはイオン化です。
測定したい物質を溶媒に溶かし、装置の試料導入部に注入します。
試料溶液は適切な方法でイオン化されます。
イオン化された試料は質量によって分けられ、検出部に送られます(イオン化前にクロマトグラフィーによって試料を分離するケースも多いです。)。
検出された試料から、下図のようなスペクトル情報が得られます(一例です)。
*「スペクトル(英語: spectrum[1])とは、複雑な情報や信号をその成分に分解し、成分ごとの大小に従って配列したもののこと」です(Wikipediaより)
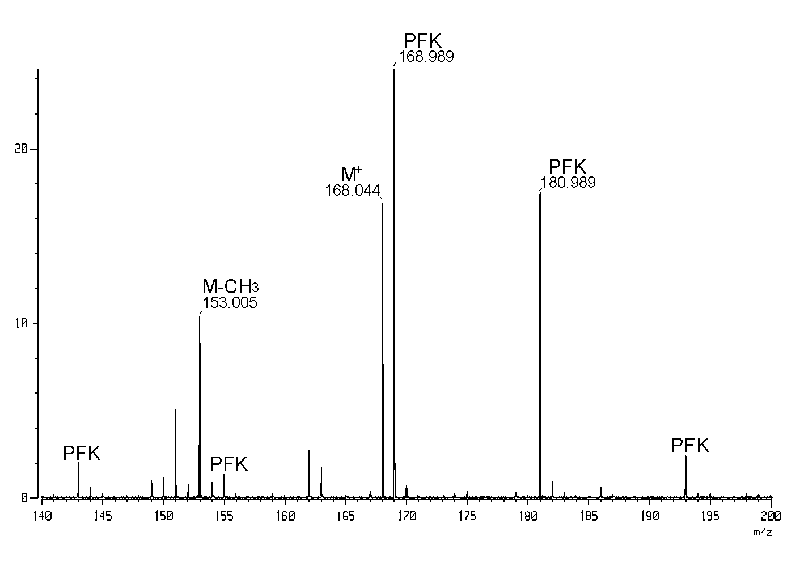
バニリン酸の精密質量測定(旭川医科大学HPより引用:http://cent-scorpio.asahikawa-med.ac.jp/akutsu/mass/milli_mass/)
この情報から、質量を知ることが出来るんです。
試料をイオン化するのは、電子衝撃法(Electron Ionization=EI)という方法です。気化させた試料に電子をぶつけ、陽イオンにします。
EI法と呼ばれ、今も低分子化合物の質量分析に用いられています。
しかし、EI法には欠点がありました。
一つは、揮発し難い物質・熱に弱い物質は測定できないこと。
もう一つは、電子をぶつけたときに試料がバラバラになり、正確な質量を測定できないという点です。特に、高分子の測定では致命的となります。
この問題を解決したのが、田中耕一さんの開発したマトリックス支援レーザー脱離イオン化法と、フェン博士の開発したエレクトロスプレーイオン化法でした。
この二つの手法はソフトイオン化法とも呼ばれます。
マトリックス支援レーザー脱離イオン化法
英語名(Matrix-Assisted Laser Desorption Ionization)を略して、 MALDI(マルディ、モールディ)と呼ばれます。
その名の通り、マトリックスと呼ばれるイオン化されやすい液体と試料を混ぜ、レーザー光を照射します。
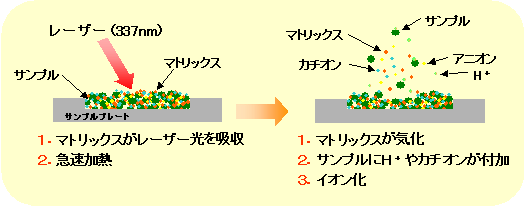
旭化成HPより(https://www.asahi-kasei.co.jp/akasc/equipment/yuki_tofms.htm)
すると、液体の表面が急速に加熱され、試料と共に気化します。
このとき、マトリックスの液体はエネルギーの高い状態(励起状態)になります。エネルギーが高く、他の物質と反応し易い状態のため、測定試料をイオン化します(プロトンの授受が起きる)。
このようにして、MALDIは試料をイオン化します。
試料に直接レーザー光をあてないので、試料は分解されることなく気化されます。これがMALDIの最大の特徴です。
そして、MALDIによってイオン化した試料は、飛行時間型質量分析(TOF/MS)によって分析されます。
その名の通り、イオン化された試料が導入部から検出器に届くまでの時間で物質を分類します。
重いイオン(イオン化した高分子など)ほど遅くなるんです。
このようにして、高分子の質量を分析します。
エレクトロスプレーイオン化法
こちらは、MALDIとは全く違う方法で高分子をイオン化します。
下図のように、測定試料を溶かした液体に高電圧をかけ、ノズル(or 細いチューブ)から押し出します。ノズル先端から出てきた溶液は帯電しているため、図のように電荷が液体の表面に移動します。さらに、帯電した分子同士の静電反発によって液滴は無数の粒になります(この分裂を何度も繰り返してより細かい粒になっていきます)。要するに、とても細かい霧になるんです。肉眼では見えないほど細かい液滴になると、溶媒は簡単に蒸発します。つまり、試料だけになるんです。帯電した試料が検出器まで運ばれます。
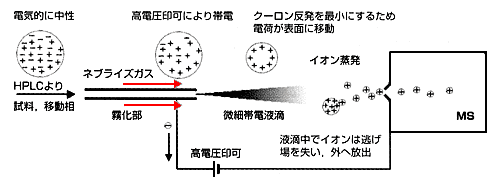
エレクトロスプレーイオン化法の模式図(島津製作所HP:https://www.an.shimadzu.co.jp/hplc/support/lib/lctalk/47/47intro.htm)
これがエレクトロスプレーイオン化法(ESI)です。
試料に強い衝撃や熱を与えることが無い上、大気圧下でイオン化できるため、MALDIよりもソフトな方法です。
ちなみに、エレクトロスプレー法は以前から存在した技術で、フェン博士はそれを質量分析に応用しました。
と言っても、質量分析を行う装置とエレクトロスプレーを組み合わせるのは容易ではなく、送液方法や電圧の印可など、様々な工夫や技術開発を行う必要がありました。
数多くのハードルを乗り越えて実現した分析方法なんです。
MALDIがESIよりも優れているのは、試料の純度が低くても測定出来ることと、ごく微量の試料でも測定可能なことです。
2つのソフトなイオン化法によって、タンパク質などの高分子の質量分析が可能となりました。
では、クルト・ビュートリッヒ博士は何を行ったのでしょうか?
この人の成果は質量分析ではないんです。
核磁気共鳴分光法(NMR法)という、分子の構造を調べる分析方法を使い、タンパク質の構造解析を行いました。
NMRとは?
NMR(エヌ・エム・アール)とは簡単に言うと、原子に磁場をかけて、原子一つ一つの状態を調べる手法です。
それによって、測定している物質がどんな原子で構成されているのか、原子同士がどのように繋がっているかが分かる画期的な分析技術です。
NMRの測定には、感度が高く測定し易い水素をターゲットにすることが多いです。ほとんどの物質には水素が付いているため、水素の状態を磁場をかけて調べれば、物質の大まかな構成が分かるんです。
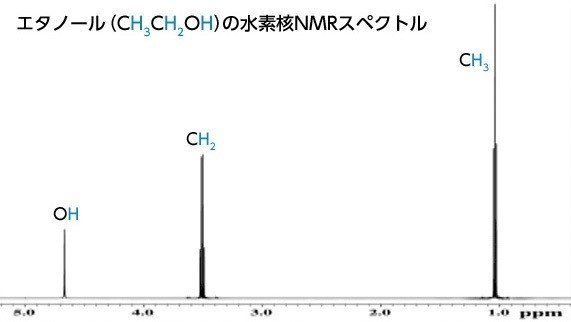
エタノールの水素核NMRスペクトル(日本電子HP : https://www.jeol.co.jp/products/nmr/basics.html)
図はエタノールを測定したシンプルな例ですが、もっと複雑な分子を分析することも可能です。
多次元NMRとタンパク質の分析
まず、1991年のノーベル化学賞について触れる必要があります。
1991年のノーベル化学賞を受賞したのはリヒャルト・エルンスト(スイス)。受賞理由は「高分解能NMRの開発への貢献 」です。
単独受賞でした。

リヒャルト・エルンスト(Wikipedia)
リヒャルト・エルンスト博士は、スイス連邦工科大学で核磁気共鳴の研究をし、より精度の高い多次元NMR法を開発します。
この技術開発によって実現したのが核磁気共鳴画像法 (MRI) です。
皆さんもご存じの、医療でよく使われる画像診断方法です。
多次元NMRを大雑把に表現すると、複数の指標(スペクトル)を使って物質の状態を分析する手法です。
さきほどご紹介したエタノールのNMRスペクトル図は多次元ではなく、通常(1次元)のNMRによるものです。
多次元だと、例えば以下のようになります。
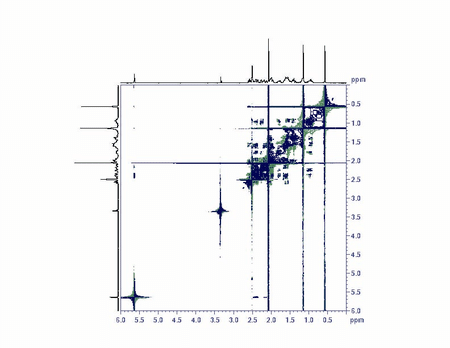
2次元NMRのスペクトル図(Wikipedia)
スペクトルが縦と横にあり、その交点(図の対角線上に交点が現れています)を読み取ります。エタノールのような単純な物質は通常(1次元)のNMRで十分なのですが、物質が複雑になると大量のスペクトルが検出され、しかもスペクトルが重なって解析困難となります。
多次元NMRなら、上のスペクトル図のように、2つの指標で得られたスペクトルの交点を読み取ることで、1次元では分からなった情報を知ることが出来ます。
*ここで説明しているのは2次元NMRです。3次元以上のNMRになると、また違ったスペクトル図になります。
そして、この研究を共に行っていたのがクルト・ビュートリッヒ博士でした。
多次元NMRの開発に貢献し、それを複雑なタンパク質分子の分析に応用しました。
ノーベル賞の対象となったのは、タンパク質を構成する分子の位置情報を決める原理を明らかにしたことです。
これによって、タンパク質の立体構造が計算可能となりました。
NMRの良いところは、タンパク質を乾燥させること無く、生きた細胞に近い状態で分析できることです。
ちなみに、多次元NMRを着想したのはベルギーの化学者、ジャン・ジェーネルでした。それを実現したのがリヒャルト・エルンストです。
まとめ
3人の功績により、複雑で大きなタンパク質分子を破壊することなく分析できるようになりました。
タンパク質を詳細に分析できるようになったことで、私たちの身体や生き物の仕組み・構造をより深く理解できるようになりました。
細胞やDNAなど、私たちの身体のほとんどがタンパク質で出来ています。赤血球も、その中に含まれるヘモグロビンもタンパク質です。
タンパク質の質量と立体構造を決定できるようになれば、タンパク質の機能を知ることが出来ます。
それによって、新薬の開発は大きく前進しました。
癌の診断や食品分析にも応用されています。
受賞理由となった「生体高分子の分析手法と構造解析の開発」の素晴らしさ、お分かり頂けたでしょうか。
分析技術は今も進化を続けています。
これからも、分析化学は社会を影から支えてくれることでしょう。
読んでいただけるだけでも嬉しいです。もしご支援頂いた場合は、研究費に使わせて頂きます。
