
【話題の最新論文解説】歯周病菌が認知症の原因ってホント!?③
前回の記事
【話題の最新論文解説】歯周病菌が認知症の原因ってホント!?②
の続きです。
"Receptor for advanced glycation end products up‐regulation in cerebral endothelial cells mediates cerebrovascular‐related amyloid β accumulation after Porphyromonas gingivalis infection"
こちらの論文の簡単解説になります。
さあ、いよいよ今回の論文の研究内容に入っていきます!
今回は、まさに”実験!!”って感じで面白いですよ!!
とは言え、「このニュースを慎重に見ようね」って趣旨は前の記事①②でほぼ伝わっていると思います。
「実験には興味ないぜ!!」って方は、最後の【まとめ】だけでも読んでもらえると嬉しいです。
※分かりやすさを重視するため、全文を解説しているわけではありません。気になる方は全文を見てください。
基礎知識:細胞がタンパク質を作る仕組み
まず、基礎知識の解説です。分かる人はスキップして下さい。
細胞がタンパク質を作る仕組みですが、こうなってます!
バン!!!
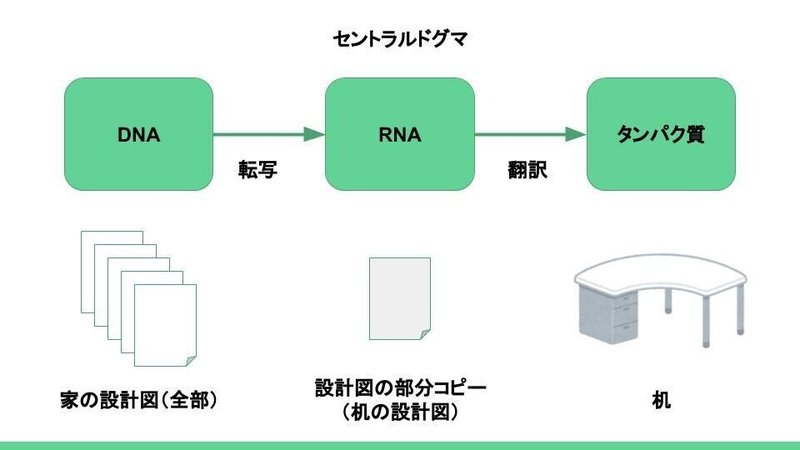
DNAというのは、みなさんご存知、細胞一つ一つの中にあって、体全体の設計図のようなものです。指の先の細胞から採ってきても、歯の中の細胞から採ってきても、同じ人のDNAは同じです。
でも、体の中の細胞は、それぞれ違う働きをします。それぞれ違う働きが出来るのは、それぞれの細胞でDNA(設計図)を使う場所が違うからです。
DNAには膨大な情報が入っているので、それを使いやすくするように、必要な部分のコピーを作ります。部分コピーですね。この部分コピーをRNAと呼びます。そしてコピーをすることを転写と言います。
そして、その部分コピーを使って、タンパク質を作ります。これを翻訳といいます。
この一連の流れをセントラルドグマと言います!!
響きがカッコいいですね!
この前の絵でも、イメージをお伝えしょう。
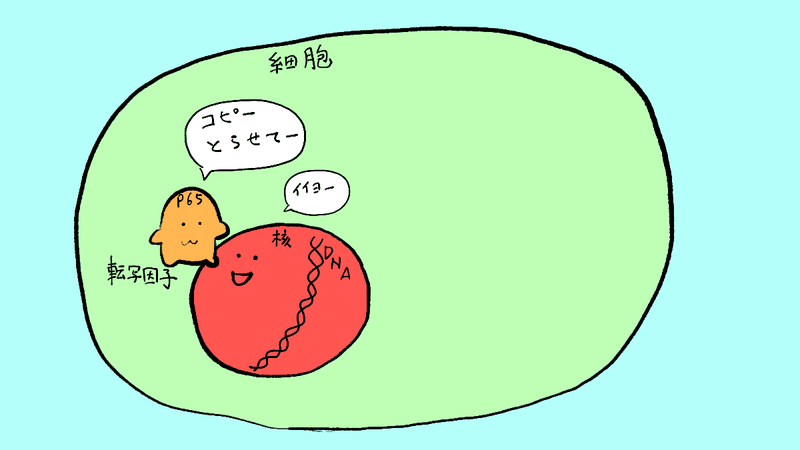
↑ここから始まります
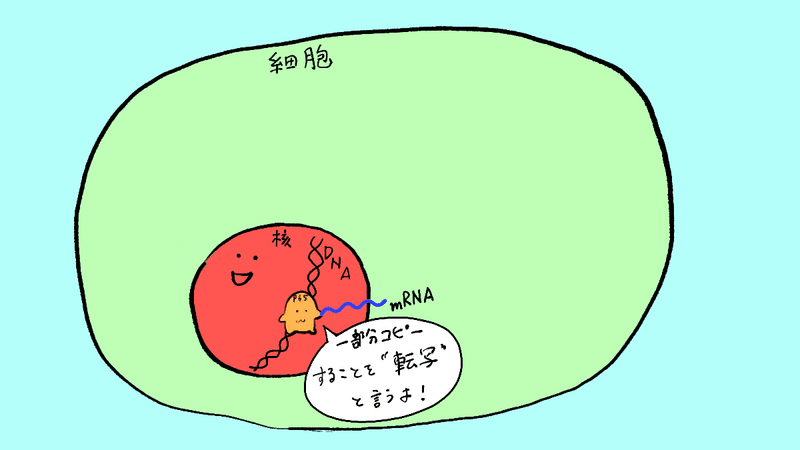
DNAから一部コピーをとってmRNAを作ります。これを転写と言います。
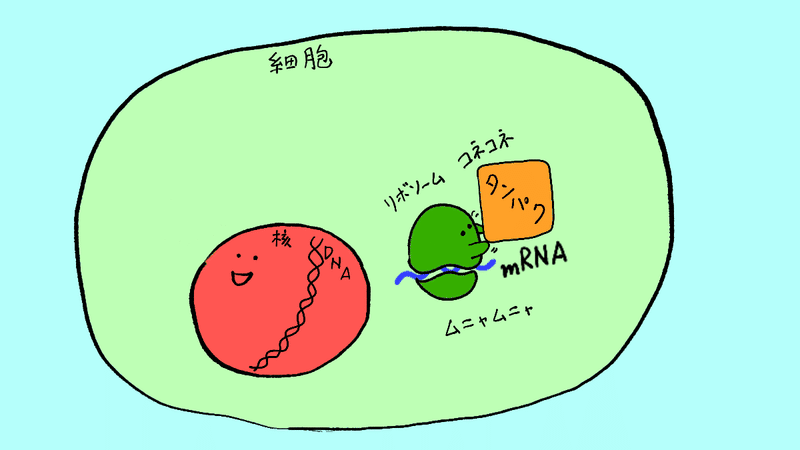
mRNAの情報をもとにリボソームというところで、タンパク質が作られます。これを翻訳と言います。
こうやって細胞内でタンパク質が作られます。
実験1:RAGE増えたよ
さて、具体的な実験内容と実験結果を見てみましょう。
実験1では脳内皮細胞(hCMEC / D3)にP. gingivalis(歯周病菌)を振りかけて、3,6,9,12時間後にどうなってるのか調べてます!
RAGEとか脳内皮細胞とか忘れた!って人のために、ちょっと復習します。
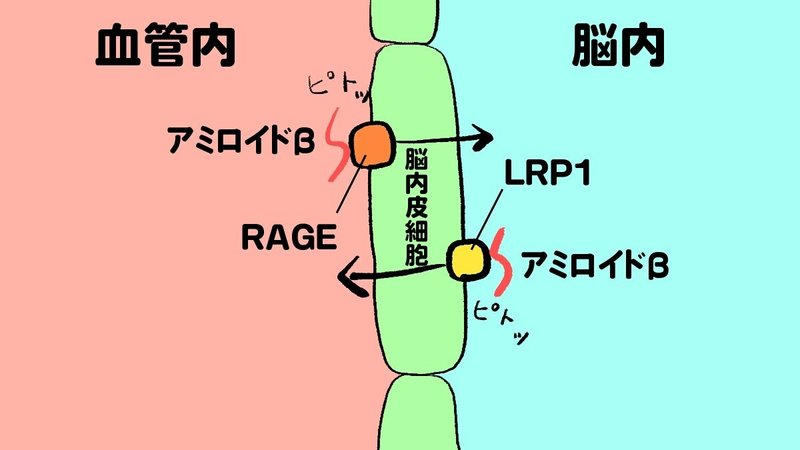
上の図を見ながら少し思い出してください。
・アルツハイマー病はアミロイドβって物質が”脳内”で蓄積することが原因で起こってるかも
・そのアミロイドβが”脳内”に行くためには、BBB(血液脳関門)≒脳内皮細胞を突破しなくてはいけない
・どうやら、脳内皮細胞のRAGE(終末糖化産物レセプター)にアミロイドβがくっつくことで、アミロイドβは脳内に移動しているらしい
どうでしょうか?思い出せましたか?では実験に戻ります。
ちょっと図の細胞を大きく書き直します(ここから細胞が主役なので)

アミロイドβはRAGE(タンパク質)にくっついて、脳内に入ることがわかっている、ということでしたね。この図に、最初に説明した、タンパク質が作られる仕組みを追加します。
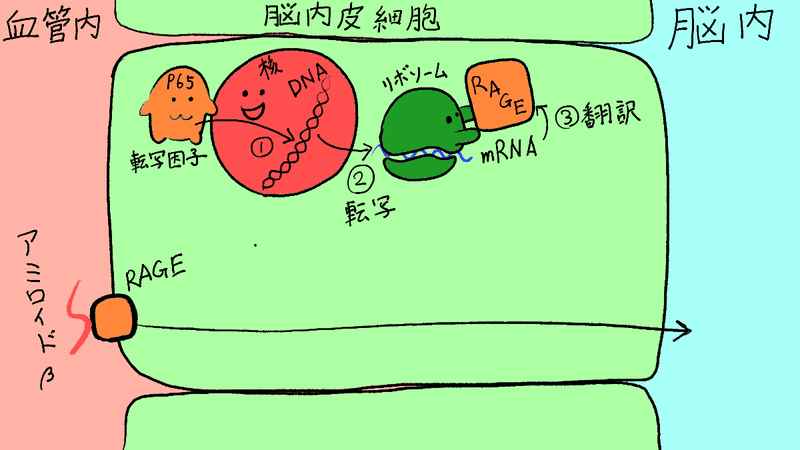
①転写因子がDNAを
②転写してRNAをつくる
③RNA情報を翻訳してタンパク質をつくる。
この絵では、タンパク質の名前をRAGEにしています。
さあ!準備は出来ました!!
P. gingivalisを振りかけてみますよ!
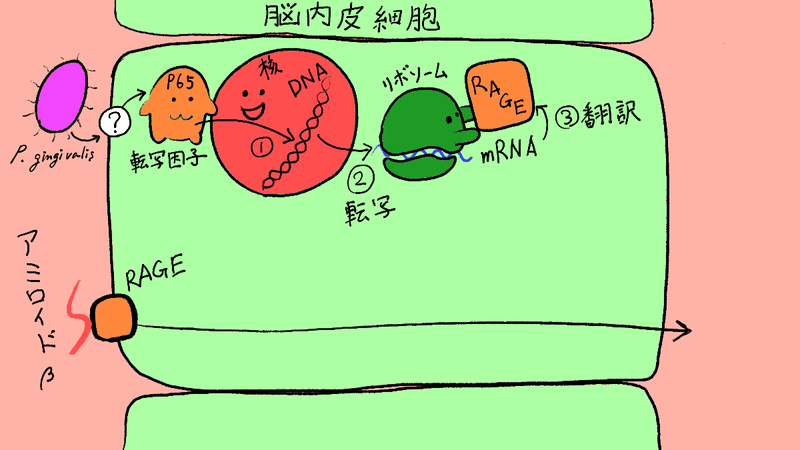
振りかけました!(試験管内の実験なので、血管内とか脳内ってのはなくしました。マイナーチェンジ)
そして、mRNAとRAGEの量を計測しました。
(3,6,9,12時間後で)
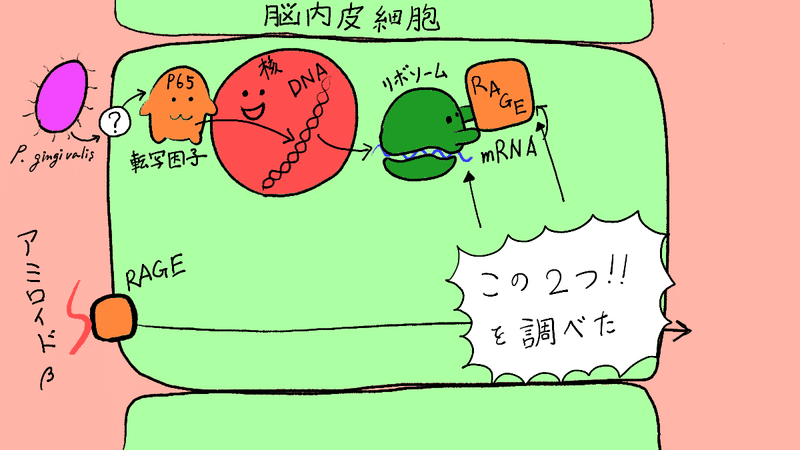
そうすると、この様になりました!(※グラフはイメージです。正式なグラフは、論文のfig. 1を見てください)
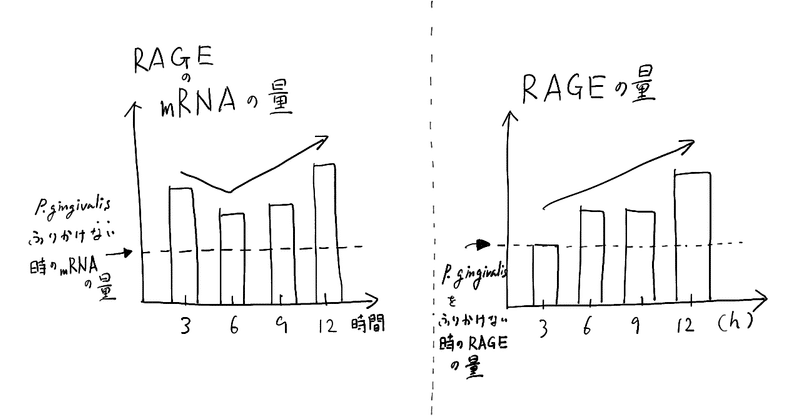
おお!mRNAの量も増えて、RAGEも確かに増え(アップレギュレーション)てそうですね!
(mRNAの量が3時間後よりも、6時間後で一旦下がっているのは、なんでかなぁ~とかは思いますが)
ちょっとだけまとめると、
P. gingivalisを脳内皮細胞に作用させると、RAGEのアップレギュレーションがおこった。
ということです。
もうここまでで、論文のタイトルはほぼ理解できるようになってませんか??
”脳内皮細胞における終末糖化産物受容体(RAGE)のアップレギュレーション(増加)は、P. ジンジバリス感染後の脳血管関連アミロイドβ蓄積を仲介します”
ね!長らくここまで読んで頂けて感謝です。
一応、この後の実験も見てみましょう(笑)
実験2:実験1のメカニズムを調べた!
脳内皮細胞に、P. gingivailsふりかけたら、RAGEが増えた。これが分かると、
「え?なんで?どういう経路で?」
と思うのが普通だと思います。それに答えてるのが実験2です。
実験1の絵の中で、?と書いた部分がありました。
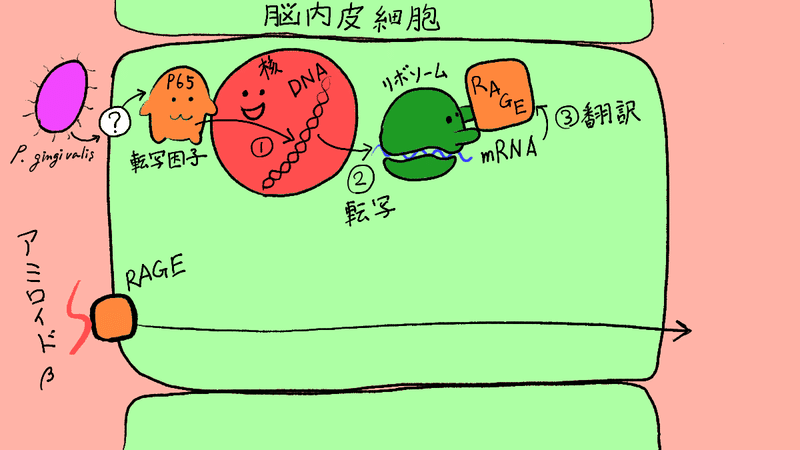
P. gingivalisが作用するのは分かったけど、そのメカニズムがどうなってるか分からない。ということで「?」としてました。実験2では、このあたりを調べてます。(ちょっと細々するので、実験3に行ってもいいですよ笑)
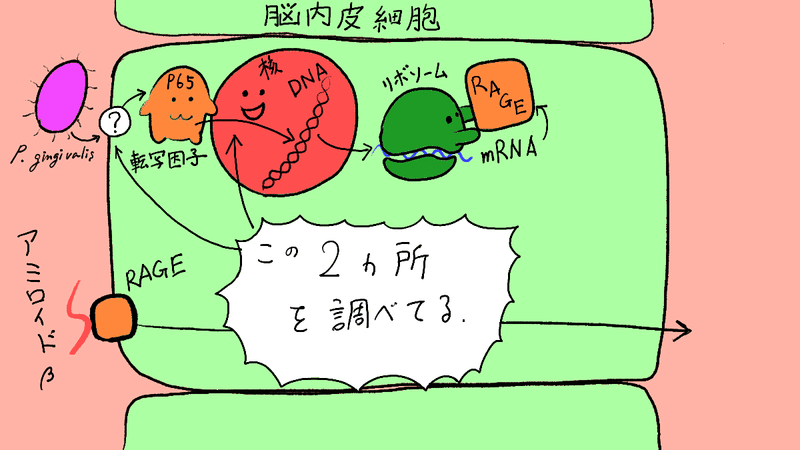
まず、P. gingivalisが細胞のどこにくっつくか?ですが、これは、他の実験から当たりをつけて、2つの”くっつく部位”(受容体と言います)を調べてます。
それが、
TLR2
TLR4
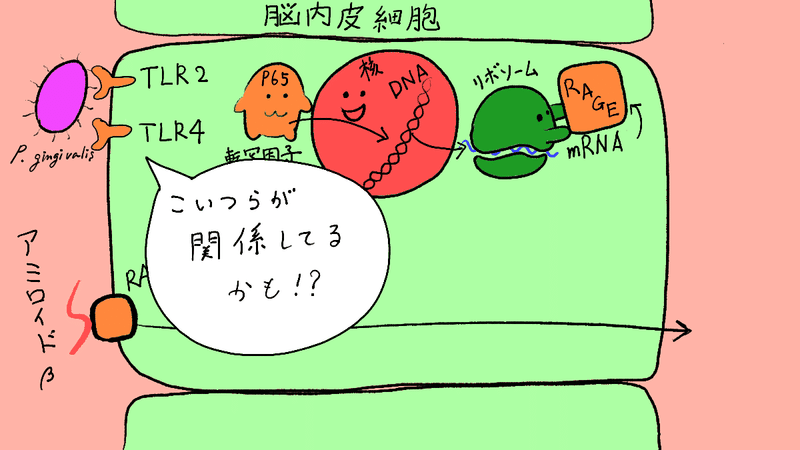
読み方は、「トル・ライク・レセプター」です。レセプター=受容体で、くっつく場所のことです。TLR2、TLR4どちらも、タンパク質で細胞内で作られて、細胞膜に配置されています。ですので、この2つのタンパク質のmRNAの量を調べました。
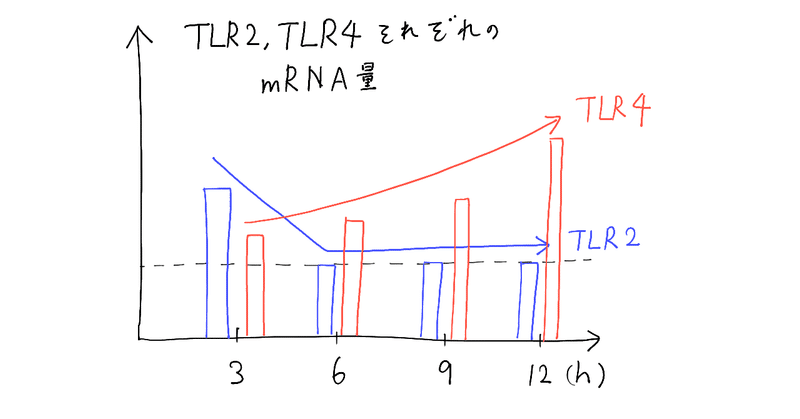
おお!TLR4は時間経過と共に増えてますね。TLR2も3時間後は増えてたけど、6時間を超えると、ベースライン(普段どおり)に戻ってますね。
一つ疑問は
「TLR2、TLR4が増えているから、P. gingivalisが”そこ”にくっついて作用している」って言える?
って事ですね。
専門ではないので、詳しくないですが、
「TLR4やTLR2を特異的に機能しないようにして、RAGEの増減を調べる」とかなら、「P. gingivalisがTLR4、TLR2にくっついて作用してる」と言えそうですが、色々技術的に難しいのかもしれません。
今回は深く追求せず、TLR2、TLR4にくっつくと仮定して話を進めましょう!
さらに詳しく調べます!
TLRにくっついた後、
転写因子(p65)←図ではオレンジ色のヤツ
が核内に入っていくと予想されます。
なので、
TLR→【?】→【p65が核内に移動】
ここの【?】の経路についても、後で調べてるのですが、
先に『p65が核内に本当に移動してる?』って事を調べているので、
先にそっちを見てみましょう。
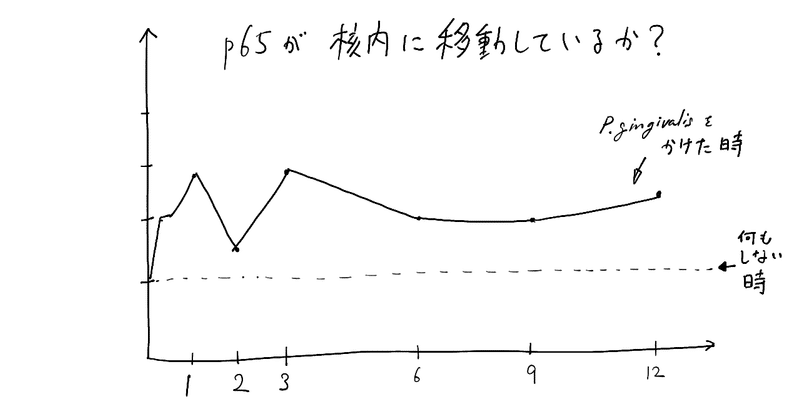
論文に載っていたグラフとは形が違うのは、横軸の目盛りが均等じゃなかったので、”だいたい”均等にしてみました。
P. gingivalisを振りかけてから、1時間後、3時間後は、何もしてないときに比べて3倍位に増えているのが分かります。
ほんまかよ?ってことで、p65を緑色に染めてみたりもしています。
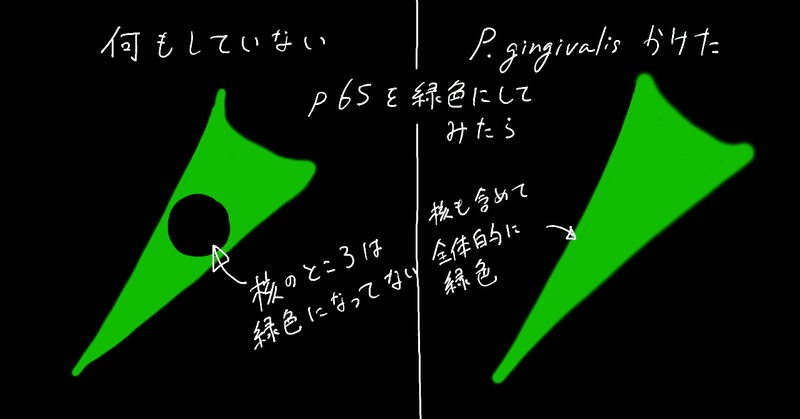
そうすると、何もしていない時は核のところは、あまり緑色になっていない(核内に移動していない)のに対して、P. gingivalisを振りかけた方は、全体に緑色になっています(核内に移動している)
このことから、転写因子p65は核内に移動していそうです。
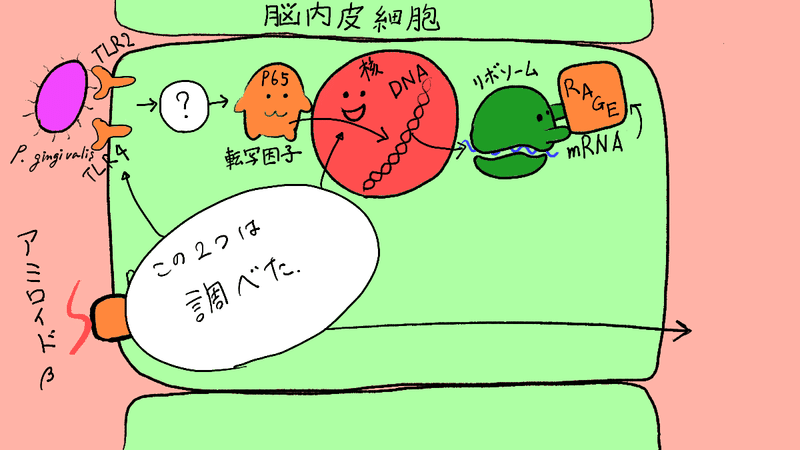
【?】の前後は調べました。では【?】の部分がどうなっているか?
これも、「TLR2、TLR4が反応すると、こういう風になったよ~」って以前の研究があるので、今回も同じように反応してるんじゃないか?
と”あたり”をつけて実験してます。
次の絵のようになってるんじゃないか?と考えて、pIκBαやIκBαの増減を調べてます。
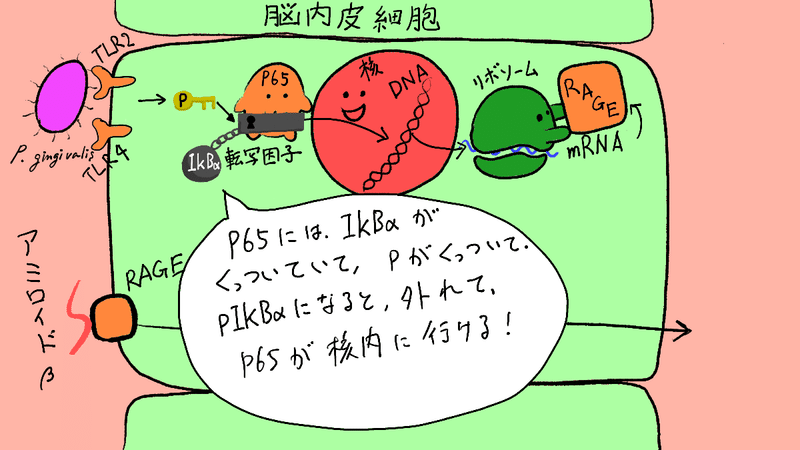
急に単語が増えて、びっくりしますね!
一つずつ解説します。
①転写因子p65はIκBαとくっついています。IκBαの”I”は”インヒビター”の”I"です。”インヒビター”とは”抑制するもの”って意味です。絵では”重し”みたいに表現してみました。
普段は、これがくっついているせいで、p65は核内に移動できません。
②そこに、pと書きましたが、”リン酸”です。リン酸がくっつくことをリン酸化と言います。リン酸化すると活性化するみたいなイメージです。今回は”鍵”にたとえてます。IκBαにpがくっついてpIκBαになると、分解されるので、p65から離れます。
③自由になったp65が核内に移動できるようになる
という仮説です。では実験でどうなっているか見てみましょう。
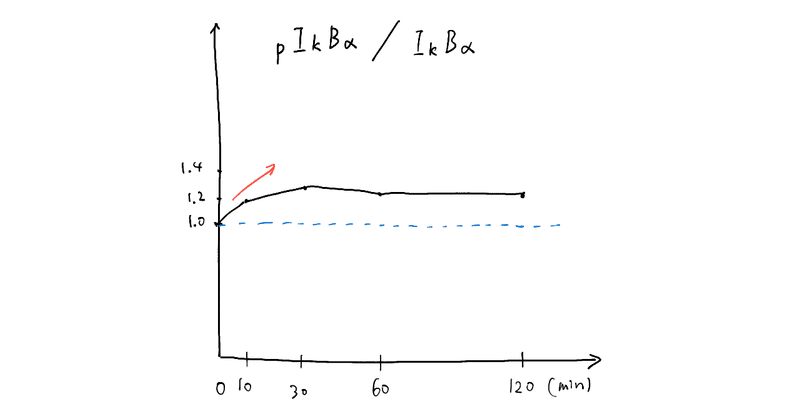
ふむふむ。pIκBαをIκBαで割っているから、相対的なpIκBαの量を見ているんですね。
pIκBαがIκBαより増えているから、IκBα→pIκBαになったのかなぁ~?って感じです。
はい。ということで、こんな流れみたいです。
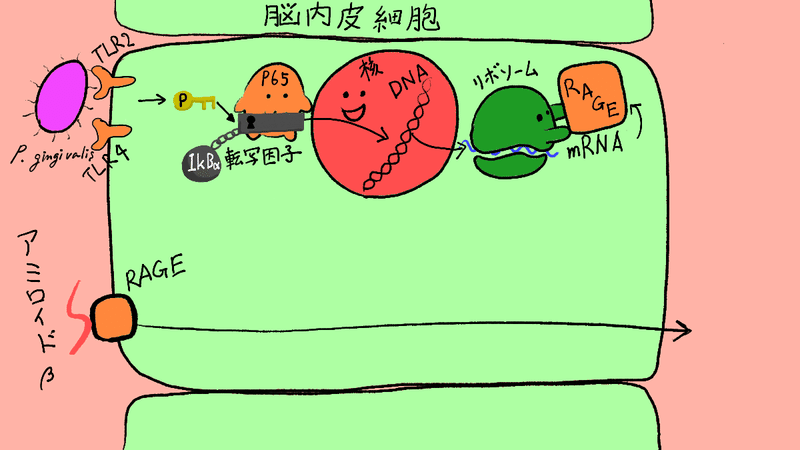
実験2の最後の仕上げとして、次のようなことをしています。
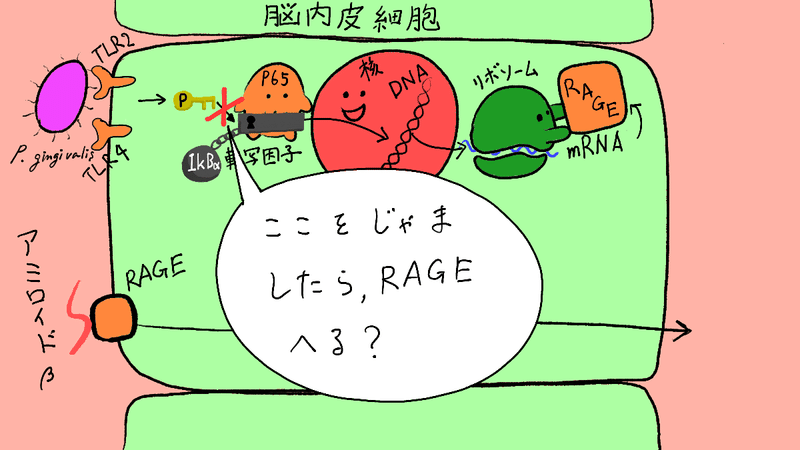
IκBα→pIκBαを邪魔する薬(阻害薬)を2種類試してみたけど、どっちもRAGE(のmRNA)の量減りました~って結果です。
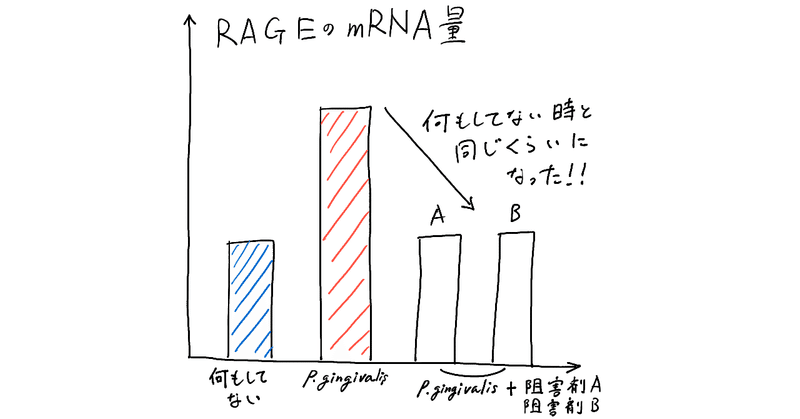
何もしてない時と、同じくらいのmRNAの量になりました!
って事は、この仮定はあってそうだなぁ~って話です。
実験3:CatBはIκBαを消化する
この実験は、まるっと省略!
なぜなら、この論文の著者が前に出した論文を補強するような実験だからです。
本筋には影響ありません。
結論だけ、CatBってタンパク質はIκBαを消化する。
実験4:RAGE増えて、ホントにアミロイドβ通過も増える!?
実験4では、ホントにRAGEが増えることで、アミロイドβが”通過”も増えているか!?って事を調べてます。
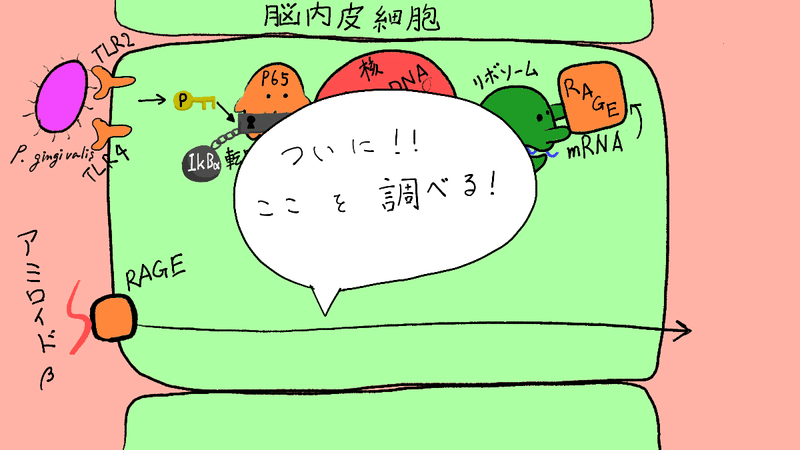
これを調べるためには、ちょっと工夫が必要でした。
この実験のために特殊な装置を作っています。
それがこちらです。
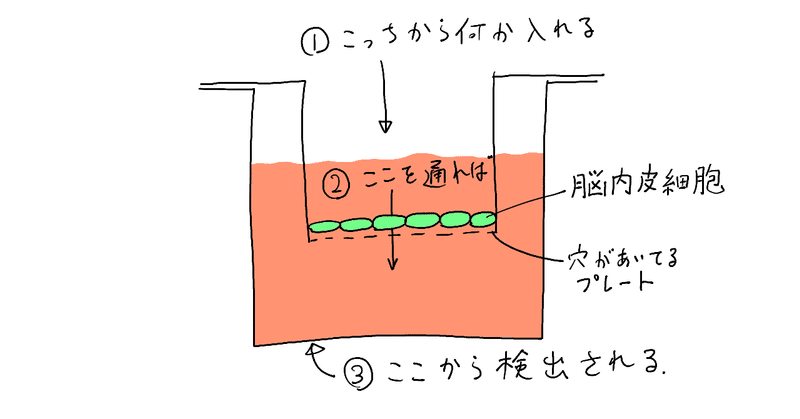
①になにか入れて、②が”選択的”に通したり、通さなかったりしてくれれば、③で検出される量が変化するということです。
まずはこの装置がちゃんと機能しているか、試します。
NaF(フッ化ナトリウム)を入れてみます!すると
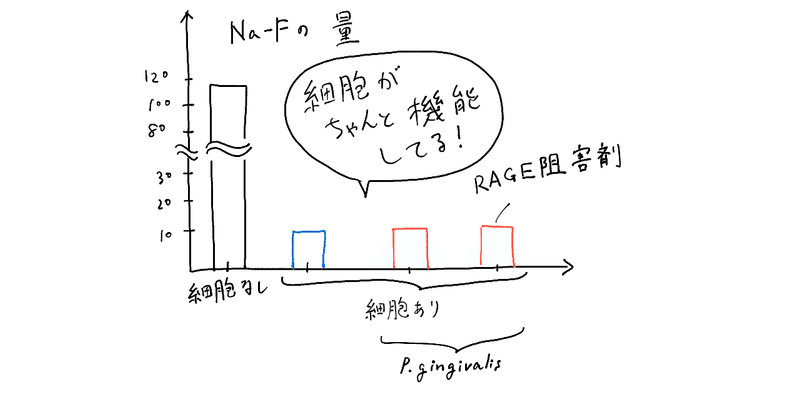
脳内皮細胞があると、NaFの量がガクッと減っていて、脳内皮細胞がフィルターのような役割をしてくれていることが分かります。
このグラフでは、脳内皮細胞あり・なし だけではなく
P. gingivalisに感染させたもの、
P. gingivalisに感染させた上にRAGEを機能させたくしたもの、
も一緒に機能していることを調べてます。この後の実験で使うので、ちゃんと機能していることを示しています。
ではアミロイドβを上から入れてみましょう!
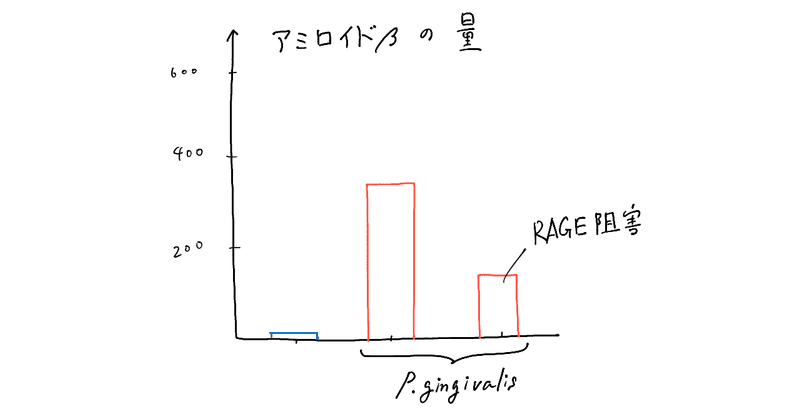
おお!P. gingivalisに感染していない脳内皮細胞は、アミロイドβをほとんど通していないのに対して、
P. gingivalisに感染するとアミロイドβを通過させていることが分かります!
(ただ、実際の論文のグラフも見て頂けるのであれば、バラツキ(誤差)が大きいのは気になります)
RAGEを阻害すると、アミロイドβの通過量も減っているので、たしかにRAGEがアミロイドβ通過に大きな役割を果たしていることが分かります。
(RAGE阻害をしていても、半分くらい通過しているのは、RAGE阻害剤の効果の問題なのかな?全部を阻害できるわけではない??)
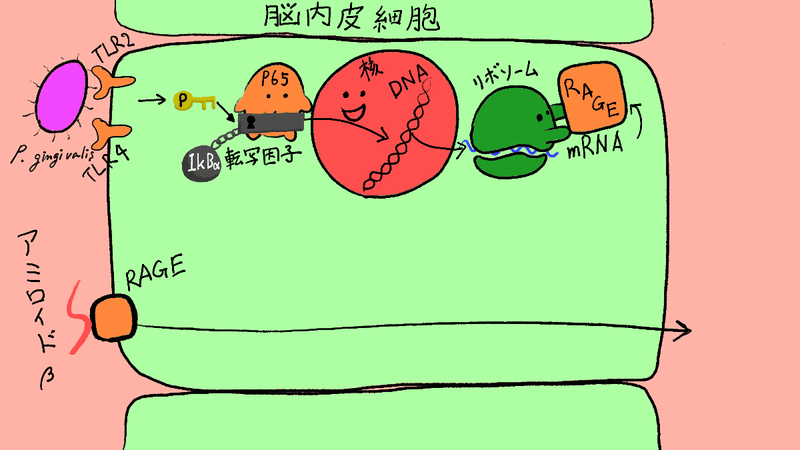
ここまでで、この図のようになってるんじゃないか?と示したことになります。
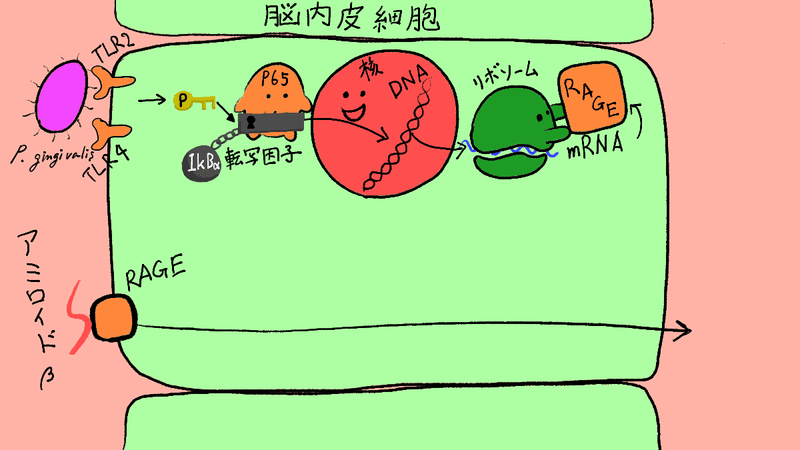
さぁいよいよ大詰め、最後の実験です。
実験5:マウスでも確かめてみよう!!
まずはマウスを準備します。
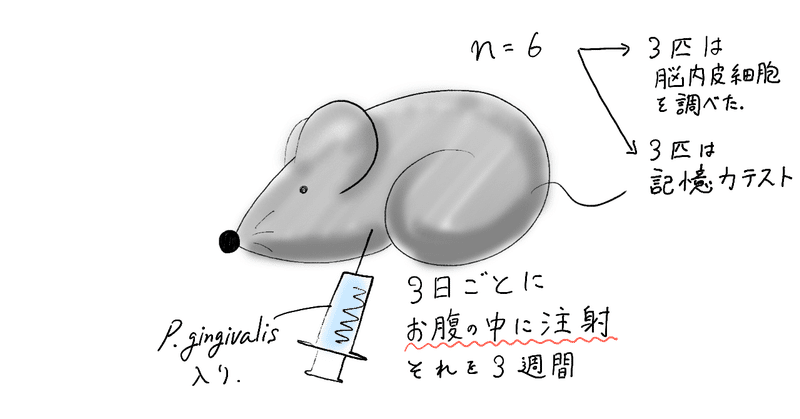
このように(?)
6匹のマウスには、P. gingivalisを3日毎に注射します。
お腹の中に直接注射ですよ!!ここはポイントです。
この内の3匹は記憶力テスト用です。
他3匹は3週間後に脳内皮細胞を調べられます。
また、比較のために3匹ずつ、計6匹はP. gingivalisを投与せずに飼います。
細胞の結果から見てみましょう。
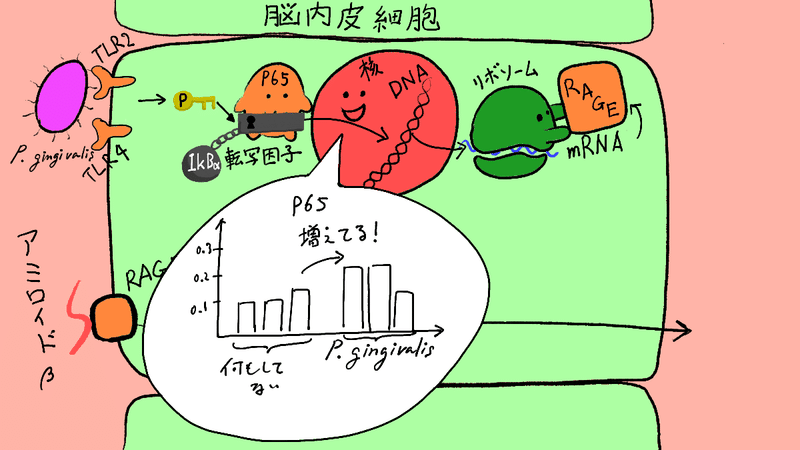
まずはP65が核内に移動しているか!?です。
数字が増えてるので、移動してそうです。
(縦棒が、3本ずつあるのは、マウスが3匹ずつだからですね)
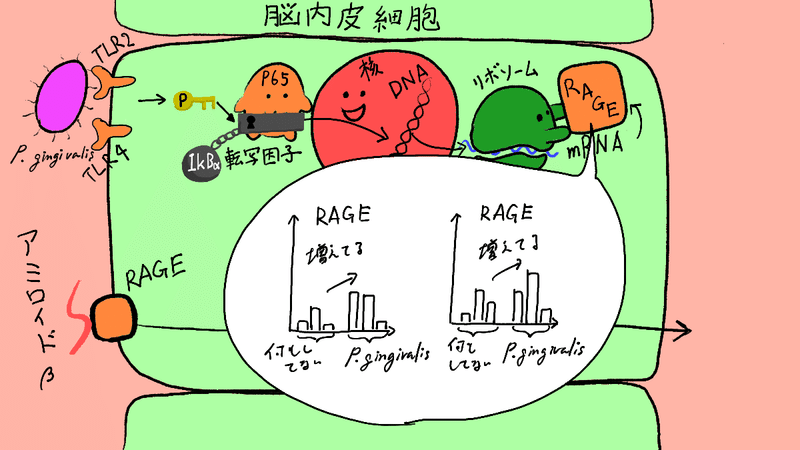
つぎにRAGEの量を2種類の方法で確認してますが、これも増えているようです!!
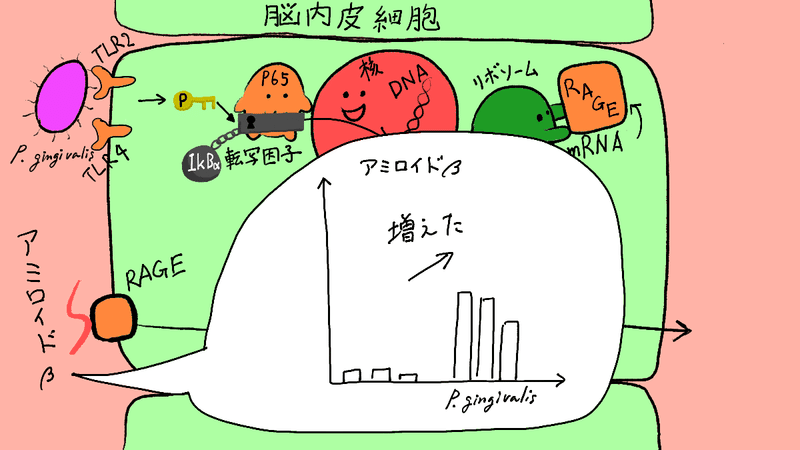
そしてアミロイドβ!これも増えてるようです!!
(脳内皮細胞付近のアミロイドβを調べているので、脳内で調べるのと差がある気もするので、そこは気になります)
つまり、このモデルってこれで良いんじゃない?と言いたいわけですね。
さあ、最後の最後に記憶力テストです!!
ニュースなどでは、ここだけ取り上げて、
「P. gingivalis で認知症に!?」
なんて煽るわけです。ここまで読んで頂いている皆様も、なんだかおかしな話だと思うはずです。
本当なら、認知症になっていることを証明したいんですが、
マウスなんでね。
認知症の診断が出来ないんですよ(笑)
なので、代わりに「ステップスルー受動回避テスト」という記憶力テストを行っているようです。
どんなテストか説明します。
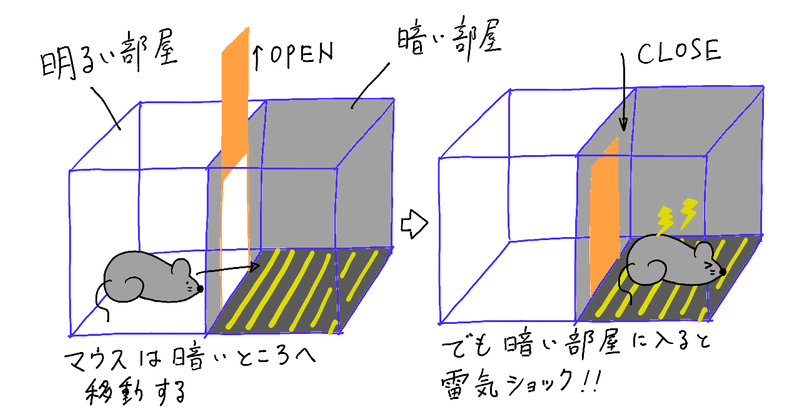
①マウスを明るい部屋に入れて、遊ばせておきます。
②ドアを開けると、マウスは暗い所が好きなので、暗い部屋に移動します。
③マウスが部屋に入ると、ドアが閉まって、電気ショックが流れます。
これによって、マウスは、この暗い部屋に入っちゃいけないって覚えるんですね。その後、
④もう一度明るい部屋にいれて、ドアを開けます
⑤マウスの記憶力が正常だと、暗い部屋に入りません。明るい部屋に今回は300秒留まってたらOKとしたようです。
この実験を、実験初日、1週間後、2週間後、3週間後で行いました。
では結果です。
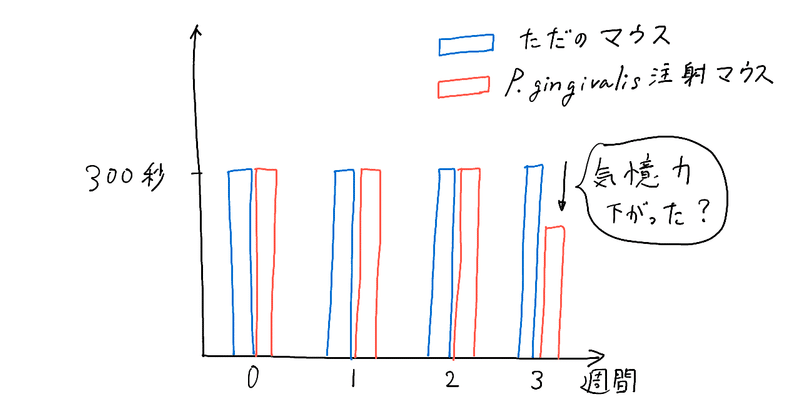
3週間後にP. gingivalisを3日毎に注射されていたマウスは、どうやら、300秒待てずに、暗い部屋に入ったようですね。
これによって、記憶力が低下していると考えられました。
(3日毎に菌を注射され続けたら、弱り果てそうな気も・・・)
まとめ
ここまで、お付き合い頂き本当にありがとうございました。
正直「誰が読むねん」と思いながら、実験の詳細を説明させて頂きました。
で、結局、この論文は何が言いたかったって言うと、これです。
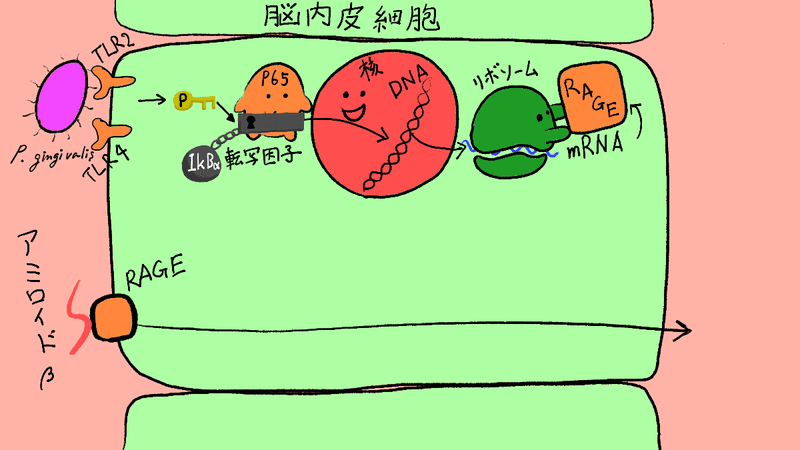
おそらく、細かいツッコミどころはたくさんあったと思います。
(特にマウスの実験)
ただ、そのツッコミの中には、自分たちの知識が足りないのが原因のものも結構あると思います。
それに、実験として、これで完璧!!って実験はなかなか難しいものです。予算もあります。時間も限られてます。
この実験は、とても面白く、緻密に詳細に調べられており、正直凄いです。尊敬します。
しかし、この研究結果を持って、
「歯周病菌が認知症の原因!」はどう考えても言い過ぎです。
認知症の予防については、WHOが
『認知機能低下および認知症のリスク低減』ガイドライン
というものを出しています。
日本語版もあります!!
まずは、このあたりの方法から試すほうが良いのではないかと思います。
以上
ではまた。
よろしければサポートお願いします。夢は大学機関なみに、論文へのフルアクセスが出来るようになる!です。
