
26)なぜ女性は男性より長生きするのか?
体がみるみる若返るミトコンドリア活性化術26
ミトコンドリアを活性化して体を若返らせる医薬品やサプリメントを解説しています。
【大きな動物は寿命が長く、太った動物は寿命が短い】
ゾウのように大きな動物は、ネズミのような小さな動物よりも寿命が長いことは良く知られています。一般的に、体の大きな動物ほど寿命が長いことになっています。その理由の一つは、大きな動物ほど成長と性成熟に時間がかかるからです。
しかし、同じ種であれば、太った個体や体格の大きい個体ほど寿命が短いことが多くのデータで明らかになっています。遺伝子改変で体格が大きくなるマウスを作ると、正常のサイズのマウスより寿命が短くなります。体格の大きなマウスは成長速度が促進し、生殖活動も旺盛ですが、活性酸素の産生が亢進し、寿命は短くなります。老化は成長の延長なので、成長が早いと老化も早くなると考えられています。
犬を例にとると、小型犬と中型犬と大型犬というように大きさによって寿命を比べると、体格の小さい犬ほど寿命が長いことが知られています。(下図)。
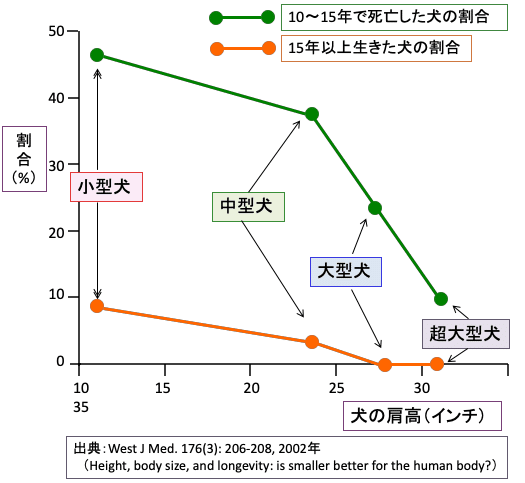
図:犬を肩高の大きさによって小型犬、中型犬、大型犬、超大型犬に分けると、体が小さいほど寿命が長いことが報告されている。上の図で、10年以上生きる割合(緑とオレンジを合わせた数値)は小型犬が50%以上で、中型犬で約40%、大型犬で約25%、超大型犬で10%程度というデータを示している。15年以上生きる犬は小型犬では10%近くいるが大型犬や超大型犬ではほとんどいない。
【身長が低いほど長生きする】
動物の例で紹介したように、同じ種の中では小さい個体ほど寿命が長いので、人間の場合でも身長と寿命は逆相関すると考えられています。実際に、身長と死亡率(特に、呼吸器系疾患と冠動脈疾患と脳卒中による死亡)との間に逆相関(身長が高いほど死亡率が高い)の関係があることが複数の研究で示されています。
低身長ほど寿命が短いというデータもあります。開発途上国のような貧困による栄養状態や衛生環境が悪い地域のデータでは、栄養不良を示唆する低身長の個体は感染症や心血管疾患の発症率が高く、寿命が短いというデータは納得できます。
しかし、栄養状態や社会環境が悪くない先進国では、低身長ほど様々な疾患の罹患率が低く、寿命が長いというデータが数多く報告されています。
例えば、アメリカのある地域で、白人や黒人や中国人や日本人やラテン系アメリカ人など体格に多様性の高い同じ地域に住む人口集団の解析では、中国人や日本人やラテン系アメリカ人の方が白人や黒人より寿命が長く、それは身長が関連していることが指摘されています。
何千人というプロ野球選手の身長と体重と死亡時の年齢のデータを解析すると身長が高いほど死亡年齢が低いことが示されています。映画スターなどの著名人を対象にした解析でも同様な結果(身長と寿命は逆相関する)ことが示されています。
米国のある研究では、身長が175.3cm以下の男性は身長が175.3cm以上の男性グループに比較して寿命が4.95年長いという報告があります。身長が170.2cm以下の男性は182.9cmの男性より7.46年長生きするという報告もあります。
低身長と高身長の寿命の差を検討した多くの研究をまとめた論文では、身長が1cm高くなると、0.47~0.51年の寿命の短縮があるという数値が報告されています。180cmの人は160cmの人の平均10年間ほど寿命が短くなるという計算です。
男性は女性より平均して約8.0%程度身長が高く、平均寿命は7.9%短いというデータがあります。これは平均すると女性は男性より約13cm身長が低く、寿命は6歳ほど長いということです。この数値は日本人でも当てはまります。1950年と2010年の30歳代の男女の身長差は12~13cm程度です。
女性の方が寿命が長い理由の一つは、体が小さいからで、その原因がインスリン/インスリン様成長因子-1/mTORC1シグナル伝達系の活性が女性の方が低いからという意見があります。 同じ身長で比較すると、女性も男性も寿命は同じという報告もあります。つまり、男女を問わず、身長や体格(=インスリン/インスリン様成長因子-1/mTORC1シグナル伝達系の活性)が寿命を決めているという仮説です。
【女性は男性よりがんの発生率が低く寿命が長い】
日本の2017年のがん統計によると、1年間にがんと診断されたのは約98万人で、そのうち男性は約56万人、女性は約42万人となっています。人口10万人あたりの粗罹患率(2017年)は男性が906.4人、女性は643.4人です。つまり、男性のがんの発生率は女性の約1.4倍です。
生涯でがんに罹患する確率は、男性65.5%で女性50.2%です。生涯でがんによって死亡する確率は、男性は24%、女性は15%というデータもあります。
がんは男女とも60歳代から増加し高齢になるほど高くなりますが、60歳代以降のがんの発生率は男性が女性より顕著に高いのが特徴です。70歳以上では1年間にがんになる率(がん罹患率)は、男性は女性の2.5倍以上です。(下図)。
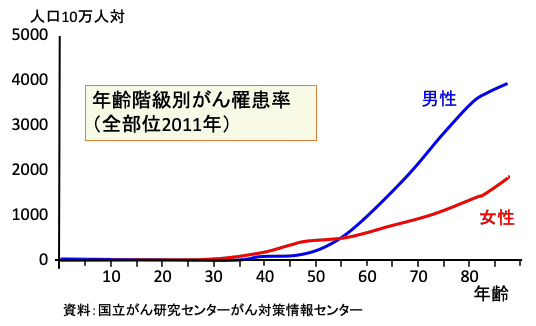
図:がんは加齢とともに発生率が上昇するが、60歳代以降のがんの発生率は男性が女性より顕著に高い。
がんの発生率が男性より女性の方がかなり低いという現象は、多くの国で確認されています。さらに、女性の寿命が男性より長いことも多くの国で認められています。
2019年の日本人の平均寿命は女性87.45歳、男性81.41歳で過去最高を更新しています。日本の場合、女性の平均寿命が男性より5~7歳長いというのは1965年以降ずっと続いています。1965年は平均寿命がまだ70歳前後のころです。1950年代は平均寿命が60歳代ですが、この頃でも女性の方が3~4歳ほど寿命が長いことがデータで示されています。
女性の方が男性より寿命が長いというのは、ほとんどの国で確認されています。特に寿命が長い先進国では、日本と同様に5~7歳くらいの男女差があり、しかも、寿命が延びるほど男女差が拡大する傾向にあります。世界中の100歳以上の人口の75%は女性で、110歳以上の人口の90%が女性と言われています。このように、がんの発生率や寿命における男女差の原因としては、様々な理由が考えられます。
一般的に男性は、喫煙や飲酒の量が多く、危険な職業等により、女性に比べて身体に悪い影響を受けていることから、女性より短命でがんの発生も多いと言われています。あるいは、女性ホルモンのエストロゲンが動脈硬化を予防する効果があるとか、性染色体(男性はXYで女性はXX)やミトコンドリアDNAの違いの関与など生物学的な様々な違いの関与も指摘されています。
女性より男性の方が身長が高いことは、男性の方が体の成長を促進する成長因子やシグナル伝達系が亢進していることを意味し、その結果、がんの発生が多く、寿命が短いと言う推測もあります。生物学的に「オスは屈強さを得るために寿命を犠牲にする」という考えです。
最近の老化の研究からこの男女差の原因の根本的な理由に哺乳類ラパマイシン標的タンパク質複合体1(mTORC1)が関与していることが指摘されています。mTORC1は体の成長を促進し、屈強な体を作る作用がありますが、この作用が老化を促進するという考えです。
【成長ホルモンやインスリンや性ホルモンは寿命を短くする】
成長ホルモン、インスリン、インスリン様成長因子-1、性ホルモンというのは体の成長や成熟に必要な因子で、中年以降に体の若々しさが低下するのはこれらの成長因子やホルモンの分泌が減少するためだと考えられています。したがって、アンチエイジング(抗老化、抗加齢)医療では、このようなホルモンや成長因子を補充して、体を若返らせようとする治療が行われています。
しかし、成長を促進し若々しさを保つような因子が、結果的には老化を促進し寿命を短くすることは多くの研究で証明されています。
例えば、線虫やショウジョウバエを使って寿命に関わる遺伝子の研究が行われています。線虫やショウジョウバエの突然変異系統(ミュータント:変異体)の中から寿命が延びた変異体を見つけ、どの遺伝子に突然変異が起きているかを解析すれば、寿命に関連する遺伝子を見つけることができます。
そのような研究によって寿命に関わる遺伝子が多数見つかっていますが、見つかった線虫やショウジョウバエの遺伝子の哺乳類の相同体を解析すると、それがインスリンやインスリン様成長因子-1(IGF-1)の受容体やそのシグナル伝達系に関与する遺伝子だということが明らかになったのです。
例えば、線虫の遺伝子でins-7とdaf-2と名付けられた遺伝子に突然変異がある変異系統の線虫は寿命が延びていました。そして、これらの遺伝子は哺乳類では、それぞれインスリンとインスリン受容体に相当するものでした。そして、インスリン受容体の下流に存在するシグナル伝達系に関与する遺伝子の突然変異も寿命を延長することが明らかになったのです。
このような線虫やハエの研究結果をもとに、遺伝子改変マウスを使った研究が行われています。例えば、成長ホルモンが過剰に発現しているマウスはIGF-1の濃度が上昇し、寿命が短くなり、がんの発生率が高まることが報告されています。成長ホルモンは肝臓に働きかけてインスリン様成長因子-1(IGF-1)を分泌させ、このIGF-1が標的組織の細胞分裂を刺激することによって体の成長を促進します。
逆に、成長ホルモンが産生できない成長ホルモン欠損マウスや成長ホルモン受容体が欠損したマウスを作成すると、これらの成長ホルモンの働かないマウスではがんの発生率が減少し寿命が延びることが示されました。ネズミに30~40%のカロリー制限を行うとIGF-1濃度が30~40%減少し、がんの発生率が低下し、寿命が延びました。
【インスリン様成長因子-1の血中濃度が低い人はがんが少なく寿命が長い】
人間でも、インスリン様成長因子-1(IGF-1)の低い人ほどがんによる死亡率が低いという報告や、IGF-1の低下しているほうが長寿であるという報告もあります。100歳以上の超長寿者では、成長ホルモンやインスリン/IGF-1シグナル伝達系の働きが低下するような遺伝子変異を持った人が多いという報告があります。
100歳以上まで生存した人(百寿者)の子孫と、比較的若く亡くなった人の子孫を比較すると、百寿者の子孫の方がIGF-1の血中濃度が低いという報告があります。成長を促進するIGF-1/インスリン系の活性が高いと寿命が短縮することを示唆しています。
高齢になってIGF-1が低い人は、寿命が伸び、がんの発生が抑制されます。そして、IGF-1の産生が低い体質や、IGF-1で誘導される細胞内シグナル伝達系の働きが弱い遺伝的素因を持った人は、長寿でがんが発生しにくいことを示唆します。
IGF-1はインスリンと構造が似ており、それらの受容体も似ているため、インスリンとIGF-1は相互に交叉反応します。したがって、インスリンの分泌を促進する糖質の多い食事は、インスリン/IGF-1シグナル伝達系を活性化し、寿命を短くし、がんの発生を促進することになります。逆に、カロリー制限やケトン食や糖質制限などの食事療法はインスリン/IGF-1シグナル伝達系を抑制し、がんを予防し寿命を延ばす効果が期待できます。
100歳以上まで健康に生きるような人は、長生きする遺伝的素質を持っているのですが、その候補の一つがインスリン/IGF-1シグナル伝達系の活性が低下するような遺伝形質ということです。
【哺乳類ラパマイシン標的タンパク質複合体1は栄養と増殖シグナルを感知して増殖を制御する】
細胞の増殖というのは、栄養とエネルギーが利用できる状態にあるときに、細胞構成成分(タンパク質、核酸、脂質など)を新規に合成して、細胞の数を増やす生化学的プロセスです。したがって、増殖するためには、細胞を新たに作る材料(栄養素)とエネルギー(糖質や脂質を分解して得られるATP)が必要です。
増殖因子や成長因子やホルモンなどによって細胞増殖のシグナルが来たときに、栄養素とエネルギーの供給が十分にある条件で、タンパク質や脂質の合成を促進して細胞増殖を実行するのが哺乳類ラパマイシン標的タンパク質複合体1(mTORC1)です。
ラパマイシン(Rapamycin)は1970年代にイースター島(モアイ像で有名な南太平洋の島)の土壌から発見された放線菌の一種が産生する有機化合物です。ラパマイシンの生体内のターゲット分子が、哺乳類ラパマイシン標的タンパク質(mammalian target of rapamycin)、略してmTOR(エムトール)というタンパク質です。
mTORはラパマイシンの標的分子として同定されたセリン・スレオニンキナーゼ(タンパク質のセリンやスレオニンをリン酸化する酵素)で、細胞の分裂や生存などの調節に中心的な役割を果たすと考えられています。
最初に酵母におけるラパマイシンの標的タンパク質が見出されてTOR(target of rapamycin)と命名され、後に哺乳類のホモログ(相同体)が見出されてmTOR(哺乳類ラパマイシン標的タンパク質)と命名されました。
mTORにはmTOR複合体1(mTORC1)とmTOR複合体2(mTORC2)の2種類があります。mTORに幾つかの他のタンパク質が結合して複合体を形成しますが、結合しているタンパク質の違いで2種類の複合体ができ、異なる機能を担っています。
mTORC1は成長因子や、糖やアミノ酸などを含む栄養素のセンサーとして機能し、mTORC2は細胞骨格やシグナル伝達の制御をしています。インスリンやインスリン様成長因子(IGF-1)によって活性化されるのはmTORC1の方です。ラパマイシンで阻害されるのもmTORC1の方です。
インスリン、インスリン様成長因子-1、成長ホルモンなどの増殖刺激が細胞に作用すると、それらの受容体などを介してPI3キナーゼ(PI3K)というリン酸化酵素が活性化され、これがAktというセリン・スレオニンリン酸化酵素をリン酸化して活性化します。活性化したAktは、細胞内のシグナル伝達に関与する様々な蛋白質の活性を調節することによって細胞の増殖や生存の調節を行います。このAktのターゲットの一つがmTORC1です。
アミノ酸も別の経路でmTORC1の活性を高めます。mTORC1の活性化においてアミノ酸(哺乳類では特にロイシン)が必須であり,これはアミノ酸が十分である場合に限り細胞がタンパク合成を開始できる仕組みと言えます。
このようにして、栄養源と増殖シグナルを感知して細胞の成長や分裂を促進するのがmTORC1です。
一方、細胞内のエネルギー低下を感知するのがAMP活性化プロテインキナーゼ(AMPK) です。グルコース欠乏や低酸素などにより細胞内ATP量が減少すると、AMP/ATP 比の増加に伴いAMPKが活性化されます。AMPKはmTORC1活性を抑制して、異化の亢進や細胞周期の停止をもたらし、エネルギー消費の抑制(同化抑制)とエネルギー産生の亢進(異化促進)へと細胞の代謝をシフトさせます。さらに、AMPKはmTORC1活性を低下させ、細胞の増殖を抑制します。
このように、mTORC1とAMPKは、細胞内の栄養素とエネルギーの状況を感知して増殖の制御に中心的な役割を担っています(下図)。
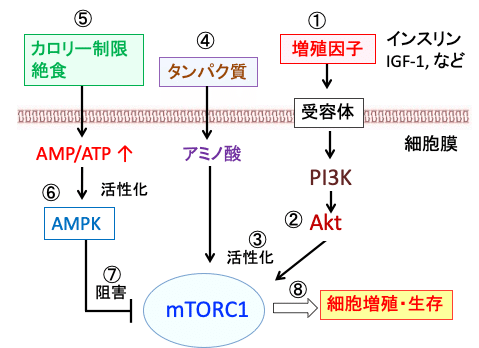
図:インスリンやインスリン様成長因子-1などの増殖因子(①)が細胞に作用すると、それらの受容体を介してPI3キナーゼ(PI3K)というリン酸化酵素が活性化され、これがAktというセリン・スレオニンリン酸化酵素をリン酸化して活性化する(②)。活性化したAktはmTORC1を活性化する(③)。タンパク質の豊富な食事は、アミノ酸によってmTORC1が活性化される(④)。カロリー制限や絶食(⑤)は、ATPの産生が低下してAMP/ATP比が上昇し、AMP活性化プロテインキナーゼ(AMPK)が活性化される(⑥)。AMPKはmTORC1活性を阻害する(⑦)。mTORC1が活性化されると細胞の増殖と生存が促進される(⑧)。このようにmTORC1とAMPKは栄養状態と増殖シグナルを感知して細胞の増殖や生存を制御している。
【mTORC1が老化を促進する】
最近の老化の研究では、インスリンやインスリン様成長因子-1などの増殖シグナルで活性化されるmTORC1(哺乳類ラパマイシン標的タンパク質複合体1)の関与の重要性が指摘されています。寿命と発がん率の男女差の説明にもmTORC1の観点から考察されています。
マウスを使った実験では、mTORC1活性を遺伝子改変や阻害剤(ラパマイシンなど)で抑制すると、老化関連疾患の発生が遅くなり、寿命が延びることが報告されています。
例えば、ある研究では、遺伝子改変技術によってmTORC1タンパク質を生存に最低限必要な約25%しか生成できないマウスを作成しました。このマウスは、通常のマウスに比べて小さかったのですが、他の身体的特徴は同一でした。
そして、このmTORC1活性が正常の25%程度しかないマウスは正常のマウスに比べて寿命が約20%延びることが明らかになりました。具体的には、mTORC1が低下したマウスのオスは平均して28.0ヶ月、メスは31.5ヶ月生き、通常のマウスの平均であるオス22.9ヶ月とメス26.5ヶ月に比べ て、約20%長生きしました。人間でいえば80歳が96歳まで寿命が延びる計算になります。
【男性は女性よりmTORC1の活性が高い】
ハエから人間を含めた哺乳類までほとんどの生物種において、オスはメスよりも大きくて強いが、寿命はメスより短いことが知られています。
細胞の成長はmTORC1によっては促進されますが、成長が完了すると、mTORC1は増殖ではなくて老化を促進します。オスとしての強さを得るためにmTORC1の活性を高める必要があるのですが、mTORC1の活性が亢進すると老化が促進されるので、オスは強さ(屈強さ)を得るために寿命を犠牲にしている可能性が指摘されています。
実際にマウスを使った実験では、メスに比べてオスの方がmTORC1活性が高いことが明らかになっています。そして、mTORC1活性を阻害するラパマイシンという薬を投与するとオスもメスも寿命が延長しました。
mTORC1が活性化されるとタンパク質や脂質の合成が亢進し、体が大きく屈強になります。
これは若いオスにとっては生存競争に有利になります。しかし、mTORC1が活性化されると老化が促進されるので、寿命を犠牲にしなければならないということになります。mTORC1はがん細胞の増殖を促進します。
したがって、オスの方がメスよりもがんの発生率が高く、寿命も短いことの説明がmTORC1の活性がオスの方が高いということで説明できるという考えです。
【老化は成長の延長】
生まれてから生殖年齢に達するまで、生き物は成長します。この成長過程において、成長ホルモンやインスリンやインスリン様成長因子や、PI3K/AKT/mTORシグナル伝達系や性ホルモンや様々な成長因子が重要な役割を果たします。特にmTORが細胞の増殖や成長の中心的役割を果たしています。成長が終了したあとは、成長に関わってきた全ての因子が老化を促進し、がんの発生を促進する方向で作用します。
性成熟を促進する女性ホルモン(エストロゲン)や男性ホルモン(アンドロゲン)はそれぞれ乳がんと前立腺がんの発生と進展を促進します。
成長ホルモンやインスリン、インスリン様成長因子、上皮成長因子など体の成長を促進する様々な因子は、成熟年齢を過ぎると、老化とがんの発生・進展を促進します。
成長した段階でmTORを低下させるようにスイッチを切り替えるとその個体の寿命を延ばすことができるのですが、生き物はそのようには進化していません。生殖年齢に達した後は、そのまま老化を促進させる方が種の繁栄には都合が良い(若い世代に生きる場所と食料を与える方が種の繁栄には有利)ので、敢えて、成長に関わる因子がそのまま老化を促進し、生殖の終わった個体の死を早めているのです。
成長は「プログラムされた正常機能」ですが、老化は「成長の延長(過剰機能)」であり、成長終了後はmTORC1の活性は老化と発がんを促進する方向に作用します。mTORC1を活性化して屈強な体を作るときは、寿命を犠牲にし、発がんリスクを高める可能性があるのです。
「老化は成長の延長」という生物の根本的な仕組みを利用すれば、自然の摂理に逆らって寿命を延ばすことができます。
つまり、中年以降はmTOR自体あるいはmTORの活性化に関わる要因を減らせば、老化性疾患の予防と寿命の延長を達成できます。 成長が終了し生殖年齢に達したあとはmTORの活性を高めるようなことはがんの発生を促進し、寿命を短くすることになります。
プロのスポーツ選手、特に体重や筋肉を増やすようなスポーツ選手は老化や発がんを促進する可能性が高いことが指摘されています。
牛乳タンパク質や糖質の多い食事も、mTORの活性を高める作用があるので、老化と発がんを促進する可能性があります。インスリンやアミノ酸のロイシンはmTORC1活性を高めます。
したがって、糖質やロイシンの多い肉や乳製品を減らし、AMPK(AMP活性化プロテインキナーゼ)活性を高めるメトホルミンやmTORC1活性を抑制するジインドリルメタン、レスベラトロール、プテロスチルベン、クルクミン、エピガロカテキンガレートなどの天然成分は、寿命延長とがん予防の両方にメリットがあると考えられています。
また、アンチエイジング(抗加齢)の治療では、年齢とともに低下した成長ホルモンや性ホルモンやインスリン様成長因子-1(IGF-1)を補って若返りをはかる方法が行われていますが、確かに体は一時的には若返りますが、長期的な寿命とがん発生リスクの上昇ということを犠牲にしている可能性があります。(下図)。
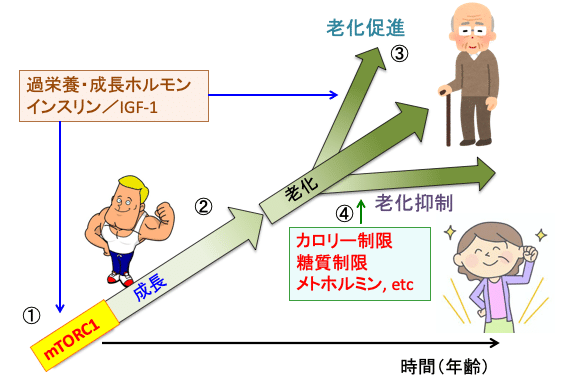
図: mTORC1(哺乳類ラパマイシン標的タンパク質複合体1)は成長ホルモンやインスリンやインスリン様成長因子-1(IGF-1)など様々な成長因子や過剰な栄養によって活性化され(①)、細胞の増殖や体の成長を促進する役割を担っている(②)。成長が終了したあともmTORC1の働きが過剰に続くと、細胞や組織の老化が促進される(③)。カロリー制限や糖質制限やメトホルミンなどはmTORC1の活性を抑制することによって、老化速度を遅くし、寿命延長の効果を発揮する(④)。
【現代社会では虚弱な方が長生きする?】
日本の場合の平均寿命の推移は以下のようになっています。
1900年ころ:男性42歳、女性44歳
1947年ころ:男性50歳、女性54歳
1960年ころ:男性65歳、女性70歳
1980年ころ:男性74歳、女性80歳
そして最近:男性80歳、女性87歳
つまり、この100年間で男女とも40歳代から80歳代に寿命はほぼ2倍になっています。
戦前の死亡原因としてもっとも多いのが、肺炎や胃腸炎といった感染症でした。肺炎と気管支炎を合計すると1899年から1922年まで第1位の死因でした。1930年代から戦後しばらくは結核が死因第1位でした。
第2次大戦後、栄養状態や衛生状態の改善や、抗生物質の出現などの医療の発達に伴い、感染性疾患が大幅に減少し、結核対策も進んだ結果、これら感染性疾患による死亡は急速に減少していきます。1950年代に入ると、感染症に代わって、悪性新生物(がん)、脳血管疾患、心臓疾患など老化と結びついた疾患が増大してきました。
感染症が死因の第一位を占めていたころは、mTORC1活性が高い屈強な人が生き残り、虚弱な人は感染症で若いうちに亡くなっていたと思われます。
しかし、抗生物質の出現や栄養状態や衛生状態の改善によって、虚弱な人でも感染症で死ななくなると、そのような虚弱な人の方が長生きするようです。
幼少期から病気をしたことが無いという屈強な人が、中年以降は糖尿病や高血圧や動脈硬化やがんなどの加齢関連の慢性疾患に罹りやすいようです。それは、mTORC1活性が高い状態は、成長期に体を屈強にして抵抗力も高いので、感染症が多い時代には生き残る上でメリットがありましたが、そのような体質は中年以降は老化を推進し、寿命を短縮することになります。
逆に、昔だったら感染症で死んでいたような虚弱な人は、中年まで生存すれば、その後は長生きするようです。mTORC1活性が低い体質なので老化速度が遅いからです。つまり、現代社会では、子供のときに病気がちな虚弱な人が、子供のときから屈強な人よりも長生きするように思います。
体が大きいほど、早死にすることは多くの研究で明らかになっています。体の大きい人は、成長ホルモンやインスリン様成長因子の活性が亢進し、mTORC1活性が高い状態にあるからです。
つまり、生殖年齢を超えた中年以降は、mTORC1活性を高めない食事や生活習慣や薬の服用によって寿命を延ばすことは可能と言えます。
この記事が気に入ったらサポートをしてみませんか?
