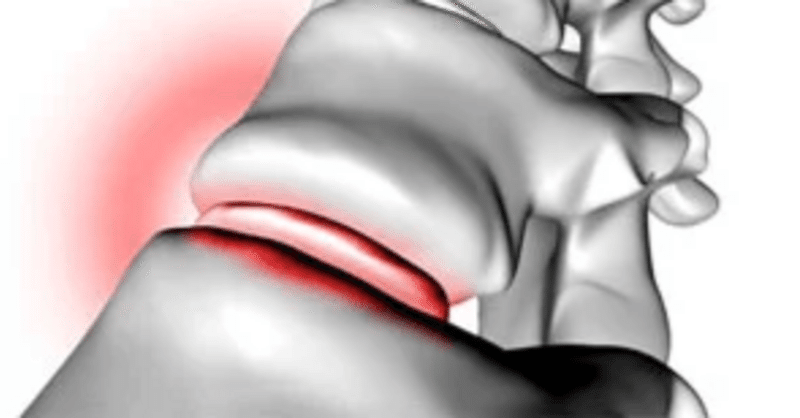
椎間板の変性:概日リズム・遺伝
24時間稼働する組織生理:椎間板の概日リズム
脳と末梢組織の概日時計は、明/暗、休息/活動、摂食/絶食サイクルを通じて、局所の生理機能を時間的に調整して、24時間のリズミカルな環境に合わせます。概日リズムの乱れ(加齢、交替勤務、時差ボケによる)は、筋骨格系を含む組織の変性や疾患の危険因子として提案されています。脊椎の椎間板 (IVD) は椎骨を分離し、脊柱の動きを可能にします。IVD 変性は高齢者の間で非常に蔓延しており、腰痛の主な原因となっています。IVD は、休息/活動サイクルの概日リズムによって引き起こされる負荷パターンの日内変化を経験することが知られています。近年、IVD 内に分子概日時計が存在し、その乱れにより組織の老化が促進され、 IVD 変性を起こしやすくなるという新たな証拠が示されています。IVD における細胞固有の概日時計は、IVD トランスクリプトームの約 3.5% の発現をリズミカルに制御することで生理機能と病態生理機能の重要な側面を制御し、細胞が 1 日を通して起こる劇的な生体力学および化学変化に対処できるようにします。実際、長期シフト勤務者に関する疫学研究では、腰痛の発生率が増加していることが示されています。このレビューでは、IVD を組織系の例として、健康と病気における概日リズムに関する最近の発見を要約します。私たちはリズミカルな IVD 機能に焦点を当て、生物学的タイミング機構を利用して組織の健康を改善し、変性を軽減する意義について議論します。筋骨格系概日時計に関する最近の発見を考慮すると、これらの発見は慢性リウマチ疾患においてより広範な意味を持つ可能性がある。

椎間板 (IVD) 内の分子概日時計は、椎間板の生理学と病態生理学を調節する上で重要な役割を果たします。これらの時計が乱れると、組織の老化が加速し、IVD変性のリスクが高まる可能性があります。 -疫学研究により、IVDの変性と関連する長期交代制勤務者の腰痛の発生率が高いことが示されています。このことから、交代制勤務者が経験するような概日運動の乱れが椎間板の変性の危険因子である可能性が示唆されている。 -休息/活動サイクルの概日リズムによって椎間板が経験する負荷パターンの日中の変化は、椎間板の健康と機能に影響を及ぼします。 -IVDの細胞固有の概日時計は、IVDトランスクリプトームのかなりの部分の発現を調節し、1日を通して起こる生体力学的および化学的変化に細胞が適応できるようにします。 -筋骨格系の概日時計は他の組織でも確認されているため、この論文の知見は慢性リウマチ性疾患に対してより広い意味を持っている。これは、生物学的タイミングメカニズムを利用して、さまざまな筋骨格系疾患における組織の健康状態を改善し、変性を緩和できる可能性を示唆している
椎間板細胞の画像評価により、椎間板修復研究に影響を与える生物多様性が明らかになった。
椎間板 (IVD) は、構造と機能が異なる結合組織の複雑な集合体であり、脊椎の骨間の重量を支えるクッションとして集合的に機能します 。IVD の外側領域は線維輪 (AF) であり、脊椎の軸方向の圧縮時に IVD 内で生成されるフープ応力を含む連続層またはラメラからなるコラーゲンが豊富な組織です。これらは AF に引張特性を与え、これらの圧縮荷重の散逸において。AFはIVDの中央領域である髄核(NP)を取り囲んでいます。髄核(NP)は、水を吸収して複合IVDに流体力学的重量支持特性を提供するプロテオグリカン(アグリカン)が豊富なゼラチン状組織(少なくとも乳児期)です。硝子様軟骨の上層と下層である軟骨終板 (CEP) には、IVD と隣接する椎体 (VB) の間の頭側および尾側で接する NP がさらに含まれており、非常に大きな圧縮荷重下で NP が VB 内に押し出されるのを防ぎます。軸方向の脊椎荷重がかかるときに影響を受けます 。IVD 組織成分は、さまざまな種類の細胞によって合成、組み立て、維持されます。AF には、細長い紡錘形の線維芽細胞のような相互接続された細胞の集合体が含まれており、これらの細胞は線維状コラーゲン性層状層の間および内部に配置されています。内側の AF では、これらの細胞は外側の AF 細胞よりもふっくらとした丸い形態をとります。NP の細胞は、新生児では大きく空胞が多いと報告されていますが、出生後すぐに小さくなり、アグリカンとアグリカンが豊富な間質および領域間マトリックス内に設定された明確な細胞周囲マトリックスに囲まれた単一の丸い軟骨細胞様細胞として発生します。 CEP の細胞は丸い軟骨細胞様の形態を持ち、線維軟骨の NP および AF、および椎体の骨と融合するガラス質硝子軟骨マトリックスに囲まれています。

椎間板石灰化のメカニズム
腰痛は、世界中で障害の主な原因となっています。椎間板(IVD)変性は腰痛を伴うことが多いですが、無症状の場合もあります。IVD 石灰化は、臨床的に重大な影響を及ぼす可能性がある、見落とされがちな椎間板表現型です。IVD 石灰化は、加齢や変性脊柱側弯症の脊椎疾患において珍しい所見ではありませんが、無視され、過少報告されることがよくあります。IVD の石灰化は、IVD の硬直化や部分的な生体力学の変化、より重度の IVD 変性、炎症、腰痛を引き起こす可能性があります。石灰化は IVD に限定されず、関節軟骨などの他の軟骨組織の変性でも観察され、組織の炎症過程に関与します。さらに、IVD 石灰化は椎骨終板にも影響を及ぼし、Modic 変化 (非腫瘍性軟骨下椎骨髄病変) や痛みの発生を引き起こす可能性があります。脊椎におけるこのような影響は、変形性関節症関連の痛みに関連する膝の軟骨下骨髄病変の発生と同様の方法で発生する可能性があります。私たちは、IVD 石灰化が臨床的に関連する椎間板変性と終板変化の表現型バイオマーカーであると提案します。IVD 石灰化は脊椎変性変化の管理と予後に影響を及ぼし、脊椎の標的治療法や再生アプローチに影響を与える可能性があるため、脊椎コミュニティでは IVD 石灰化に対する認識を高める必要があります。
椎間板 (IVD) の石灰化は IVD 変性と関連しており、痛みを引き起こす可能性があります。
IVD 石灰化は、椎間板の運動学や変性の重症度に影響を与える可能性があり、隣接する椎骨終板にも影響を与える可能性があり、病的な非腫瘍性軟骨下骨髄病変(モディック変化)を引き起こす可能性があります。
IVD の変性過程における石灰化は、変形性関節症における軟骨組織の変性過程の石灰化に匹敵します。
IVD 石灰化は、臨床的に関連する独特の表現型であり、患者ケアへの個別化されたアプローチに影響を与える可能性があり、さらなる研究が必要です。
椎間板変性の遺伝的影響
椎間板変性症 (IDD) は腰痛の主な病因であると考えられており、世界中の人口の 80% 以上が人生のある時点で罹患することになります。IDD は、高い障害率と、鎮痛のための投薬、理学療法、脊椎注射、手術などの高額な治療費を生み出します 。
患者の生活に大きな影響を与えるにもかかわらず、IDD の病因と病態生理学は完全には理解されていません 。椎間板変性プロセスは人生の早い段階で始まり、細胞外マトリックス (ECM) の変化とコラーゲンとプロテオグリカンの産生の減少による老化と細胞老化に関連しています 。遺伝学、環境要因、ライフスタイルは椎間板変性の一因となります 。椎間板変性に対する遺伝的影響は最大 74% です 。肥満、毎日の喫煙、機械的負荷は、IDD に関連する独立した症状です 。反復的な物理的負荷の影響が少ないことが双子の研究で観察されました 。IDDと遺伝および環境との相関は、COL9A3多型と持続性肥満、および全身振動とIL1A-889T対立遺伝子で観察された。
外因性または内因性因子による DNA 損傷および遺伝子発現の変化は、IDD の重要なバイオマーカーとなる可能性があります。この論文の目的は、IDD に対する DNA 損傷の影響に関する文献レビューを実施して、遺伝毒性バイオマーカーを決定すること、および IDD の DNA 損傷を評価するための最良のアッセイを示すことです。
椎間板の老化と身体の老化
IDD には、老化の進行に関連した形態的および機能的変化があります 。
自然な過程において、異なる時期に異なる IVD 構造が影響を受け、それが痛みや障害の原因となり、IDD を特徴付ける病理学的状態につながる可能性があります。残念ながら、IVD を区別するための特定のバイオマーカーが不足しているため、どの IVD が症状を示すようになるかを事前に予測することはまだ不可能です。
細胞老化は、テロメア短縮の細胞周期を停止させる不可逆的な細胞老化プロセスで構成されています。椎間板の老化について受け入れられている主な仮説は、椎間板のECMを分解することによって変性を促進する、同化機構と異化機構の間の不均衡に基づいている。マトリックス分解酵素と炎症誘発性サイトカインの増加により、異化作用が同化作用を上回り、変性プロセスが促進されます 。DNA 損傷応答によって引き起こされるテロメアの進行性の減少は、不完全な DNA 複製を引き起こし、p53-p21-Rb シグナル伝達経路を活性化し、複製老化を促進します。プロテオグリカン生成とコラーゲン放出のこれらの減少は酸化ストレス環境を作り出し、活性酸素代謝物を増加させて円板細胞の増殖を阻害し、p16-Rb シグナル伝達経路を活性化して DNA 損傷に応答して円板細胞の細胞周期停止を誘導します 。
遺伝的影響の手がかり
Fengら[ 18 ]は、機械的ストレスに対する円板細胞の老化反応を研究した。この実験研究は、非生理的周期的機械的張力が、NP細胞の核におけるγ-H2A.X病巣の形成によるNPラット細胞のDNA損傷に対する直接的な遺伝的影響の効果により、細胞の早期老化を増加させることを実証した。NP 細胞の早期老化は刺激の 48 時間後に始まり、最大 12 時間の周期的な機械的張力の負荷の間、時間依存的に発生しました。このことは、椎間板への非生理学的負荷の負荷時間が長ければ長いほど、老化の影響が大きくなることを示唆しています。 DNA の損傷とその上での老化細胞の形成が考えられます 。同じ研究グループによる別の論文で、著者らは高酸素分圧の影響を評価しました。

O 2( 20%) は円板細胞老化に影響を及ぼし、活性酸素種 (ROS) の増強が p53-p21-Rb および p16-Rb 経路の上方制御により DNA 損傷を引き起こし、早期老化促進効果を媒介することを証明した 。このプロセスに関与するもう 1 つの内因性因子は、N-アセチル化プロリン-グリシン-プロリン (N-Ac-PGP) です。これは、変性ヒト NP で最近発見されたコラーゲン由来のケモカインであり、老化の進行に対する炎症の寄与を強化します。N-Ac-PGP と円板細胞老化の関係は、ラット NP 細胞のin vitro培養物で評価され、ECM 異化作用の増強、それに続く炎症カスケードと、その結果として N-Ac-PGP によって誘導される早期老化が示されました 。さらに、y-H2A.X陽性細胞の割合の上昇は、テロメラーゼ活性に影響を与えることなく、ROS産生とp53-p21-Rbおよびp16-Rb経路の両方の上方制御に関連するDNA損傷を示唆した。
ナストら は、ラットのin vivoモデルを実施して、7 週間 (ヒトでは約 3.5 年) のタバコの外因性物質への曝露を評価しました。タバコ吸入を受けたラットは、IVD において重大な変性変化とプロテオグリカン マトリックス成分の喪失を示しました。しかし、効果は軽度で有意ではなかったため、これらの発見は DNA 損傷によって部分的にのみ説明できます (p < 0.18)。脊椎変性症によく見られる椎間板栄養と血管新生の欠如は、喫煙による DNA 損傷の役割を証明するためにさらに研究される必要がある 。マウスの円板細胞における DNA 損傷は、癌治療薬メクロレタミンと電離放射線への慢性曝露でも確認されました 。これらの結果は、DNA 損傷が椎間板恒常性の喪失を引き起こし、このプロセスで主要な役割を果たし、変性カスケードを開始することを実証しました 。
周ら および Dimoziらは、酸化ストレスをシミュレートして DNA 損傷を誘発する過酸化水素 (H 2 O 2 ) の能力を評価しました。細胞老化と DNA 修復に役割を果たす重要なタンパク質であるクロモボックス ホモログ 8 (CBX8) の発現は、ラット NP 細胞における DNA 損傷の増加と相関し、II 型コラーゲンとプロテオグリカンの量の喪失および細胞増殖阻害と関連していた 。興味深いことに、これは、NP 細胞における DNA 損傷を検証するためにコメットアッセイによって DNA 損傷を評価した唯一の研究でした 。同様に、細胞毒性未満の濃度の H 2 O 2への長期曝露によって引き起こされる遺伝的影響は異化表現型を誘導し、ヒト椎間板細胞の早期老化を引き起こしました 。最後に、y-H2A.X の高度なリン酸化と細胞外マトリックス分解酵素の上方制御により、DNA 損傷が増強されることが証明されました。
この記事が気に入ったらサポートをしてみませんか?
